名校
解题方法
1 . 据报道,摩托罗拉公司曾经研制过一种由甲醇和氧气以及强碱作电解质溶液的手机电池,电量可达镍氢电池或锂电池的10倍。有关此电池的叙述错误的是
| A.正极电极反应式:O2+2H2O+4e-=4OH- |
| B.负极电极反应式:CH3OH+4OH-−4e-=CO2+4H2O |
| C.电池在使用过程中,电解质溶液的pH降低 |
| D.当外电路通过1.2mole-时,理论上消耗甲醇6.4g |
您最近一年使用:0次
名校
2 . 电催化氮气制备铵盐和硝酸盐的原理如图所示。下列说法正确的是
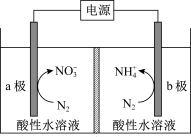

A.a极反应式为 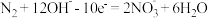 |
| B.电解一段时间,a、b两电极区的pH 均减小 |
| C.相同时间内,a、b两极消耗N2的物质的量之比为5:3 |
| D.电解过程中 H⁺从a极通过质子交换膜转移至b极 |
您最近一年使用:0次
23-24高二上·福建南平·期中
名校
解题方法
3 . 完成下列问题。
(1)电解精制饱和食盐水制取氯气、氢气、烧碱和氯的含氧酸盐等一系列化工产品。如图是离子交换膜法电解食盐水的示意图。电解精制饱和食盐水的离子方程式为___________ 。

(2)氨电解法制氢气
利用电解原理,将氨转化为高纯氮气,其装置如图所示。

电解过程中,阳极的电极方程式为___________ 。
(3)图甲是一种将废水中的氯乙烯(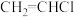 )转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
)转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。

①M为_______ (填写“正极、负极、阴极、阳极”),镀铜时,______ (填写X或Y)与铁电极相连,工作过程中,N极电极反应式___________ ,当N极有3.2g O2完全反应时,通过质子交换膜的H+的数目为___________ 。
②若M极消耗0.1mol氯乙烯,则铁电极增重___________ g,硫酸铜溶液的浓度将___________ (填写“增大、减小、不变”)
(1)电解精制饱和食盐水制取氯气、氢气、烧碱和氯的含氧酸盐等一系列化工产品。如图是离子交换膜法电解食盐水的示意图。电解精制饱和食盐水的离子方程式为

(2)氨电解法制氢气
利用电解原理,将氨转化为高纯氮气,其装置如图所示。

电解过程中,阳极的电极方程式为
(3)图甲是一种将废水中的氯乙烯(
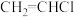 )转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
)转换成对环境无害的微生物电池装置,同时利用此装置在铁上镀铜。
①M为
②若M极消耗0.1mol氯乙烯,则铁电极增重
您最近一年使用:0次
23-24高二·全国·假期作业
解题方法
4 . 十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下列说法正确的是
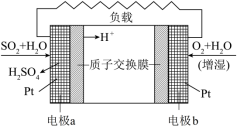

| A.该电池放电时质子从电极b移向电极a |
| B.电极a附近发生的电极反应为SO2+2H2O-2e-=H2SO4+2H+ |
| C.电极b附近发生的电极反应为O2+4e-+2H2O=4OH- |
| D.相同条件下,放电过程中消耗的SO2和O2的体积比为2∶1 |
您最近一年使用:0次
名校
解题方法
5 . 利用图所示装置可以将温室气体 转化为燃料气体
转化为燃料气体 ,下列说法中
,下列说法中不正确 的是
 转化为燃料气体
转化为燃料气体 ,下列说法中
,下列说法中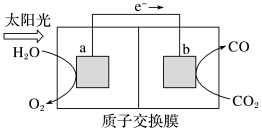
| A.该过程是将太阳能转化为化学能的过程 |
| B.电极a表面发生氧化反应 |
C.该装置工作时, 从a极区向b极区移动 从a极区向b极区移动 |
D.该装置中每生成 ,同时生成 ,同时生成 |
您最近一年使用:0次
2024-01-05更新
|
178次组卷
|
3卷引用:北京一零一中学2023-2024学年上学期11月高二统练三化学试题
北京一零一中学2023-2024学年上学期11月高二统练三化学试题(已下线)专题07 原电池-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)福建省福州超德中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
6 . 电化学原理被广泛应用于生产、生活的许多方面,利用电解法脱除煤中的含硫物质[主要成分是二硫化亚铁(FeS2)]的原理如下图所示。
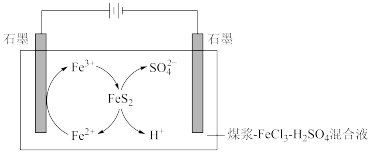
(1)阴极石墨棒上有无色气体产生,阴极的电极反应式是___________ 。
(2)补全脱硫反应的离子方程式_________ 。
 FeS2+
FeS2+ ___+
___+ ___=
___=
 +
+ ___+
___+ ___
___
(3)相同反应时间,FeCl3对脱硫率的影响如下图所示。
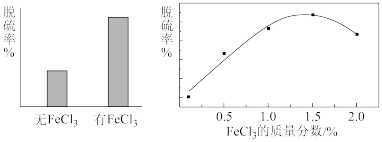
①电解脱硫过程中,FeCl3所起的作用是___________ 。
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,结合电极反应式解释可能的原因是___________ 。
(4)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率低。电解效率η的定义:η(B)= ,某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其他含硫物质,混合液中H2SO4浓度为0.01mol·L-1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(
,某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其他含硫物质,混合液中H2SO4浓度为0.01mol·L-1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c( )=0.02mol·L-1,η(
)=0.02mol·L-1,η( )=
)=___________ (忽略电解前后溶液的体积变化)。
(5)利用电解法脱硫的优点有___________ (写出一点即可)。

(1)阴极石墨棒上有无色气体产生,阴极的电极反应式是
(2)补全脱硫反应的离子方程式
 FeS2+
FeS2+ ___+
___+ ___=
___=
 +
+ ___+
___+ ___
___(3)相同反应时间,FeCl3对脱硫率的影响如下图所示。

①电解脱硫过程中,FeCl3所起的作用是
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,结合电极反应式解释可能的原因是
(4)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率低。电解效率η的定义:η(B)=
 ,某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其他含硫物质,混合液中H2SO4浓度为0.01mol·L-1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(
,某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其他含硫物质,混合液中H2SO4浓度为0.01mol·L-1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c( )=0.02mol·L-1,η(
)=0.02mol·L-1,η( )=
)=(5)利用电解法脱硫的优点有
您最近一年使用:0次
23-24高二上·福建龙岩·期中
名校
解题方法
7 . 用铅蓄电池电解 溶液,a、b电极均为石墨。已知铅蓄电池的总反应为
溶液,a、b电极均为石墨。已知铅蓄电池的总反应为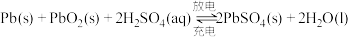 ,通电时a电极质量增加,回答下列问题:
,通电时a电极质量增加,回答下列问题:

(1)①乙中a极是该电池的___________ (填“阳极”或“阴极”)。
②甲中Y电极的电极反应式为___________ 。
(2)乙中装有 溶液,工作一段时间后,停止通电,若甲中放电时共转移
溶液,工作一段时间后,停止通电,若甲中放电时共转移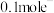 ,通电后乙中发生反应的总反应方程式为
,通电后乙中发生反应的总反应方程式为___________ ,欲使溶液恢复到起始状态,可向溶液中加入___________ (填字母),质量为___________ 。
A.Ag B. C.
C.
(3)①欲用丙装置防止金属铁被腐蚀,则金属铁应为___________ (填“c”或“d”)极。
②欲用丙装置精炼铜,则粗铜应为___________ (填“c”或“d”)极。
 溶液,a、b电极均为石墨。已知铅蓄电池的总反应为
溶液,a、b电极均为石墨。已知铅蓄电池的总反应为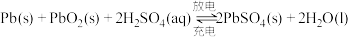 ,通电时a电极质量增加,回答下列问题:
,通电时a电极质量增加,回答下列问题:
(1)①乙中a极是该电池的
②甲中Y电极的电极反应式为
(2)乙中装有
 溶液,工作一段时间后,停止通电,若甲中放电时共转移
溶液,工作一段时间后,停止通电,若甲中放电时共转移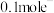 ,通电后乙中发生反应的总反应方程式为
,通电后乙中发生反应的总反应方程式为A.Ag B.
 C.
C.
(3)①欲用丙装置防止金属铁被腐蚀,则金属铁应为
②欲用丙装置精炼铜,则粗铜应为
您最近一年使用:0次
23-24高三上·江西南昌·期中
解题方法
8 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用向两侧电极分别通入NO和H2,以盐酸为电解质来进行制备,其电池装置(图1)和含Fe的催化电极反应机理(图2)如图。不考虑溶液体积的变化,下列说法正确的是
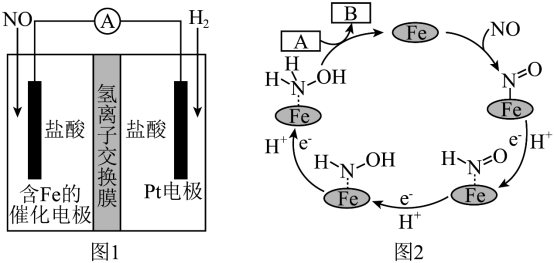

| A.电池工作时,含Fe的催化电极为正极,发生还原反应 |
B.图2中,A为H+和e-,B为 |
| C.电池工作时,每消耗标况下2.24LNO,左室溶液质量增加3.0g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
您最近一年使用:0次
9 . 将两根铂插入 的
的 溶液中进行电解,通电一段时间后,某电极质量增加
溶液中进行电解,通电一段时间后,某电极质量增加 (设电解时无
(设电解时无 放出,且不考虑水解和溶液体积变化)。此时溶液中
放出,且不考虑水解和溶液体积变化)。此时溶液中 浓度约为
浓度约为
 的
的 溶液中进行电解,通电一段时间后,某电极质量增加
溶液中进行电解,通电一段时间后,某电极质量增加 (设电解时无
(设电解时无 放出,且不考虑水解和溶液体积变化)。此时溶液中
放出,且不考虑水解和溶液体积变化)。此时溶液中 浓度约为
浓度约为A. | B. | C. | D.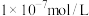 |
您最近一年使用:0次
23-24高二·全国·假期作业
解题方法
10 . 某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数数值,其实验方案的要点为:①用直流电电解氯化铜溶液,所用仪器如下图所示。②在电流强度为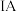 ,通电时间为
,通电时间为 后,精确测得电极上析出铜的质量为
后,精确测得电极上析出铜的质量为 。
。

试回答:
(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示。下同)
E接___________ ,C接___________ ,___________ 接F。
(2)写出B电极上发生反应的离子方程式:___________ ;G试管中淀粉 溶液变化的现象为
溶液变化的现象为___________ ,相应的离子方程式是___________ 。
(3)为精确测定电极上析出的铜的质量,所必需的实验步骤的先后顺序应是___________ 。(选填下列操作步骤的编号)
①称量电解前电极质量
②刮下电解后电极上的铜并清洗
③用蒸馏水清洗电解后的电极
④低温烘干电极后称量
⑤低温烘干刮下的铜后称量
⑥再次低温烘干后称量至恒重
(4)已知电子的电量为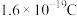 。试列出阿伏加德罗常数的计算公式:
。试列出阿伏加德罗常数的计算公式:
___________ 。
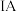 ,通电时间为
,通电时间为 后,精确测得电极上析出铜的质量为
后,精确测得电极上析出铜的质量为 。
。
试回答:
(1)连接这些仪器的正确顺序为(用图中标注仪器接线柱的英文字母表示。下同)
E接
(2)写出B电极上发生反应的离子方程式:
 溶液变化的现象为
溶液变化的现象为(3)为精确测定电极上析出的铜的质量,所必需的实验步骤的先后顺序应是
①称量电解前电极质量
②刮下电解后电极上的铜并清洗
③用蒸馏水清洗电解后的电极
④低温烘干电极后称量
⑤低温烘干刮下的铜后称量
⑥再次低温烘干后称量至恒重
(4)已知电子的电量为
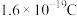 。试列出阿伏加德罗常数的计算公式:
。试列出阿伏加德罗常数的计算公式:
您最近一年使用:0次



