名校
解题方法
1 . 锌锰干电池的历史悠久,其结构如图所示。下列说法错误的是

| A.锌锰干电池属于一次电池 | B.电池工作时,锌筒为正极 |
| C.电池工作时,石墨棒不会变细 | D.电池工作时,MnO2发生还原反应 |
您最近一年使用:0次
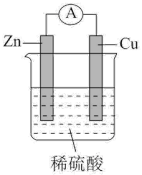
2 . 如图所示的锌 铜及稀硫酸组成的原电池中,下列有关说法正确的是
铜及稀硫酸组成的原电池中,下列有关说法正确的是
 铜及稀硫酸组成的原电池中,下列有关说法正确的是
铜及稀硫酸组成的原电池中,下列有关说法正确的是

A.锌片上有气泡产生,溶液中的 变小 变小 |
| B.电子从铜片沿导线流向锌片 |
C.稀硫酸中, 移向铜片 移向铜片 |
D.铜片上的电极反应为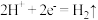 |
您最近一年使用:0次
名校
解题方法
3 . 《加快推动建筑领域节能降碳工作方案》的公布,对实现碳达峰碳中和、推动高质量发展意义重大。一种Zn-CO2电池的结构如图所示,工作时,H2O在双极膜界内解离成H+和OH-。下列说法错误的是
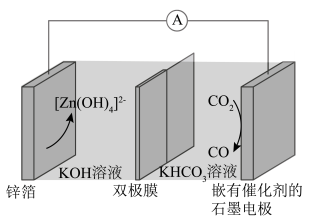
| A.双极膜中产生的H+移向石墨电极 |
| B.锌箔上发生的电极反应为Zn-2e-+4OH-=[Zn(OH)4]2- |
C.正极上的电极反应式为3CO2+2e-+H2O=2 +CO+2H+ +CO+2H+ |
| D.当外电路中转移0.2mole-时,锌箔质量减少6.5g |
您最近一年使用:0次
4 . 根据原电池原理,人们研制出了性能各异的化学电池。回答下列问题:
(1)某原电池装置示意图如图。___________ (填“Zn”或“Cu”)极经导线流向___________ 极,硫酸铜溶液浓度逐渐___________ (填“变大”或“变小”)。
②Cu片上发生的电极反应为___________ 。
③若该电池中两电极最初的总质量为500g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为498g,此时铜电极增重___________ g,该反应转移的电子的物质的量为___________ mol。
(2)由 和
和 组成的燃料电池结构如图所示。
组成的燃料电池结构如图所示。___________ 。
②当消耗1.6g甲烷时,溶液增重___________ g(忽略 的溶解)。
的溶解)。
③当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为___________ (保留3位有效数字)。
(1)某原电池装置示意图如图。
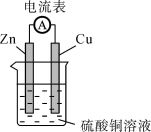
②Cu片上发生的电极反应为
③若该电池中两电极最初的总质量为500g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为498g,此时铜电极增重
(2)由
 和
和 组成的燃料电池结构如图所示。
组成的燃料电池结构如图所示。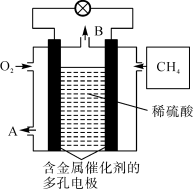
②当消耗1.6g甲烷时,溶液增重
 的溶解)。
的溶解)。③当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为
您最近一年使用:0次
9-10高二下·河北·阶段练习
解题方法
5 . (1) 电池反应通常是放热反应,下列反应在理论上可设计成原电池的化学反应是_____________ (填序号)。此类反应具备的条件是①_________ 反应,②_________ 反应。
A.C(s)+H2O(g)==CO(g)+H2(g):△H>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)==BaCl2(aq)+2NH3·H2O(l)+8H2O(l)△H>0
C.CaC2(s)+2 H2O(l)==Ca(OH)2(s)+C2H2(g);△H<0
D.CH4(g)+2O2(g)==CO2(g)+2H2O(l):△H<0
(2) 以KOH溶液为电解质溶液,依据(I)所选反应设计一个电池。其负极反应为:__________ 。
(3) 电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则
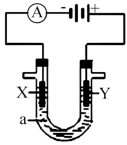
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是________ 。
②若X、Y分别为石墨和铁,a仍为饱和的NaCI溶液,则电解过程中生成的白色固体露置在空气中,可观察到的现象是__________________________ 。
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为_______________________ 。通电一段时间后,向所得溶液中加入0.05 mol Cu(OH)2,恰好恢复电解前的浓度和PH,则电解过程中电子转移的物质的量为____________ mol.
(4)利用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液。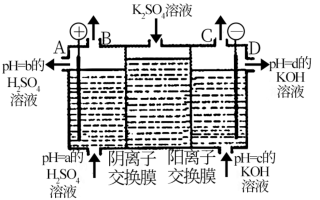
①该电解槽的阳极反应式为________ ,通过阴离子交换膜的离子数______ (填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为___________ ;
③电解一段时间后,B口与C口产生气体的质量比为_________________ 。
A.C(s)+H2O(g)==CO(g)+H2(g):△H>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)==BaCl2(aq)+2NH3·H2O(l)+8H2O(l)△H>0
C.CaC2(s)+2 H2O(l)==Ca(OH)2(s)+C2H2(g);△H<0
D.CH4(g)+2O2(g)==CO2(g)+2H2O(l):△H<0
(2) 以KOH溶液为电解质溶液,依据(I)所选反应设计一个电池。其负极反应为:
(3) 电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则

①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是
②若X、Y分别为石墨和铁,a仍为饱和的NaCI溶液,则电解过程中生成的白色固体露置在空气中,可观察到的现象是
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为
(4)利用工业上离子交换膜法制烧碱的原理,用如图所示装置电解K2SO4溶液。

①该电解槽的阳极反应式为
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为
③电解一段时间后,B口与C口产生气体的质量比为
您最近一年使用:0次
名校
6 . 原电池工作时能量转化的主要形式是
| A.化学能转化为电能 | B.电能转化为化学能 |
| C.化学能转化为热能 | D.化学能转化为光能 |
您最近一年使用:0次
名校
解题方法
7 . 化学实验是科学研究中的重要方法。
(1)如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应。将铝片加入小试管内,然后注入足量的盐酸,U形导管中液面A______ (请填写“上升”或“下降”),说明此反应是_______ (请填写“放热”或“吸热”)反应。

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中电流的流动方向为:沿导线_______ (请填写“从A流向B”或“从B流向A”)。
②装置乙中正极的电极反应式为_______ 。
③四种金属的活动性由强到弱的顺序是_____ 。
(3)将 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得 定向移向A电极,则
定向移向A电极,则___ (请填写A或B,下同)为负极,___ 处电极入口通 。
。
(1)如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应。将铝片加入小试管内,然后注入足量的盐酸,U形导管中液面A

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
| 甲 | 乙 | 丙 | |
| 装置 | 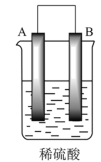 |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中电流的流动方向为:沿导线
②装置乙中正极的电极反应式为
③四种金属的活动性由强到弱的顺序是
(3)将
 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
实验测得
 定向移向A电极,则
定向移向A电极,则 。
。
您最近一年使用:0次
名校
8 . 莫尔盐 ,易溶于水,不溶于乙醇,用途广泛。
,易溶于水,不溶于乙醇,用途广泛。
某实验小组以废铁屑等为原料制备莫尔盐并设计实验检验其热分解产物。
Ⅰ.莫尔盐的制备
(1)洗涤铁屑:用热的NaOH溶液清洗废铁屑,其目的为___________ 。
(2)制备 溶液:将洗涤后的铁屑用稀硫酸溶解,为加快溶解速率,可向其中加入少量固体单质,该固体单质可以是
溶液:将洗涤后的铁屑用稀硫酸溶解,为加快溶解速率,可向其中加入少量固体单质,该固体单质可以是___________ (填化学式)。
(3)制备莫尔盐:将所得 溶液转移至蒸发皿中,加入适量
溶液转移至蒸发皿中,加入适量 固体充分溶解,再经
固体充分溶解,再经___________ 、过滤、洗涤、干燥,得产品。
(4)测定纯度
称取4.000g上述产品,配成100mL溶液,取出25.00mL置于锥形瓶中,用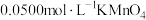 标准溶液滴定,重复三次,消耗
标准溶液滴定,重复三次,消耗 标准溶液的平均体积为10.00mL。
标准溶液的平均体积为10.00mL。
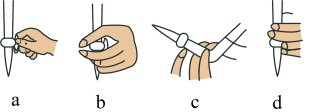
①将 标准溶液装入滴定管后,排气泡的正确操作为
标准溶液装入滴定管后,排气泡的正确操作为___________ (填选项字母)。
②经计算,该产品的纯度为___________ 。
Ⅱ.热分解产物的检验
莫尔盐自身受热分解会产生 、
、 、
、 、
、 等气体,小组同学欲用下图中装置检验其中的
等气体,小组同学欲用下图中装置检验其中的 和
和 。
。

(5)装置连接的合理顺序为___________ (填编号),装置C中盛装碱石灰的仪器名称为___________ 。
(6)D中加入的盐酸需足量,否则可能会引发的后果为___________ (用化学方程式表示)。
 ,易溶于水,不溶于乙醇,用途广泛。
,易溶于水,不溶于乙醇,用途广泛。某实验小组以废铁屑等为原料制备莫尔盐并设计实验检验其热分解产物。
Ⅰ.莫尔盐的制备
(1)洗涤铁屑:用热的NaOH溶液清洗废铁屑,其目的为
(2)制备
 溶液:将洗涤后的铁屑用稀硫酸溶解,为加快溶解速率,可向其中加入少量固体单质,该固体单质可以是
溶液:将洗涤后的铁屑用稀硫酸溶解,为加快溶解速率,可向其中加入少量固体单质,该固体单质可以是(3)制备莫尔盐:将所得
 溶液转移至蒸发皿中,加入适量
溶液转移至蒸发皿中,加入适量 固体充分溶解,再经
固体充分溶解,再经(4)测定纯度
称取4.000g上述产品,配成100mL溶液,取出25.00mL置于锥形瓶中,用
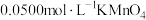 标准溶液滴定,重复三次,消耗
标准溶液滴定,重复三次,消耗 标准溶液的平均体积为10.00mL。
标准溶液的平均体积为10.00mL。
①将
 标准溶液装入滴定管后,排气泡的正确操作为
标准溶液装入滴定管后,排气泡的正确操作为②经计算,该产品的纯度为
Ⅱ.热分解产物的检验
莫尔盐自身受热分解会产生
 、
、 、
、 、
、 等气体,小组同学欲用下图中装置检验其中的
等气体,小组同学欲用下图中装置检验其中的 和
和 。
。
(5)装置连接的合理顺序为
(6)D中加入的盐酸需足量,否则可能会引发的后果为
您最近一年使用:0次
名校
解题方法
9 . 某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,部分实验结果记录如下:
根据上表中记录的实验现象,推断下列说法不正确的是
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀硫酸 | 偏向Al |
| 2 | Cu、Al | 稀硫酸 | …… |
| 3 | Mg、Al | NaOH溶液 | 偏向Mg |
| A.实验1中Al做电池的负极,发生还原反应 |
B.实验2中 在Cu极上得电子,电流表的指针偏向Cu 在Cu极上得电子,电流表的指针偏向Cu |
C.实验3中的Al电极反应式为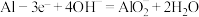 |
| D.通过以上实验说明原电池的正负电极不仅与电极的性质有关,而且与电解质溶液有关 |
您最近一年使用:0次
2023-10-03更新
|
0次组卷
|
2卷引用:河北省衡水市第二中学2023-2024学年高三上学期学科素养评估(三调)化学试题
名校
解题方法
10 . 某小组研究金属电化学腐蚀,实验如下:
下列说法正确的是
| 实验 | 装置 | 5min时现象 | 25min时现象 |
| Ⅰ | 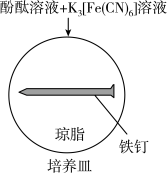 | 铁钉表面及周边未见明显变化 | 铁钉周边出现少量红色和蓝色区域,有少量红棕色铁锈生成 |
| Ⅱ | 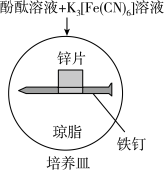 | 铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化 | 铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化 |
| A.实验Ⅱ中5min时出现红色区域,说明铁钉腐蚀速率比Ⅰ快 |
B.实验Ⅱ中正极的电极反应式为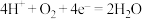 |
| C.若将Ⅱ中Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
| D.实验Ⅰ如果使用纯铁材质铁钉腐蚀速率会更快 |
您最近一年使用:0次



