解题方法
1 . 某研究性学习小组根据反应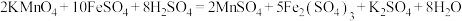 设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(1)此原电池的负极是石墨___________ (填“a”或“b”),电池工作时,盐桥中的 移向
移向___________ (填“甲”或“乙”)烧杯。
(2)正极反应式为:___________ 。
(3)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:
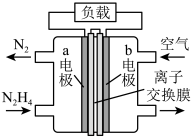
①该燃料电池中正极为___________ (填a或b)电极,负极发生的反应式为___________ 。
②当电池放电转移4 mol电子时,至少消耗燃料肼___________ g。
(4)下列反应通过原电池装置,不能实现化学能直接转化为电能的是___________ (填序号)。
A.2H2+O2 2H2O B.CaO+H2O=Ca(OH)2 C.Fe+Cu2+=Cu+Fe2+
2H2O B.CaO+H2O=Ca(OH)2 C.Fe+Cu2+=Cu+Fe2+
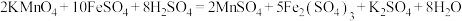 设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
回答下列问题:
(1)此原电池的负极是石墨
 移向
移向(2)正极反应式为:
(3)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:

①该燃料电池中正极为
②当电池放电转移4 mol电子时,至少消耗燃料肼
(4)下列反应通过原电池装置,不能实现化学能直接转化为电能的是
A.2H2+O2
 2H2O B.CaO+H2O=Ca(OH)2 C.Fe+Cu2+=Cu+Fe2+
2H2O B.CaO+H2O=Ca(OH)2 C.Fe+Cu2+=Cu+Fe2+
您最近一年使用:0次
2 . 随着环境问题的日益加剧,用原电池原理解决大气污染的方法得到广泛的应用。
(1)某实验室将汽车尾气(NO、NO2)转化为HNO3的原理如图1所示,其中A、B为多孔导电材料。

①A电极为__ (填“正极”或“负极”)。
②B电极附近硝酸的浓度会__ (填“增大”“减小”或“不变”)。
(2)有学者想借助如图2所示装置用原电池原理将SO2转化为重要的化工原料。若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为__ ,溶液中H+的移动方向为__ (填“M→N”或“N→M”)。

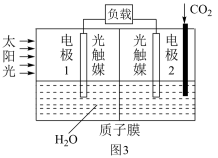
(3)为缓解温室效应,科学家利用人工模拟光合作用合成甲酸的原理为2CO2+2H2O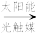 2HCOOH+O2,其装置如图3所示。电极2的电极反应式为
2HCOOH+O2,其装置如图3所示。电极2的电极反应式为__ 。若将质子膜换成阴离子交换膜,则该电池__ (填“能”或“不能”)正常工作。
(1)某实验室将汽车尾气(NO、NO2)转化为HNO3的原理如图1所示,其中A、B为多孔导电材料。

①A电极为
②B电极附近硝酸的浓度会
(2)有学者想借助如图2所示装置用原电池原理将SO2转化为重要的化工原料。若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为

(3)为缓解温室效应,科学家利用人工模拟光合作用合成甲酸的原理为2CO2+2H2O
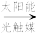 2HCOOH+O2,其装置如图3所示。电极2的电极反应式为
2HCOOH+O2,其装置如图3所示。电极2的电极反应式为
您最近一年使用:0次
解题方法
3 . 原电池反应一般是氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子,电子通过外电路输送到正极上,氧化剂在正极上得电子,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
(1)甲醇燃料电池结构简单、能量转化率高,工作原理如图1所示。加入的a是___________ (填名称),该电极的名称是___________ (填“正”或“负”)极,其电极反应式为___________ 。
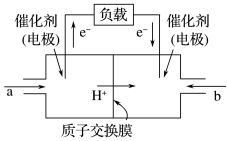
图1
(2)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图2所示。
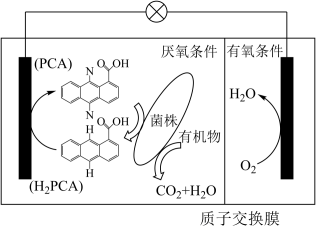
图2
①该电池的电流方向:由___________ (填“左”或“右”,下同)侧电极经过负载流向___________ 侧电极。
②当1molO2参与电极反应时,从左侧穿过质子交换膜进入右侧的H+数目为___________ NA.
(1)甲醇燃料电池结构简单、能量转化率高,工作原理如图1所示。加入的a是

图1
(2)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图2所示。

图2
①该电池的电流方向:由
②当1molO2参与电极反应时,从左侧穿过质子交换膜进入右侧的H+数目为
您最近一年使用:0次
2021-12-16更新
|
259次组卷
|
2卷引用:河南省南阳地区 2021-2022学年高二上学期 12 月阶段检测化学试题
名校
解题方法
4 . 电化学在生产生活中都具有重要的作用和意义。
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl
①该电池的负极反应式为___________ ;
②在电池中,Na+不断移动到“水”电池的___________ 极(填“正”或“负”);
③外电路每通过4 mol电子时,生成Na2Mn5O10的物质的量是___________ ;
(2)中国科学院应用化学研究所在二甲醚(CH3OCH3)燃料电池技术方面获得新突破。二甲醚燃料电池的工作原理如图所示。
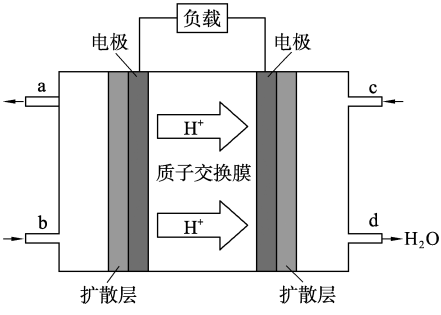
①该电池工作时,b口通入的物质为___________ ;
②该电池负极的电极反应式为___________ ;
③工作一段时间后,当9.2 g二甲醚完全反应生成CO2时,有___________ 个电子转移。
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl
①该电池的负极反应式为
②在电池中,Na+不断移动到“水”电池的
③外电路每通过4 mol电子时,生成Na2Mn5O10的物质的量是
(2)中国科学院应用化学研究所在二甲醚(CH3OCH3)燃料电池技术方面获得新突破。二甲醚燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为
③工作一段时间后,当9.2 g二甲醚完全反应生成CO2时,有
您最近一年使用:0次
5 . 空军通信卫星电源是以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2为原料的燃料电池,电极材料均采用Pt,其工作原理如图所示。回答下列问题:

(1)该燃料电池能量转化的主要形式是__ ,外电路中电子的流动方向为___ (填标号)。
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为___ 。
(3)图中离子交换膜为___ (填“阴”或“阳”)离子交换膜,电池工作时,Na+往___ (填“电极a”或“电极b”)方向迁移。
(4)每生成0.01molOH-,转移的电子数为__ NA,需要H2O2溶液(质量分数2%)的质量为___ g。
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为___ 。

(1)该燃料电池能量转化的主要形式是
①电极a→用电器→电极b;②电极b→用电器→电极a;③电极a→离子交换膜→电极b;④电极b→离子交换膜→电极a。
(2)电极a上的电极反应式为
(3)图中离子交换膜为
(4)每生成0.01molOH-,转移的电子数为
(5)若用LiAlH4代替NaBH4进行上述反应,则该电池的总反应为
您最近一年使用:0次
解题方法
6 . 利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含 废水,电解过程中溶液发生反应:
废水,电解过程中溶液发生反应: ,已知Y是循环的绿色硝化剂N2O5。如图所示:
,已知Y是循环的绿色硝化剂N2O5。如图所示:
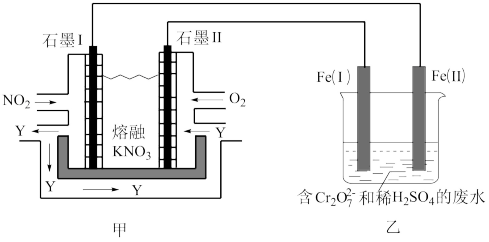
(1)以上装置中的反应共涉及___________ 种还原剂(填阿拉伯数字)。
(2)甲池工作时,电极石墨Ⅰ发生的是___________ 反应(填“氧化”或“还原”);石墨Ⅱ附近发生的电极反应式为___________ 。
(3)工作时,甲池内的 向
向___________ 移动(填“左”或“右”);在相同条件下,消耗的O2和NO2的体积比为___________ 。
(4)乙池中Fe(I)棒上消耗1.00 mol Fe,则甲池消耗标况下的氧气的体积为___________ 。
(5)若外电路中转移了1.0 mol电子,则处理废液中的 的物质的量为
的物质的量为___________ 。
 废水,电解过程中溶液发生反应:
废水,电解过程中溶液发生反应: ,已知Y是循环的绿色硝化剂N2O5。如图所示:
,已知Y是循环的绿色硝化剂N2O5。如图所示:
(1)以上装置中的反应共涉及
(2)甲池工作时,电极石墨Ⅰ发生的是
(3)工作时,甲池内的
 向
向(4)乙池中Fe(I)棒上消耗1.00 mol Fe,则甲池消耗标况下的氧气的体积为
(5)若外电路中转移了1.0 mol电子,则处理废液中的
 的物质的量为
的物质的量为
您最近一年使用:0次
7 . 用锌棒、石墨和CuCl2溶液组成的原电池,锌棒为___________ 极,其上发生___________ 反应(填“氧化”或“还原”),该电极反应式为___________ ;石墨棒为___________ 极,其上观察到的现象为___________ 。该装置在工作过程中,电子从___________ 经过___________ (填“导线”或“溶液”)流向___________ 。该原电池总反应的离子方程式为___________ 。
您最近一年使用:0次
解题方法
8 . 近段时间,全国范围内的雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。汽车尾气中含有较多的 和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。
和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。
已知:①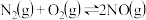
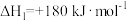
②
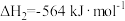
(1)请写出把汽车尾气转化为无毒无害的物质的热化学方程式:___________ 。
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
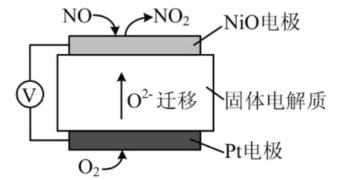
① 电极上发生的是反应
电极上发生的是反应___________ (填“氧化”或“还原”)。
②外电路中,电子的流动方向是从___________ 电极流出(填 或
或 );
); 电极上的电极反应式为
电极上的电极反应式为___________ 。
 和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。
和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。已知:①
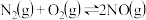
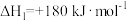
②

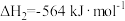
(1)请写出把汽车尾气转化为无毒无害的物质的热化学方程式:
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①
 电极上发生的是反应
电极上发生的是反应②外电路中,电子的流动方向是从
 或
或 );
); 电极上的电极反应式为
电极上的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . 探究原电池原理并应用原电池原理制作多种电池,对现实生活具有重要的意义。
(1)以CH4和O2为活性物质的甲烷燃料电池应用十分广泛。
①下图中b处通入的气体为___________ ,c电极的电极反应式为___________ 。

②下图中通入甲烷的电极的电极反应式为___________ 。
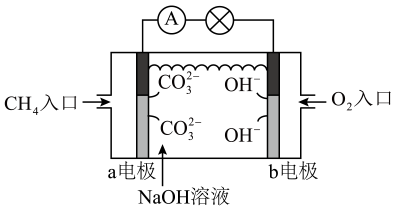
(2)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,高铁电池的研制也在进行中,模拟实验装置如图所示,实验过程中碳电极周围出现红褐色沉淀。

①该电池放电时正极的电极反应式为___________ ;
②盐桥中盛有饱和KCl琼胶,其中氯离子向___________ 移动(填“左”或“右”)。
(3)NO2、O2和熔融NaNO3可制作燃料电池,原理如图1所示。石墨Ⅰ为电池的___________ 极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为___________ 。
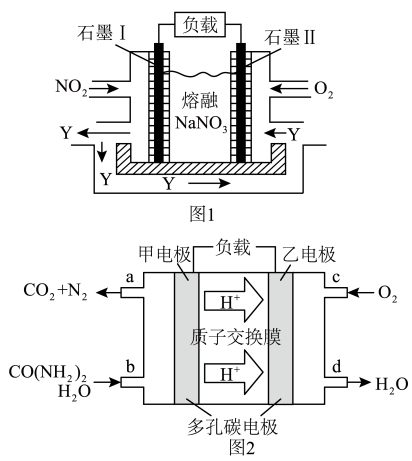
(4)化学家正在研究可净化尿素的燃料电池,原理如图2所示,甲电极的电极反应式为___________ 。
(1)以CH4和O2为活性物质的甲烷燃料电池应用十分广泛。
①下图中b处通入的气体为

②下图中通入甲烷的电极的电极反应式为

(2)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,高铁电池的研制也在进行中,模拟实验装置如图所示,实验过程中碳电极周围出现红褐色沉淀。

①该电池放电时正极的电极反应式为
②盐桥中盛有饱和KCl琼胶,其中氯离子向
(3)NO2、O2和熔融NaNO3可制作燃料电池,原理如图1所示。石墨Ⅰ为电池的

(4)化学家正在研究可净化尿素的燃料电池,原理如图2所示,甲电极的电极反应式为
您最近一年使用:0次
名校
解题方法
10 . 某化学小组探究不同条件下化学能转变为电能的装置如下图。回答问题:
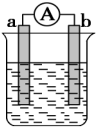
(1)若电极a为 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:_______ 。
(2)若电极a为 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置_______ (填“能”或“不能”)形成原电池。
(3)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入_______ 极(填a或b,下同),电子从_______ 极流出。电池的负极反应式为:_______ 。

(1)若电极a为
 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:(2)若电极a为
 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置(3)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入
您最近一年使用:0次
2021-10-01更新
|
305次组卷
|
3卷引用:四川省广安市武胜烈面中学校2021-2022学年高二上学期入学考试化学试题
四川省广安市武胜烈面中学校2021-2022学年高二上学期入学考试化学试题(已下线)第四章第一节 原电池(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)安徽省蚌埠第三中学2021-2022学年高二上学期10月教学质量检测化学试题



