解题方法
1 . 铅蓄电池的总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O,请回答下列问题:
2PbSO4+2H2O,请回答下列问题:
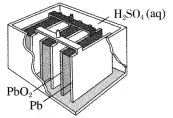
(1)放电时,正极的材料是_______ ;电解液中H2SO4浓度将变_______ (填“大”或“小”);电流方向从_______ (填“正”或“负”,下同)极流向_______ 极。当外电路通过1mol电子时,理论上负极板的质量增加_______ g。
(2)充电时Pb为_______ 极,Pb电极上的电极反应式为_______ 。
 2PbSO4+2H2O,请回答下列问题:
2PbSO4+2H2O,请回答下列问题:
(1)放电时,正极的材料是
(2)充电时Pb为
您最近一年使用:0次
2 . 燃料电池是利用燃料(如H2、CO、CH4、CH3OH、NH3等)与O2反应从而将化学能转化为电能的装置:
(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为_______ ,正极电极反应式为_______ ,放电过程中溶液的pH_______ (填“增大”“减小”或“不变”)。
(2)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠(NASICON),其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,充入气体中CO的含量越高,请回答:

①a极电极反应式为_________ 。
②工作时,O2-由电极_______ (填“a”或“b”,下同)向电极_______ 移动,电子由电极_______ 通过传感器流向电极_______ 。
(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为
(2)CO无色无味有毒,世界各国每年均有不少人因CO中毒而失去生命。一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇—氧化钠(NASICON),其中O2-可以在固体介质NASICON中自由移动。传感器中通过的电流越大,充入气体中CO的含量越高,请回答:

①a极电极反应式为
②工作时,O2-由电极
您最近一年使用:0次
解题方法
3 . 如图所示,组成一个原电池。

(1)当电解质溶液为稀硫酸时:
①Zn电极是_____ (填“正”或“负”)极,其电极反应为____ 。
②Cu电极是____ 极,其电极反应为____ 。
③电子的流向_____ 。
(2)由铜、铁和稀硫酸组成的原电池中,铁是_____ 极,电极反应式是____ ;原电池总反应方程式是____ 。(写离子方程式)。

(1)当电解质溶液为稀硫酸时:
①Zn电极是
②Cu电极是
③电子的流向
(2)由铜、铁和稀硫酸组成的原电池中,铁是
您最近一年使用:0次
23-24高一上·全国·假期作业
4 . 现有A、B、C、D四种金属片,把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向由A经过导线到C。根据上述情况,回答下列问题:
(1)在中,金属片_______ 发生氧化反应
(2)在中,金属片_______ 做负极
(3)在中,电流流动方向为_______ 。
(4)如果把B、D用导线连接后同时浸入稀硫酸溶液中,则金属片_______ 上有气泡产生
(5)上述四种金属的活动顺序是_______ 。
(1)在中,金属片
(2)在中,金属片
(3)在中,电流流动方向为
(4)如果把B、D用导线连接后同时浸入稀硫酸溶液中,则金属片
(5)上述四种金属的活动顺序是
您最近一年使用:0次
解题方法
5 . 如图是一个原电池装置,请按要求填空。
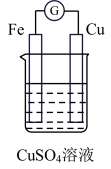
(1)正极材料是_______ ,正极发生_______ 反应。负极材料是_______ ,负极发生_______ 反应。
(2)电子的流向是由_______ (填“Fe”或“Cu”,不同)极经外电路流向_______ 极。
(3)写出电极反应式:负极_______ ,正极_______ 。
(4)原电池是一种_______ 。该原电池中发生的总反应离子方程式为_______ 。

(1)正极材料是
(2)电子的流向是由
(3)写出电极反应式:负极
(4)原电池是一种
您最近一年使用:0次
名校
6 . 某化学兴趣小组探究不同条件下化学能转化为电能的装置如图所示。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为___________ ,负极的电极反应式为___________ ,当反应中收集到标准状况下448mL气体时,电极消耗的质量为___________ g。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能。现设计一种燃料电池,以电极a为正极,电极b为负极,乙醇(C2H5OH)为燃料,氢氧化钠溶液为电解质溶液,则乙醇应通入___________ (填“a”或“b”,下同)极,溶液中OH-向___________ 极移动。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的能量直接转化为电能。现设计一种燃料电池,以电极a为正极,电极b为负极,乙醇(C2H5OH)为燃料,氢氧化钠溶液为电解质溶液,则乙醇应通入
您最近一年使用:0次
名校
7 . 某研究性学习小组的同学设计了一个原电池如图所示:
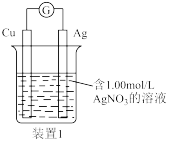
Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是_______ 极(填“正”或“负”),铜电极上发生的电极反应式是_______ 。
(2)溶液中的NO3-的移动方向为_______ (填“自右向左” 或“自左向右”)。
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为_______ 。
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为_______ 。
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应_______ (写出该反应的离子方程式)。
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下最宜 选用为该电池电解质溶液的是_______ (填标号)。
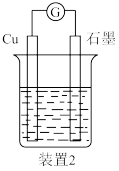
a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:
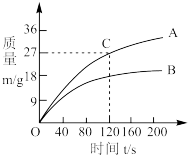
(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是_______ (填“A”或“B”) 。
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=_______ (保留2位有效数字,忽略溶液的体积变化)。

Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是
(2)溶液中的NO3-的移动方向为
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下

a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:

(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=
您最近一年使用:0次
2022-07-07更新
|
158次组卷
|
2卷引用:重庆市七校2021-2022学年高一下学期期末考试化学试题
8 . 选择适宜的材料和试剂,请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池。回答下列问题:
(1)负极材料:___ ;正极材料:___ ;电解质溶液:___ 。
(2)写出电极反应式:
正极:___ ;
负极:___ 。
(3)原电池中电子从___ 极流出,电解质溶液中阴离子流向___ 极(填“正”或“负”)。
(1)负极材料:
(2)写出电极反应式:
正极:
负极:
(3)原电池中电子从
您最近一年使用:0次
2022-03-21更新
|
780次组卷
|
2卷引用:课中-6.1.3 设计原电池、化学电源-人教2019必修第二册
名校
9 . 利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,即能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图1所示,回答问题:

(1)电流从_______ (填“左”或“右”)侧电极经过负载后流向另一电极;电极A发生_______ 反应(填“氧化”或“还原”)。
(2)为使电池持续放电,离子交换膜需选用_______ (填“阴”或“阳”)离子交换膜。
(3)A电极上的电极反应式为:_______ 。
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为_______ 。
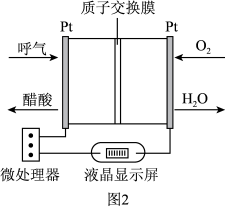
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:_______ 。

(1)电流从
(2)为使电池持续放电,离子交换膜需选用
(3)A电极上的电极反应式为:
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:

您最近一年使用:0次
名校
10 . 乙醇是一种比较理想的可用于燃料电池的有机物。乙醇来源丰富,可以通过含糖有机物的发酵进行大规模的生产。下图是以乙醇燃料电池为电源,电解含NO的废气制备HNO3示意图(c、d均为石墨电极)。
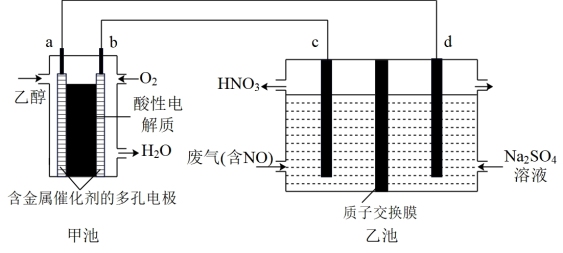
(1)请写出甲池中a极上的电极反应式:___________ 。
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。___________
(3)请写出乙池中c极上的电极反应式:___________ 。
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为___________ (标准状况);若忽略溶液体积变化,乙池右侧溶液的pH与电解前相比___________ (填“增大”、“减小”或“不变”)。

(1)请写出甲池中a极上的电极反应式:
(2)导线中电子转移的方向为___________→___________、___________ →___________ (用a、b、c、d表示)。
(3)请写出乙池中c极上的电极反应式:
(4)假设电解前,乙池两侧溶液体积均为100ml,左侧溶液中c (HNO3)为0.1 mol/L。电解结束后,左侧溶液中c (HNO3)变为0.3 mol/L,则处理NO的体积为
您最近一年使用:0次
2022-03-01更新
|
112次组卷
|
2卷引用:河北省保定市徐水综合高级中学2021-2022学年高二上学期第二次月考化学试题



