名校
解题方法
1 . (1)图1是高铁电池的模拟实验装置,放电时电池反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH
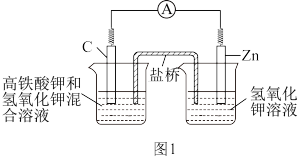

①该电池放电时正极的电极反应式为_________ 。
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向______ 移动(填“左”或“右”)。
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________________ 。
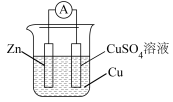
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为_______ 。
(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2 −4e−═4CO2
−4e−═4CO2
正极反应式____________ ;总电池反应_______________ 。


①该电池放电时正极的电极反应式为
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为

(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2
 −4e−═4CO2
−4e−═4CO2正极反应式
您最近一年使用:0次
名校
解题方法
2 . 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如下图所示),在每次实验时记录电压表指针的移动方向和电压表的读数如下表。已知构成两电极的金属,其金属活动性相差越大,电压表的读数越大,请依据表中数据判断:

(1)__________ 金属可能是最强的还原剂,__________ 金属一定不能从CuSO4溶液中置换出铜。
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到蓝色沉淀析出的是__________ (填字母)金属,其对应的原电池的负极反应式是__________ 。

| 金属 | 电子流动方向 | 电压/V |
| A | A→Cu | +0.78 |
| B | Cu→B | -0.15 |
| C | C→Cu | +1.35 |
| D | D→Cu | +0.03 |
(1)
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到蓝色沉淀析出的是
您最近一年使用:0次
解题方法
3 . 能源与人类的生存和发展息息相关,化学反应在人类利用能源的历史过程中充当重要的角色。回答下列问题:
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,光能转化为________ 能,水分解时断裂的化学键是________ (填“离子键”或“共价键”)
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能量为Q1kJ,断开1mol氧气中的化学键消耗的能量为Q2kJ,形成1mol水中的化学键释放的能量为Q3kJ,则下列关系正确的是____________
A.Q1+Q2<Q3 B.2Q1+Q2<2Q3 C.2Q1+Q2>2Q3 D.Q1+Q2>Q3
(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
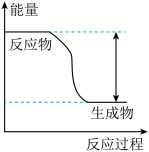
①该反应为________ 反应(填“吸热”或“放热”)。
②若要使该反应的反应速率加快,下列措施可行的是________ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
③若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______ (填“正”或“负”)极。该极上发生的电极反应为___________________ ,外电路中电子由______ 极(填“正”或“负”,下同)向______ 极移动。
(1)科学家最近研制出利用太阳能产生激光,使海水分解。太阳光分解海水时,光能转化为
(2)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。若断开1mol氢气中的化学键消耗的能量为Q1kJ,断开1mol氧气中的化学键消耗的能量为Q2kJ,形成1mol水中的化学键释放的能量为Q3kJ,则下列关系正确的是
A.Q1+Q2<Q3 B.2Q1+Q2<2Q3 C.2Q1+Q2>2Q3 D.Q1+Q2>Q3
(3)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

①该反应为
②若要使该反应的反应速率加快,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
③若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近一年使用:0次
解题方法
4 . 图是铜-锌原电池原理图:

(1)X极是__ 极(填正或负)发生____ 反应(填氧化或还原)。
(2)Y极的电极反应:___ ;原电池的总反应:___ ;电流的流动方向:___

(1)X极是
(2)Y极的电极反应:
您最近一年使用:0次
解题方法
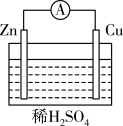
5 . 由铜、锌和硫酸溶液组成的原电池中,作正极的是____ (填化学式),正极的电极反应式为____ ;作负极的是____ (填化学式),电子由____ (填“正”或“负”,下同)极经导线移向_____ 极。

您最近一年使用:0次
2020-07-01更新
|
60次组卷
|
2卷引用:新疆吐蕃市高昌区第二中学2019-2020学年高一下学期期末考试化学试题
6 . 某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu:相对原子质量为64)。
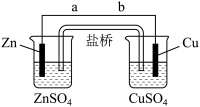
按照实验步骤依次回答下列问题:
(1)导线中电子移动方向为___ (用a、b表示)。
(2)原电池的正极为__ 。
(3)写出装置中铜电极上的电极反应式:___ 。
(4)若装置中铜电极的质量增加32g,则导线中转移的电子数目为__ 。
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向__ (填“左侧”或“右侧”)烧杯移动。

按照实验步骤依次回答下列问题:
(1)导线中电子移动方向为
(2)原电池的正极为
(3)写出装置中铜电极上的电极反应式:
(4)若装置中铜电极的质量增加32g,则导线中转移的电子数目为
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向
您最近一年使用:0次
解题方法
7 . 乙醇燃料电池采用硫酸作为电解质溶液,是一种可再生清洁的电池,电池的示意图如图,电池总反应式为C2H5OH+3O2=2CO2+3H2O。
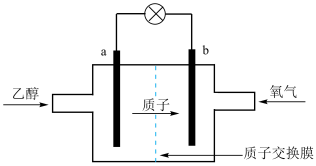
(1)a是___ 极(选“正”或“负”),发生___ 反应;电流由___ 极流向___ 极(选“a”或“b”),SO42-移向___ 极(选“a”或“b”)。
(2)随着电池的不断放电,硫酸溶液的物质的量浓度将___ 。(选“变大”或“不变”或“变小”)
(3)电池的负极电极反应式是___ 。

(1)a是
(2)随着电池的不断放电,硫酸溶液的物质的量浓度将
(3)电池的负极电极反应式是
您最近一年使用:0次
解题方法
8 . 依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如下图所示。

请回答下列问题:
(1)电极X的材料是____________ ;电解质溶液Y是__________________ 。
(2)铜电极为电池的________ 极,发生的电极反应为_______________________ X极上发生的电极反应为______________ 。
(3)外电路中的电子是从________ 极流向__________ 极(填名称)。
(4)盐桥中的Cl-向________ 极移动,如将盐桥撤掉,电流计的指针将________ 偏转。

请回答下列问题:
(1)电极X的材料是
(2)铜电极为电池的
(3)外电路中的电子是从
(4)盐桥中的Cl-向
您最近一年使用:0次
2020-02-26更新
|
144次组卷
|
3卷引用:福建省莆田市仙游县枫亭中学2019-2020学年高二上学期期中考试(选考)化学试题
名校
解题方法
9 . 依据氧化还原反应:2Ag+(aq) +Cu(s) = Cu2+(aq) +2Ag(s)
设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是________ ;电解质溶液Y是___________ ;
(2)电极反应为: 正极:___________ 负极: ___________
(3)外电路中的电子是从_______ 电极流向________ 电极。
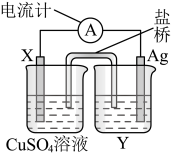
设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是
(2)电极反应为: 正极:
(3)外电路中的电子是从

您最近一年使用:0次
解题方法
10 . 在铜、锌、稀硫酸构成的原电池中(如图所示)
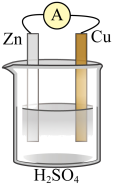
(1)负极是__________ (填“铜”或“锌”),_________ 电子(填“失去”或“得到”),发__________ (填“氧化”或 “还原”),电极反应方程式______________ ;
(2)电流由__________ 流向__________ (填“铜”或“锌),铜片上观察到的现象是________________ 。

(1)负极是
(2)电流由
您最近一年使用:0次
2019-11-28更新
|
232次组卷
|
3卷引用:陕西省西安电子科技大学附属中学2019-2020学年高二上学期期中考试化学(文)试题



