名校
1 . 上海交通大学利用光电催化脱除 与制备
与制备 相耦合,高效协同转化过程如图(在电场作用下,双极膜中间层的
相耦合,高效协同转化过程如图(在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移)。下列说法中正确的是
,并向两极迁移)。下列说法中正确的是
 与制备
与制备 相耦合,高效协同转化过程如图(在电场作用下,双极膜中间层的
相耦合,高效协同转化过程如图(在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移)。下列说法中正确的是
,并向两极迁移)。下列说法中正确的是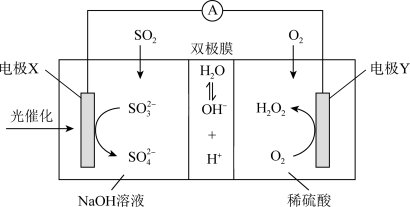
A.电流的转移方向为电极 电解质溶液 电解质溶液 电极X 电极X |
B.每消耗标准状况下 氧气,转移 氧气,转移 电子 电子 |
C.当生成 时。负极区溶液质量增重 时。负极区溶液质量增重 |
D.协同转化总反应: |
您最近半年使用:0次
名校
2 . 化学电源与我们的生活密切相关,回答下列问题:
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为_______ 。
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为_______ 极,电极上发生的是_______ (填“氧化”或“还原”)反应,铜电极反应式是_______ ;向锌电极移动的离子为_______ 。随着实验地进行,溶液质量_______ (填增加、减小或不变),若溶液质量变化2g,则转移的电子数为_______ (NA表示阿伏伽德罗的数值)。
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为

您最近半年使用:0次
3 . 锂离子电池及其迭代产品依然是目前世界上主流的手机电池。科学家近期研发的一种新型的Ca—LiFePO4可充电电池的原理示意图如图,电池反应为: ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是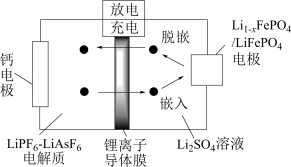
| A.放电时,钙电极为负极,发生还原反应 |
B.充电时, / / 电极的电极反应式为 电极的电极反应式为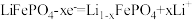 |
| C.锂离子导体膜的作用是允许Li+和水分子通过,同时保证Li+定向移动以形成电流 |
| D.充电时,当转移0.2mol电子时,理论上阴极室中电解质的质量减轻4.0g |
您最近半年使用:0次
名校
解题方法
4 . 图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是____ 。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片
E.乙溶液中 向锌片方向移动
向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为____ (填写选项字母)。
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为____ L。
(4)下列反应可以作为原电池工作时发生的反应的是:_______。
(5)乙中负极电极反应方程式为:________ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的
 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片E.乙溶液中
 向锌片方向移动
向锌片方向移动(2)变化过程中能量转化的形式主要是:甲为
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有
 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为(4)下列反应可以作为原电池工作时发生的反应的是:_______。
A.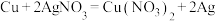 | B.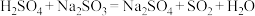 |
C. | D.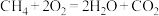 |
您最近半年使用:0次
5 . 科学家研制出了一种薄如纸片,可剪裁、能折叠的轻型“纸电池”。将特殊工艺加工后的电极材料涂在纸上,形成效率比普通锂电池效率高10倍的“纸电池”。其电池总反应为: 。下列有关说法正确的是
。下列有关说法正确的是

 。下列有关说法正确的是
。下列有关说法正确的是
A.电池的正极反应式为 |
B.涂在纸上的电极材料是 和 和 |
C.每生成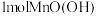 ,电池中转移 ,电池中转移 个电子 个电子 |
D.电池中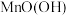 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
您最近半年使用:0次
名校
6 . 我国某大学团队通过水系电解质中氧化还原离子载流子和卤化物离子的协同作用实现 电极的六电子氧化还原反应,电池装置如图。下列说法正确的是
电极的六电子氧化还原反应,电池装置如图。下列说法正确的是 电池中单位质量的
电池中单位质量的 转移的电子数越多,电池的能量密度越大。
转移的电子数越多,电池的能量密度越大。
 电极的六电子氧化还原反应,电池装置如图。下列说法正确的是
电极的六电子氧化还原反应,电池装置如图。下列说法正确的是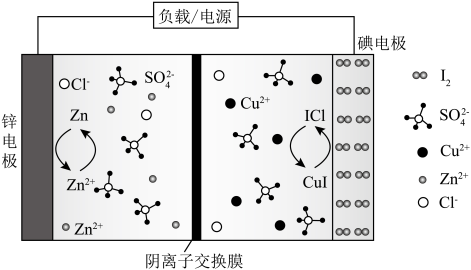
 电池中单位质量的
电池中单位质量的 转移的电子数越多,电池的能量密度越大。
转移的电子数越多,电池的能量密度越大。| A.充电时,锌电极与电源的正极相连 |
B.放电时,正极反应式为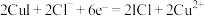 |
C.转移 的同时通过阴离子交换膜的阴离子数目不可能大于 的同时通过阴离子交换膜的阴离子数目不可能大于 |
D.与传统水系 电池的双电子氧化还原对比,图示原理的 电池的双电子氧化还原对比,图示原理的 电池的能量密度较小 电池的能量密度较小 |
您最近半年使用:0次
2024-03-13更新
|
107次组卷
|
3卷引用:江西省九江市同文中学多校联考2024届高三下学期3月月考化学试题
名校
解题方法
7 . 如图是实验室用氯化钠溶液模拟河流入海口航标灯常用的“海水-河水”电池,两极均为Ag-AgCl复合电极。下列说法错误的是
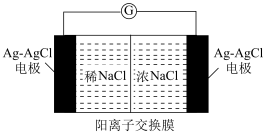

| A.右侧Ag-AgCl复合电极为负极 |
| B.利用该原理可设计检测NaCl浓度的设备 |
C.左侧电极反应为 |
| D.电池放电转移0.1mol电子,右侧电极减少10.8g |
您最近半年使用:0次
解题方法
8 . 瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 ,O2-可以在其中自由移动。下列有关叙述正确的是
,O2-可以在其中自由移动。下列有关叙述正确的是
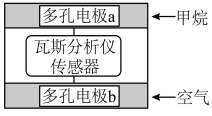
 ,O2-可以在其中自由移动。下列有关叙述正确的是
,O2-可以在其中自由移动。下列有关叙述正确的是
| A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| B.电极b是正极,O2-由电极a流向电极b |
C.电极a的反应式为: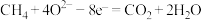 |
| D.当固体电解质中有1mol O2-通过时,电子转移4mol |
您最近半年使用:0次
9 . 有关下列四个常用电化学装置的叙述中,错误的是
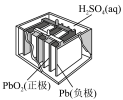 | 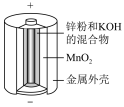 | 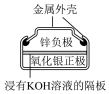 |  |
| 图1 铅-硫酸蓄电池 | 图2 碱性锌锰电池 | 图3 锌银纽扣电池 | 图4 电解精炼铜 |
| A.图1所示电池放电过程中,硫酸浓度不断减小 |
B.图2所示电池中, 参加正极反应做氧化剂 参加正极反应做氧化剂 |
C.图3所示电池中, 是氧化剂,电池工作过程中被还原为Ag 是氧化剂,电池工作过程中被还原为Ag |
D.图4所示装置工作过程中,电解质溶液中 浓度始终不变 浓度始终不变 |
您最近半年使用:0次
名校
解题方法
10 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质与NH4Cl类似。工业上主要采用电化学法制备,装置如图1所示,含Fe的催化电极反应机理如图2所示,不考虑溶液体积的变化。
下列说法正确的是

下列说法正确的是

| A.电池工作时,Pt电极为正极 |
| B.图2中,M为H+,N为NH3OH+ |
| C.电池工作时,每消耗2.24LNO左室溶液质量增加3.3g |
| D.电池工作一段时间后,正极区溶液的pH减小 |
您最近半年使用:0次
2024-02-11更新
|
134次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期1月月考化学试题



