1 . 某化学实验探究小组探究MnO2与某些盐溶液的反应,设计如图装置。左烧杯中加入50mL6mol·L-1硫酸,右烧杯中加入50mL6mol·L-1CaCl2溶液,盐桥选择氯化钾琼脂。当闭合开关K时,电流表中出现指针偏转,下列说法正确的是
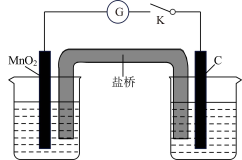
| A.该实验装置属于电解池 |
| B.左侧烧杯中的电极反应为MnO2+4H++2e-=Mn2++2H2O |
| C.右侧C电极上发生还原反应,产生的气体可使湿润的碘化钾淀粉试纸变蓝 |
| D.若将盐桥中氯化钾琼脂换成KNO3琼脂,则C电极上产生的气体的总量增加 |
您最近半年使用:0次
2 . 某原电池装置的总反应为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.电池工作时正极上发生氧化反应 |
B.装置工作时,溶液中的 向负极移动 向负极移动 |
| C.可改用Fe做电极材料 |
| D.装置工作时每转移1mol电子,将消耗64gCu |
您最近半年使用:0次
3 . 某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如表:
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)______ (填“相同”或“不相同”)。
(2)对实验3完成下列填空:
①铝为_____ 极,电极反应式:______ 。
②石墨为_____ 极,电极反应式:______ 。
③电池总反应方程式:______ 。
(3)实验4中铝作______ ,理由是______ 。写出铝电极的电极反应式:______ 。
(4)解释实验5中电流计指针偏向铝的原因:______ 。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极(正极或负极)
(2)对实验3完成下列填空:
①铝为
②石墨为
③电池总反应方程式:
(3)实验4中铝作
(4)解释实验5中电流计指针偏向铝的原因:
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素:
您最近半年使用:0次
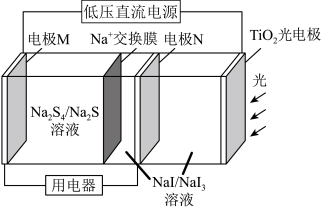
4 . 以 光电极作辅助电极,
光电极作辅助电极,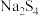 溶液和NaI溶液为初始电解液组成二次电池装置如图所示,充电时
溶液和NaI溶液为初始电解液组成二次电池装置如图所示,充电时 光电极受光激发产生电子和空穴,在空穴作用下NaI转化为
光电极受光激发产生电子和空穴,在空穴作用下NaI转化为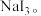 下列说法正确的是
下列说法正确的是
 光电极作辅助电极,
光电极作辅助电极,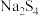 溶液和NaI溶液为初始电解液组成二次电池装置如图所示,充电时
溶液和NaI溶液为初始电解液组成二次电池装置如图所示,充电时 光电极受光激发产生电子和空穴,在空穴作用下NaI转化为
光电极受光激发产生电子和空穴,在空穴作用下NaI转化为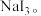 下列说法正确的是
下列说法正确的是
A.充电时,M极的电极反应式为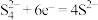 |
B.放电时, 流向M电极室 流向M电极室 |
C.空穴带正电荷,充电过程中能将 还原为 还原为 |
| D.充电过程中能量转换形式为光能最终转化为电能 |
您最近半年使用:0次
解题方法
5 . 一种利用废旧三元锂离子电池分步回收金属的实验流程如下:
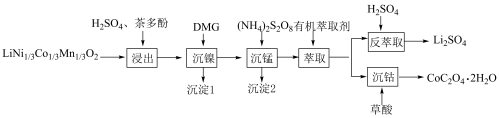
已知:
① 中元素
中元素 、
、 、
、 的价态分别为+1、+2、+3;
的价态分别为+1、+2、+3;
②室温下,几种金属离子形成氢氧化物沉淀的 如下表:
如下表:
③DMG的结构为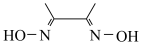 ;
;
④金属离子与有机萃取剂TBP结合能力为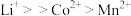 ,与P507的结合能力为
,与P507的结合能力为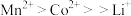 。
。
回答下列问题:
(1) 中锰元素的化合价是
中锰元素的化合价是___________ 。
(2) 可表示为LNCM,充放电时
可表示为LNCM,充放电时 分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的
分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的___________ (填“正极”或“负极”)材料。
(3)“浸出”后的溶液中过渡金属离子的化合价均为+2,茶多酚的作用是___________ 。
(4)沉淀1为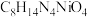 ,“沉镍”过程主要反应的离子方程式是
,“沉镍”过程主要反应的离子方程式是___________ (DMG用化学式表示),该过程中应控制溶液的 ,理论上最佳的
,理论上最佳的 不超过
不超过___________ (填序号),原因是___________ 。
A.7.2 B.8.1 C.8.7 D.10.1
(5)沉淀2为 ,“沉锰”过程主要反应的离子方程式是
,“沉锰”过程主要反应的离子方程式是___________ 。
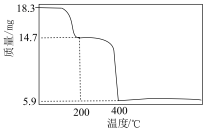
(6)有机萃取剂应选择___________ (填“TBP”或“P507”),利用 的热重图进行计算,可知400℃时的固体成分是
的热重图进行计算,可知400℃时的固体成分是___________ (填化学式)。

已知:
①
 中元素
中元素 、
、 、
、 的价态分别为+1、+2、+3;
的价态分别为+1、+2、+3;②室温下,几种金属离子形成氢氧化物沉淀的
 如下表:
如下表:| 金属离子 |  |  |  |
开始沉淀 | 8.1 | 7.2 | 7.2 |
完全沉淀 | 10.1 | 8.7 | 8.7 |
 ;
;④金属离子与有机萃取剂TBP结合能力为
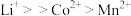 ,与P507的结合能力为
,与P507的结合能力为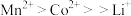 。
。回答下列问题:
(1)
 中锰元素的化合价是
中锰元素的化合价是(2)
 可表示为LNCM,充放电时
可表示为LNCM,充放电时 分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的
分别脱出、嵌入。为提高锂的回收率,回收前应对电池进行放电处理。判断LNCM是电池的(3)“浸出”后的溶液中过渡金属离子的化合价均为+2,茶多酚的作用是
(4)沉淀1为
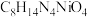 ,“沉镍”过程主要反应的离子方程式是
,“沉镍”过程主要反应的离子方程式是 ,理论上最佳的
,理论上最佳的 不超过
不超过A.7.2 B.8.1 C.8.7 D.10.1
(5)沉淀2为
 ,“沉锰”过程主要反应的离子方程式是
,“沉锰”过程主要反应的离子方程式是(6)有机萃取剂应选择
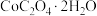 的热重图进行计算,可知400℃时的固体成分是
的热重图进行计算,可知400℃时的固体成分是
您最近半年使用:0次
6 . 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是___________ 。
(2)放电时,正极发生___________ (填“氧化”或“还原”)反应。
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为___________ 。
(4)放电时,___________ (填“正”或“负”)极附近溶液的碱性增强。
 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)已知负极反应为Zn-2e-+2OH-=Zn(OH)2,则正极反应为
(4)放电时,
您最近半年使用:0次
7 . 1910年,植物学家Potter把酵母菌或大肠杆菌放入含有葡萄糖的厌氧环境中培养,其产物能在铂电极上形成电压和电流,微生物燃料电池的研究自此开始.某科研团队借助以上理念设计了以下微生物电池,用以处理工业有机废水(以醋酸钠为例),实现能量的转化.以下说法错误的是
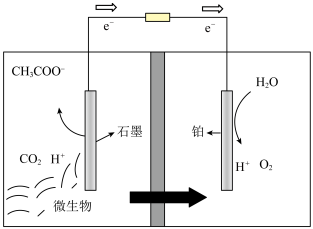

A.铂电极区域 变大导 变大导 |
| B.高温条件下能提高电池的效率 |
| C.撤去阳离子交换膜,电池电势差减小 |
D.负极电极反应: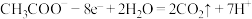 |
您最近半年使用:0次
名校
8 . i.写出下列物质在水溶液中的电离方程式:
(1) :
:___________ 。
(2)磷酸的分步电离:___________ 。
ii.向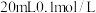 氨水中滴加
氨水中滴加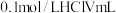 ,回答下列问题(填“>”“<”或“>”)。
,回答下列问题(填“>”“<”或“>”)。
(3)当 时,
时,
___________ 20。
(4)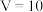 时,溶质是
时,溶质是 和
和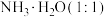 ,溶液显碱性,
,溶液显碱性,
_______ 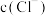 。
。
iii.利用反应 可得到清洁能源
可得到清洁能源 。
。
(5)该反应化学平衡常数表达式
___________ 。
(6)该反应的平衡常数随温度的变化如下表:
从上表可以推断:此反应是___________ (填“吸热”或“放热”)反应。
ⅳ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
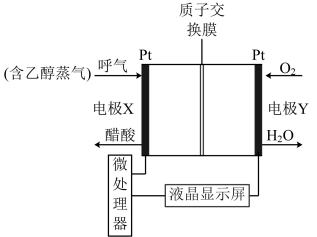
(7)电极 是该电池的
是该电池的___________ (填“正”或“负”)极。
(8)负极的电极反应式为___________ ,正极的电极反应式为___________ 。
(9)电池工作时, 通过交换膜
通过交换膜___________ (填“从左向右”或“从右向左”)迁移。
(1)
 :
:(2)磷酸的分步电离:
ii.向
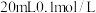 氨水中滴加
氨水中滴加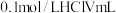 ,回答下列问题(填“>”“<”或“>”)。
,回答下列问题(填“>”“<”或“>”)。(3)当
 时,
时,
(4)
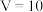 时,溶质是
时,溶质是 和
和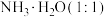 ,溶液显碱性,
,溶液显碱性,
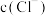 。
。iii.利用反应
 可得到清洁能源
可得到清洁能源 。
。(5)该反应化学平衡常数表达式

(6)该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数 | 10 | 9 | 1 | 0.6 |
ⅳ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

(7)电极
 是该电池的
是该电池的(8)负极的电极反应式为
(9)电池工作时,
 通过交换膜
通过交换膜
您最近半年使用:0次
解题方法
9 . 如图是牺牲阳极法保护金属的实验装置图,烧杯内为经过酸化的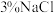 溶液。
溶液。
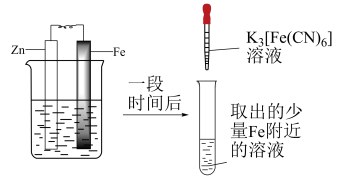
下列关于该装置的叙述错误的是
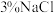 溶液。
溶液。
下列关于该装置的叙述错误的是
| A.铁作正极被保护 |
B.将 换成 换成 ,也可以保护铁不被腐蚀 ,也可以保护铁不被腐蚀 |
C.向试管中加入 溶液,无明显现象 溶液,无明显现象 |
D.正极反应式为 |
您最近半年使用:0次
名校
解题方法
10 . 微生物燃料电池能将污水中的乙二胺( )氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法正确的是
)氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法正确的是

 )氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法正确的是
)氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法正确的是
| A.燃料电池是将化学能转化为热能的装置 |
| B.电池工作时电流方向是b→a→质子交换膜→b |
| C.电池工作时,乙二胺在a电极得到电子 |
D.b电极的电极反应为 |
您最近半年使用:0次
2024-01-25更新
|
332次组卷
|
2卷引用:云南省昆明市西山区2023-2024学年高二上学期1月期末化学试题



