名校
解题方法
1 . 化学能还能转化为电能。某原电池装置如图所示。___________ 。
(2)该装置中的 是
是___________ 极,氧化反应在___________ 极附近发生(均填“正”或“负”)。请在图中画出电子的移动路径___________ 。
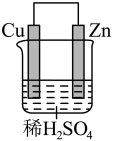
(2)该装置中的
 是
是
您最近半年使用:0次
2 . 下图是一种太阳能电池工作原理的示意图,其中电解质溶液为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液。___________ 。
(2)电池工作时,下列描述正确的是___________。
(3)正极上发生的电极反应为___________ 。
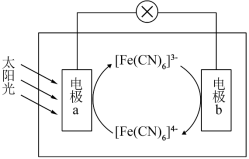
(2)电池工作时,下列描述正确的是___________。
| A.电极a为正极 | B.K+向电极a移动 |
| C.电子由电极a经导线流向电极b | D.电极b上发生氧化反应 |
您最近半年使用:0次
名校
3 . 以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能可将 转化为乙烯,工作原理如图所示。
转化为乙烯,工作原理如图所示。 为太阳能电池的
为太阳能电池的_____ 。
A.正极 B.负极
(2) 的移动方向是
的移动方向是_____ 。
A.从左至右 B.从右至左
(3)产生乙烯的电极反应式为_____ 。
 转化为乙烯,工作原理如图所示。
转化为乙烯,工作原理如图所示。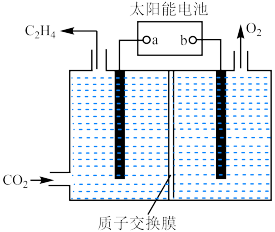
 为太阳能电池的
为太阳能电池的A.正极 B.负极
(2)
 的移动方向是
的移动方向是A.从左至右 B.从右至左
(3)产生乙烯的电极反应式为
您最近半年使用:0次
名校
4 . 某装置如图。_____ (填电极名称),B极发生反应的类型为_____ 反应(填:氧化、还原)。电流方向为_____ 时针方向(填:顺、逆)
(2)若需将反应 设计成如图所示的原电池装置,则正极电极反应式为
设计成如图所示的原电池装置,则正极电极反应式为_____ 。
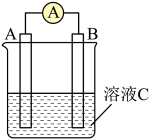
(2)若需将反应
 设计成如图所示的原电池装置,则正极电极反应式为
设计成如图所示的原电池装置,则正极电极反应式为
您最近半年使用:0次
解题方法
5 . 利用热再生氨电池可实现电解废液的浓缩再生。电池装置如下图所示,甲、乙两室均预加相同的电解废液,向甲室通入足量NH3后电池开始工作。下列说法正确的是


| A.甲室Cu电极为正极 |
| B.一段时间后,乙室电极质量增加 |
| C.仅正离子可以通过隔膜 |
| D.NH3扩散到乙室将对电池放电效率无影响 |
您最近半年使用:0次
解题方法
6 . 上海世博会新能源车展中介绍了多种新型电池,推动社会发展历程。下图是质子交换膜燃料电池工作原理,下列叙述正确的是
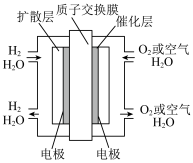

| A.通入氧气的电极发生氧化反应 | B.总反应式为 |
| C.通入氢气的电极为正极 | D.正极反应式为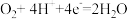 |
您最近半年使用:0次
解题方法
7 . 如图所示将锌、铜通过导线相连,置于硫酸溶液中。
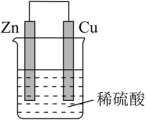
(1)该装置将___________ 能转化为___________ 能。
(2)Zn电极为___________ 极,发生___________ (填“氧化”或“还原”)反应,电极方程式为___________ 。
(3)外电路电流由___________ (填“锌”或“铜”,下同)电极经导线流向___________ 电极。
(4)标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。

(1)该装置将
(2)Zn电极为
(3)外电路电流由
(4)标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为
您最近半年使用:0次
名校
8 . 银锌钮扣电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O=Zn(OH)2+Ag,其工作示意图如下。
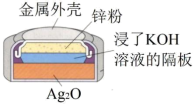
| A.该电池工作时KOH 没有发挥作用 |
| B.Ag2O电极发生还原反应 |
| C.正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH- |
| D.Zn电极是负极 |
您最近半年使用:0次
名校
解题方法
9 . I.水体酸化也是重要的环境污染问题,会造成水生动植物死亡。NaOH中和法是消除水体酸化的重要方法之一。25℃时,向某厂含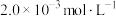 氢氟酸的废水(假设除HF外不含其它溶质)中,加入NaOH固体(忽略体积变化),得到
氢氟酸的废水(假设除HF外不含其它溶质)中,加入NaOH固体(忽略体积变化),得到 、
、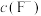 与溶液pH的变化关系,如图所示:
与溶液pH的变化关系,如图所示:
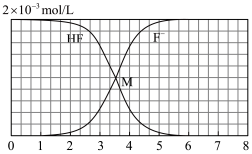
(1)两曲线交点M的纵坐标数值=___________ 。
(2)25℃时,若HF电离平衡常数为Ka,则Ka的负对数pKa=___________ 。
Ⅱ.废液中的重金属离子浓度可以用浓差电池进行测得:工作时,电池的“浓差”会逐渐减小。下图是某浓差电池的示意图:
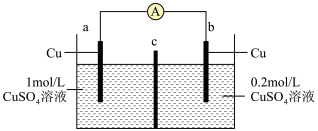
(3)a电极为___________。
(4)c膜为___________ 交换膜。
A.阴离子 B.阳离子 C.质子
(5)若此时图中电流表示数为0.01A,若将右槽中0.2mol/L的 溶液换成含
溶液换成含
 mol/L的工业废水,则此时电流表示数将
mol/L的工业废水,则此时电流表示数将___________ 0.01A。
A.大于 B.小于 C.等于
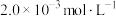 氢氟酸的废水(假设除HF外不含其它溶质)中,加入NaOH固体(忽略体积变化),得到
氢氟酸的废水(假设除HF外不含其它溶质)中,加入NaOH固体(忽略体积变化),得到 、
、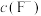 与溶液pH的变化关系,如图所示:
与溶液pH的变化关系,如图所示:
(1)两曲线交点M的纵坐标数值=
(2)25℃时,若HF电离平衡常数为Ka,则Ka的负对数pKa=
Ⅱ.废液中的重金属离子浓度可以用浓差电池进行测得:工作时,电池的“浓差”会逐渐减小。下图是某浓差电池的示意图:

(3)a电极为___________。
| A.正极 | B.负极 | C.阳极 | D.阴极 |
(4)c膜为
A.阴离子 B.阳离子 C.质子
(5)若此时图中电流表示数为0.01A,若将右槽中0.2mol/L的
 溶液换成含
溶液换成含
 mol/L的工业废水,则此时电流表示数将
mol/L的工业废水,则此时电流表示数将A.大于 B.小于 C.等于
您最近半年使用:0次
名校
解题方法
10 . 俄国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
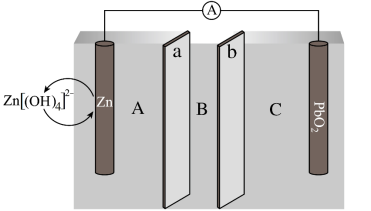
回答下列问题:
(1)电池中,Zn为_______ 极,B区域的电解质为_______ (填“K2SO4”“H2SO4”或“KOH”)。
(2)电池反应的离子方程式为_______ 。
(3)阳离子交换膜为图中的_______ 膜(填“a”或“b”)。
(4)此电池中,消耗6.5gZn,理论上可产生的容量(电量)为_______ C(1mol电子的电量为1F,F=96500C/mol,结果保留整数)。

回答下列问题:
(1)电池中,Zn为
(2)电池反应的离子方程式为
(3)阳离子交换膜为图中的
(4)此电池中,消耗6.5gZn,理论上可产生的容量(电量)为
您最近半年使用:0次
2024-02-11更新
|
133次组卷
|
2卷引用:上海市宜川中学2023-2024学年高三上学期期中考试卷(化学)



