11. 某校同学在完成铜与硝酸的分组实验后,产生大量含有H
+、Cu
2+等离子的废液,为了测定Cu
2+的浓度并对废液进行处理,进行如下实验。
I 测定废液中铜离子含量
原理:2Cu
2++4I
−=2CuI↓+I
2,I
2+
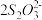
=2I
−+

步骤:①取10.00 mL废液样品,加入一定量的硫酸并煮沸。
②加入氨水调节溶液的pH=3.2 ~ 4.0,再加入过量的KI,将溶液定容为100 mL。
③取步骤②中定容后的溶液20.00 mL,淀粉作指示剂,用0.0500 mol·L
−1 Na
2S
2O
3溶液滴定,多次滴定,平均消耗Na
2S
2O
3溶液的体积为16.00 mL。
(1)步骤①加入一定量的硫酸并煮沸的目的是
_______。
(2)步骤②中溶液的pH<3.2,可能会导致测定的铜离子浓度
_______。
A.偏高
B. 偏低
C. 无影响
判断依据
_______。
(3)步骤③中所取的20.00 mL溶液应加入到
(4)计算原废液中c(Cu
2+)=
_______mol·L
−1。
Ⅱ中和沉淀法处理
已知:①该区域含铜废液的排放标准为Cu
2+的浓度不超过0.01 mg·L
−1②常温下,K
sp[Cu(OH)
2]=2.2×10
−20(5)常温下,若向废液样品中加入石灰乳至中性,判断处理后的废液能否达到排放标准
______。(写出计算过程)
(6)向废液样品中滴加氨水,调节溶液的pH,铜去除率与溶液pH的关系,如图所示。解释pH由7到10时,铜去除率下降的主要原因
_______。
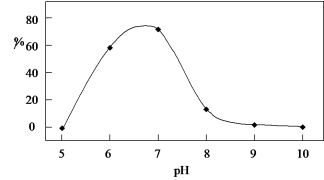
Ⅲ硫化物沉淀法处理
已知:常温下K
a1(H
2S)=1.3×10
−7、K
a2(H
2S)=7.0×10
−15、K
sp(CuS)=6.4×10
−36(7)常温下,调节Na
2S溶液的pH=7,比较溶液中含硫微粒浓度的大小
_______。
(8)常温K
sp(FeS)=6.3×10
−18,下列说法正确的是
| A.常温下,CuS的溶解度大于FeS |
| B.反应Cu2++H2S=CuS↓+2H+不能发生 |
| C.除去废液中的Cu2+,可选用FeS作沉淀剂 |
| D.常温下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)减小 |
Ⅳ溶剂萃取法
用萃取剂RH(一种有机酸)可萃取废液中的Cu
2+,有机层能形成较高浓度的含铜配合物,向分离出的有机层中加入20%的H
2SO
4溶液进行反萃取,可以回收铜。
(9)实验室进行萃取操作时,需对分液漏斗放气,正确放气的图示为
(10)用RH萃取时,适度增大溶液的pH,Cu
2+萃取率会升高的原因是
_______。