名校
解题方法
1 . 纤维电池的发明为可穿戴电子设备的发展奠定了基础。一种纤维状钠离子电池放电时的总反应为: Na0.44MnO2+NaTi2(PO4)3 = Na0.44-xMnO2+Na1+xTi2(PO4)3,其结构简图如图所示。下列说法错误的是
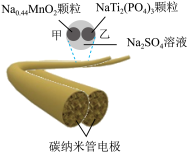
A.放电时, 向乙电极移动 向乙电极移动 |
| B.放电时乙电极的电极反应式为:NaTi2(PO4)3+xe-+xNa+ =Na1+xTi2(PO4)3 |
| C.该电池充电时甲电极应该与电源负极相连 |
| D.该电池充电过程中Mn元素的化合价降低 |
您最近一年使用:0次
2023-04-08更新
|
701次组卷
|
4卷引用:新疆维吾尔自治区乌鲁木齐市2023届高三下学期第二次质量检测理综化学试题
新疆维吾尔自治区乌鲁木齐市2023届高三下学期第二次质量检测理综化学试题(已下线)狂飙卷 03 -【热题狂飙】2023年高考化学样卷(全国卷专用)宁夏回族自治区银川一中2023届高三下学期第三次模拟理科综合化学试题(已下线)选择题11-14
名校
解题方法
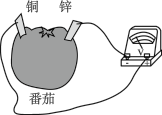
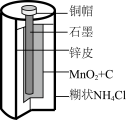
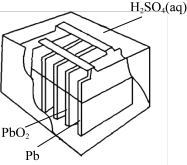
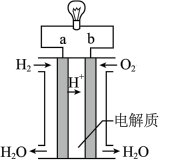
2 . 下列四个常用电化学装置的叙述错误的是
|
|
|
|
| 图I水果电池 | 图II干电池 | 图III铅蓄电池 | 图IV氢氧燃料电池 |
| A.图I所示电池中,电子从锌片流出 |
| B.图II所示干电池中锌作负极 |
C.图III所示电池为二次电池,放电时正极的电极反应式为Pb-2e-+ =PbSO4 =PbSO4 |
D.图IV所示电池中正极反应为: |
您最近一年使用:0次
2023-03-25更新
|
1963次组卷
|
9卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题
新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题四川省内江市第六中学2022-2023学年高一下期第一次月考(创新班)化学试题广东省广州市天河区第八十九中学2022~2023学年高一下学期期中考试化学选考试题安徽省合肥市第一中学2022-2023学年高一下学期第4次月考化学试题(已下线)【2023】【高一下】【期中考】【学军紫金港】【高中化学】【洪翔峰收集】云南省昆明市官渡区第三中学2022-2023学年高一下学期期中考试化学试题四川省南充市嘉陵第一中学2022-2023学年高一下学期4月期中考试化学试题云南省开远市第一中学校2022-2023学年高一下学期4月月考化学试题河北省唐山市开滦第二中学2023-2024学年高一下学期4月月考化学试题
3 . 某种电池充放电时的反应原理为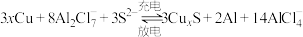 。下列物质为放电时负极产物的是
。下列物质为放电时负极产物的是
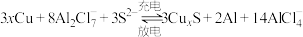 。下列物质为放电时负极产物的是
。下列物质为放电时负极产物的是A. | B. | C. | D. |
您最近一年使用:0次
2023-02-15更新
|
442次组卷
|
2卷引用:新疆生产建设兵团第二师八一中学2022-2023学年高一下学期期末考试化学试题
名校
4 . 电子表和电子计算器的电源通常用微型银—锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应式为Ag2O+H2O+Zn=Zn(OH)2+2Ag。下列说法正确的是
| A.Ag2O是正极,Zn是负极 |
| B.锌电极上发生的电极反应为Zn-2e-=Zn2+ |
| C.工作时,电池负极区溶液pH增大 |
| D.工作时,电子由Ag2O极经外电路流向Zn极 |
您最近一年使用:0次
2023-02-15更新
|
127次组卷
|
2卷引用:新疆哈密市第八中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
5 . M、N、P、E四种金属,已知:①M+N2+=N+M2+;②M、P用导线连接放入硫酸氢钠溶液中,M表面有大量气泡逸出;③N、E用导线连接放入E的硫酸盐溶液中,电极反应为E2++2e-=E,N-2e-=N2+。则这四种金属的还原性由强到弱的顺序是
| A.P>M>N>E | B.E>N>M>P | C.P>N>M>E | D.E>P>M>N |
您最近一年使用:0次
2023-01-16更新
|
445次组卷
|
11卷引用:新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题
新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题陕西省西安交通大学附属中学分校2021-2022学年高一下学期期中考试化学试题辽宁省重点高中沈阳市联合体2021-2022高一下学期期中考试化学试题云南省腾冲市第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第16讲 原电池 新型电源 (练)-2023年高考化学一轮复习讲练测(新教材新高考)河北省石家庄市第四十二中学2022-2023高二上学期10月月考化学试题西藏拉萨那曲高级中学2020-2021学年高二下学期期中考试化学试题(已下线)第六章 化学反应与能量 第35练 原电池 化学电源四川省青神中学校2022-2023学年高二下学期3月月考化学试题第1课时 原电池的工作原理(已下线)第3讲 原电池 化学电源
6 . 1905年哈伯实现了以氮气和氢气为原料合成氨气,生产的氨制造氮肥服务于农业,养活了地球三分之一的人口,哈伯也因此获得了1918年的诺贝尔化学奖。一百多年过去了,对合成氨的研究依然没有止步。
(1)已知在一定温度下进行的化学反应,反应所释放或吸收的能量称为该温度下的反应热。反应热用符号△H表示;△H =反应物断键吸收总能量-生成物成键放出总能量,若△H<0为放热反应,△H>0为吸热反应。如H2和O2反应: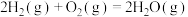 放热,且断开1 mol H-H键、1mol O=O键、1 molO-H键需吸收的能量分别为
放热,且断开1 mol H-H键、1mol O=O键、1 molO-H键需吸收的能量分别为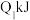 、
、 、
、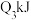 ,可推知△H数值
,可推知△H数值 ,则反应中能量变化为
,则反应中能量变化为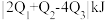 。对工业合成氨的反应如下:
。对工业合成氨的反应如下: ,已知断裂1 mol N2中的共价键吸收的能量为947 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2(g)和H2 (g)生成1 mol NH3(g)的能量变化为
,已知断裂1 mol N2中的共价键吸收的能量为947 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2(g)和H2 (g)生成1 mol NH3(g)的能量变化为_______ kJ;下图能正确表示该反应中能量变化的是_________ (填“A”或“B”)。
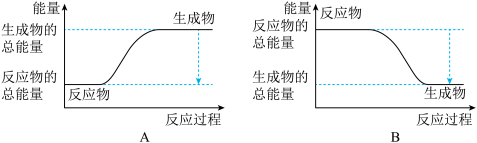
(2)反应 在三种不同条件下进行,N2、N2的起始浓度为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
在三种不同条件下进行,N2、N2的起始浓度为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
根据上表数据回答:实验①②中,有一个实验使用了催化剂,它是实验_______ (填序号);实验③达平衡时NH3的转化率为_______ 。在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_______ (填字母)。
a.NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
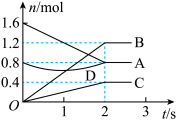
(3)某温度下,在体积为3 L的容器中,A、B、C三种气体物质物质的量随着时间变化的关系如图所示,则①该反应的化学方程式为_______ ,②反应开始至2 s时,B的平均反应速率为_______ 。
(4)氢气是未来最理想的能源。科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用下使海水分解得到氢气的新技术: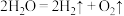 ,制得的氢气可用于制作燃料电池。试回答下列问题:
,制得的氢气可用于制作燃料电池。试回答下列问题:
①某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为 ,则A极是电池的
,则A极是电池的_______ 极。
②一种人工合成汽油的方法是先将煤制成CO和H2,然后在一定条件下将CO与H2转化为碳原子数为5~8的烷烃(人工合成汽油)。若以CnH2n+2表示人工合成汽油的成分,请写出用CO与H2制取CnH2n+2的化学方程式_______ 。
(1)已知在一定温度下进行的化学反应,反应所释放或吸收的能量称为该温度下的反应热。反应热用符号△H表示;△H =反应物断键吸收总能量-生成物成键放出总能量,若△H<0为放热反应,△H>0为吸热反应。如H2和O2反应:
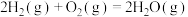 放热,且断开1 mol H-H键、1mol O=O键、1 molO-H键需吸收的能量分别为
放热,且断开1 mol H-H键、1mol O=O键、1 molO-H键需吸收的能量分别为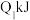 、
、 、
、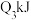 ,可推知△H数值
,可推知△H数值 ,则反应中能量变化为
,则反应中能量变化为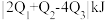 。对工业合成氨的反应如下:
。对工业合成氨的反应如下: ,已知断裂1 mol N2中的共价键吸收的能量为947 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2(g)和H2 (g)生成1 mol NH3(g)的能量变化为
,已知断裂1 mol N2中的共价键吸收的能量为947 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2(g)和H2 (g)生成1 mol NH3(g)的能量变化为
(2)反应
 在三种不同条件下进行,N2、N2的起始浓度为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
在三种不同条件下进行,N2、N2的起始浓度为0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。| 实验序号 | 时间浓度温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| ① | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| ② | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| ③ | 500℃ | 1.0 | 0.40 | 0.25 | 0.15 | 0.15 | 0.15 | 0.15 |
a.NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
(3)某温度下,在体积为3 L的容器中,A、B、C三种气体物质物质的量随着时间变化的关系如图所示,则①该反应的化学方程式为

(4)氢气是未来最理想的能源。科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用下使海水分解得到氢气的新技术:
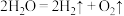 ,制得的氢气可用于制作燃料电池。试回答下列问题:
,制得的氢气可用于制作燃料电池。试回答下列问题:①某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为
 ,则A极是电池的
,则A极是电池的②一种人工合成汽油的方法是先将煤制成CO和H2,然后在一定条件下将CO与H2转化为碳原子数为5~8的烷烃(人工合成汽油)。若以CnH2n+2表示人工合成汽油的成分,请写出用CO与H2制取CnH2n+2的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 有一种新型电池既可以实现海水淡化,又可以进行废水处理,还能获得电能。下列装置处理含 的废水。下列说法正确的是
的废水。下列说法正确的是
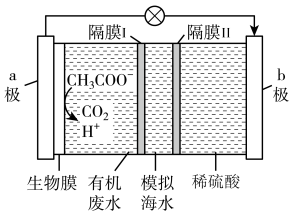
 的废水。下列说法正确的是
的废水。下列说法正确的是
| A.a极为负极,发生还原反应 |
B. 通过隔膜II进入右室 通过隔膜II进入右室 |
C.负极反应为 |
D.若处理含有29.5g 的废水,模拟海水理论上可除NaCl 234g 的废水,模拟海水理论上可除NaCl 234g |
您最近一年使用:0次
2022-12-24更新
|
662次组卷
|
4卷引用:新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
8 . 有A、B、D、E四种金属,当A、B组成原电池时,电子流动方向A→B;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
| A.A﹥B﹥E﹥D | B.A﹥B﹥D﹥E |
| C.D﹥E﹥A﹥B | D.D﹥A﹥B﹥E |
您最近一年使用:0次
2022-12-20更新
|
834次组卷
|
49卷引用:新疆昌吉教育共同体2020-2021学年高一下学期期中考试化学试题
新疆昌吉教育共同体2020-2021学年高一下学期期中考试化学试题新疆霍城县第二中学2022-2023学年高二上学期(线上)期中考试化学试题新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题(已下线)2010年福建省福州市八县(市)协作校第一学期期中联考高二理科化学试卷(已下线)2011学年浙江省瑞安十校高二第二学期期中联考化学试卷(已下线)2013-2014学年福建省长乐二中等五校高二上学期期中考试化学试卷(已下线)2014年高一下学期化学必修2 2-2-1 化学能转化为电能练习卷2014-2015浙江省温州市十校联合体高一下学期期中化学试卷2015-2016学年河北省容城中学高二上学期第一次月考化学试卷2015-2016学年青海省平安一中高二下期末化学试卷2016-2017学年西藏拉萨中学高二上月考三化学卷河北省张家口市第一中学2016-2017学年高一(实验班、普通班)6月月考(文)化学试题内蒙古包头市铁路一中2016-2017学年高二下学期期末考试化学试题山东省枣庄市第八中学南校区高二10月份月考化学试题山东省垦利第一中学2017-2018学年高二上学期第一次月考化学试题宁夏银川一中2017-2018学年高二下学期期中考试化学试题吉林省榆树一中2017-2018学年高一下学期期末考试化学试题2017-2018学年人教新版高一化学必修一第三章第一节基础题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期开学考试化学试题【全国百强校】内蒙古第一机械制造(集团)有限公司第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安第四中学2018-2019学年高二上学期12月月考化学试题山西省晋中市祁县第二中学校2018-2019学年高一下学期期中考试化学试题江苏省海安高级中学2019-2020学年高二上学期入学考试化学试题四川省泸州市泸县第五中学2019-2020学年高二上学期期中考试化学试题山西省应县第一中学校2019-2020学年高二上学期第四次月考化学试题河北省唐山市遵化市第一中学2019-2020学年高二上学期第一次月考化学试题辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题四川省棠湖中学2019-2020学年高一下学期期中考试化学试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(实验班)试题高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 课时1 原电池的工作原理吉林省长春市农安县2019-2020学年高一下学期期末考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期开学考试化学试题安徽省六安市新安中学2020-2021学年高二上学期期末考试(普通班)化学试题安徽省六安市新安中学2020-2021学年高二下学期入学考试(普通班)化学试题福建省南安市柳城中学2020-2021学年高二上学期第一次月考化学试题福建省南安市柳城中学2020-2021学年高二上学期期中考试化学试题吉林省“BEST合作体”2020-2021学年高一下学期期中化学试题河南省济源市第五中学2020-2021学年高二下学期6月月考化学试题选择性必修1专题1第二单元 课时1 原电池的工作原理福建省泉州市永春第一中学2021-2022学年高二上学期9月线上考试化学试题陕西省西北农林科技大学附属中学2021-2022学年高一下学期期中考试化学试题吉林省长春市第二实验中学 2021-2022 学年高一下学期期中考试化学试题江苏省连云港高级中学2022-2023高二上学期第一次阶段测试化学试题四川省广安代市中学校2020-2021学年高一下学期第三次月考化学试题福建省平潭翰英中学2022-2023学年高二上学期第一次月考化学试题福建省平潭翰英中学2021-2022学年高二上学期第一次月考(选考)化学试题四川省成都东部新区养马中学2020-2021学年高一下学期期中考试化学试题1.2.1原电池的工作原理 课中四川省成都市西南交通大学附属中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
9 . 某科学家用含食盐水的湿抹布夹在银板和锌板的圆形板中间,堆积成圆柱状,制造出最早的电池一伏打电池(如图)。下列叙述正确的是
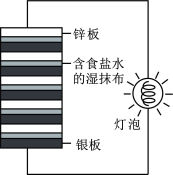

| A.该电池中电子由银极经导线流向锌极 |
B.银极上消耗 (标准状况下)氧气时,转移 (标准状况下)氧气时,转移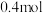 电子 电子 |
| C.若用稀硫酸替代食盐水,则在正极放电的物质不变 |
D.该电池负极的电极反应式为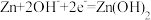 |
您最近一年使用:0次
2022-10-28更新
|
517次组卷
|
8卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
解题方法
10 . 根据原电池原理,结合装置图,按要求解答问题:

(1)若X为Zn,Y为硫酸铜溶液,则X为_______ (填电极名称),判断依据:_______ ;铜电极的名称是_______ ,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(2)若X为银,Y为硝酸银溶液,则X为_______ (填电极名称),判断依据:_______ ;铜电极的名称是_______ ,溶液中的Ag+移向_______ (填“Cu”或“X”)电极。
(3)若X为Fe,Y为浓硝酸,则Cu为_______ (填电极名称),铜电极可能观察到的现象是_______ ;X电极的名称是_______ 。

(1)若X为Zn,Y为硫酸铜溶液,则X为
(2)若X为银,Y为硝酸银溶液,则X为
(3)若X为Fe,Y为浓硝酸,则Cu为
您最近一年使用:0次