名校
解题方法
1 . 由锌片、铜片和 稀硫酸组成的原电池如图所示。
稀硫酸组成的原电池如图所示。
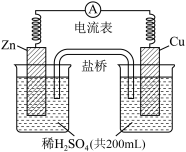
(1)原电池的负极反应式为_______ ,正极反应式为_________ 。
(2)电流的方向是_____ 。
(3)一段时间后,当在铜片上放出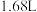 (标准状况)气体时,
(标准状况)气体时, 恰好消耗一半。则产生这些气体的同时,共消耗
恰好消耗一半。则产生这些气体的同时,共消耗____ g锌,有_____ 个电子通过了导线,原稀硫酸的物质的量浓度是______ (设 为阿伏加 德罗常数的值,溶液体积不变)。
为阿伏加 德罗常数的值,溶液体积不变)。
 稀硫酸组成的原电池如图所示。
稀硫酸组成的原电池如图所示。
(1)原电池的负极反应式为
(2)电流的方向是
(3)一段时间后,当在铜片上放出
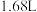 (标准状况)气体时,
(标准状况)气体时, 恰好消耗一半。则产生这些气体的同时,共消耗
恰好消耗一半。则产生这些气体的同时,共消耗 为阿伏加 德罗常数的值,溶液体积不变)。
为阿伏加 德罗常数的值,溶液体积不变)。
您最近一年使用:0次
2020-09-12更新
|
252次组卷
|
5卷引用:鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 综合训练
鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 综合训练高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 第一节综合训练(已下线)4.1.1 原电池的工作原理(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北阜城中学2020-2021学年高二上学期期中考试化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题
名校
解题方法
2 . 有关电化学知识的描述正确的是

A.反应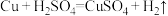 可设计成原电池 可设计成原电池 |
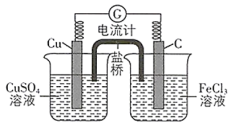
B.利用 ,可设计如图所示原电池装置,盐桥内 ,可设计如图所示原电池装置,盐桥内 向 向 溶液移动 溶液移动 |
C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中组成原电池,铁作负极,铜作正极,其负极反应式为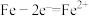 |
D.由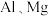 与氢氧化钠溶液组成的原电池,其负极反应式为 与氢氧化钠溶液组成的原电池,其负极反应式为 |
您最近一年使用:0次
2020-09-12更新
|
1019次组卷
|
11卷引用:【校级联考】福建省福州八县一中2018-2019学年高二上学期期中考试化学试题
【校级联考】福建省福州八县一中2018-2019学年高二上学期期中考试化学试题【校级联考】山西省陵川第一中学、高平一中、阳城一中2018-2019学年高二上学期第三次月考化学试题【校级联考】天津市七校(静海一中、宝坻一中、杨村一中等)2018-2019学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第2节 化学能转化为电能——电池 课时1 原电池的工作原理福建省泰宁第一中学2018-2019学年高二上学期第二阶段考试化学(理)试题高中必刷题高二选择性必修1第四章 化学反应与电能 第一节 原电池 课时1 原电池的工作原理人教版(2019)高二选择性必修第一册 第四章 化学反应与电能 第一节 原电池 教材帮辽宁省辽河油田第二高级中学2022-2023学年高二上学期期末考试化学试题选择性必修1专题1第二单元 课时1 原电池的工作原理河北省衡水市第十四中学2021-2022学年高二上学期二调考试化学试题1.2.1原电池的工作原理 课后
名校
解题方法
3 . 如图是某同学设计的一个简易的原电池装置,请回答下列问题。
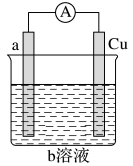
(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为___________________ ,当有3.2g的负极材料溶解时,导线中转移的电子的数目为________ 。
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为_________________ ,该燃料电池的优点是_______________________ 。
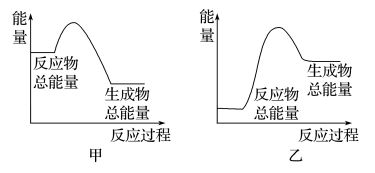
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可________ (填“吸收”或“放出”)热量________ kJ;该反应的能量变化可用图______ (填“甲“或“乙”)表示。

(1)若a电极材料为碳、b溶液为FeCl3溶液,则正极的电极反应式为
(2)氢氧燃料电池已用于航天飞机。这种电池以30%KOH溶液为电解质溶液,供电时总反应为2H2+O2===2H2O,则正极的电极反应式为
(3)已知H—H键、N—H键、N≡N键的键能分别为436kJ·mol-1、391kJ·mol-1、946kJ·mol-1,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有1molNH3生成,可

您最近一年使用:0次
名校
解题方法
4 . 由下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴加浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2>Co2O3 |
| B | 在镁、铝为电极,氢氧化钠为电解质的原电池装置 | 镁表面有气泡 | 金属活动性:Al>Mg |
| C | 测定等物质的量浓度的NaCl与Na2CO3溶液的pH | 后者较大 | 非金属性:Cl>C |
| D | 将10 mL 2 mol/L的KI溶液与1 mL 1 mol/L FeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 某原电池装置如图所示。下列有关叙述中正确的是( )
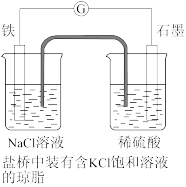
| A.电池工作中,盐桥中的Cl-向负极移动 |
| B.负极反应式:2H++2e-=H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.Fe作正极,发生氧化反应 |
您最近一年使用:0次
2020-08-27更新
|
259次组卷
|
8卷引用:2016-2017学年福建省四地六校高二上第一次月考化学试卷
2016-2017学年福建省四地六校高二上第一次月考化学试卷(已下线)1.2.1 原电池的工作原理 练习《新教材同步备课》(鲁科版选择性必修1)辽宁省鞍山市第一中学2023-2024学年高一下学期第一次月考化学试卷(已下线)第16讲 原电池 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)江苏省泰州中学2021-2022学年高二上学期第一次月度检测化学试题河南省宋基信阳实验中学2021-2022学年高三上学期12月月考化学试题云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题第1课时 原电池的工作原理
名校
解题方法
6 . 已知铅蓄电池充放电的总反应为Pb+PbO2+2H2SO4 2H2O+2PbSO4,下列关于铅蓄电池的说法正确的是( )
2H2O+2PbSO4,下列关于铅蓄电池的说法正确的是( )
 2H2O+2PbSO4,下列关于铅蓄电池的说法正确的是( )
2H2O+2PbSO4,下列关于铅蓄电池的说法正确的是( )| A.在放电时,两极质量均增加 |
| B.在充电时,电池中硫酸的浓度不断变小 |
C.在放电时,负极发生的反应是Pb+2e-+SO =PbSO4 =PbSO4 |
D.在放电时,正极发生的反应是PbSO4+2e-=Pb+SO |
您最近一年使用:0次
2020-08-25更新
|
194次组卷
|
4卷引用:辽宁省沈阳铁路实验中学2016-2017学年高一下学期期中考试化学试题
7 . 如图是锌片和铜片与稀硫酸组成的原电池装置a、b为两个电极。下列判断正确的是
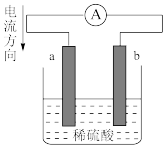

| A.电池工作时,化学能全部转化为电能 |
B.电池工作时,溶液中 浓度基本不变 浓度基本不变 |
| C.b电极为锌片,发生氧化反应 |
D.电池工作时,溶液中 向b电极移动 向b电极移动 |
您最近一年使用:0次
解题方法
8 . 下面是某同学学习原电池后整理的学习笔记,出现错误有
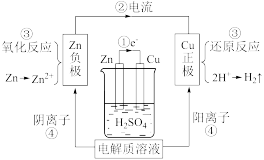 | 图注释: ①电子流动方向(一定)②电流方向(一定) ③电极反应(一定)④溶液中离子移动方向(一定) 拓展: ⑤负极金属活动性较强(一定) ⑥负极溶解质量减少,正极产生气体或质量增加变粗(不一定) |
| A.0处 | B.1处 | C.2处 | D.4处 |
您最近一年使用:0次
名校
解题方法
9 . 铜锌原电池装置如图所示,有关说法正确的是
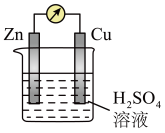

| A.锌片作正极 | B.铜片上产生气泡 |
| C.可将电能转化成化学能 | D.电子由铜片经溶液流向锌片 |
您最近一年使用:0次
2020-08-17更新
|
409次组卷
|
4卷引用:辽宁省大石桥市第三高级中学2020-2021学年高二12月月考化学试题
名校
解题方法
10 . 某种氨硼烷(NH3·BH3)电池装置如图所示(未加入氨硼烷之前,两极室内液体质量相等),电池反应为NH3∙BH3+3H2O2=NH4BO2+4H2O(不考虑其他反应的影响)。已知:质子交换膜只能允许H+通过。下列说法正确的是( )


| A.负极的电极反应式为H2O2+2H++2e-=2H2O |
| B.电池中电子由a经由导线流入b |
| C.电池工作时H+由右侧极室经质子交换膜进入左侧极室 |
| D.若加入的氨硼烷全部放电后左右两极室内液体质量差为3.8g,则电路中转移1.2mol电子 |
您最近一年使用:0次
2020-08-12更新
|
600次组卷
|
2卷引用:辽宁省东北育才学校2019-2020学年高一下学期期末考试化学试题



