名校
解题方法
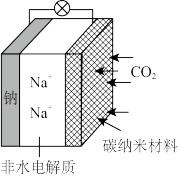
1 . 一种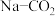 二次电池的装置如图所示,电池放电时正极反应式为
二次电池的装置如图所示,电池放电时正极反应式为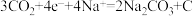 。下列说法中不正确的是
。下列说法中不正确的是
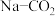 二次电池的装置如图所示,电池放电时正极反应式为
二次电池的装置如图所示,电池放电时正极反应式为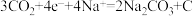 。下列说法中不正确的是
。下列说法中不正确的是
A.放电时,电解质溶液中 向碳纳米材料区移动 向碳纳米材料区移动 |
B.放电时,负极反应式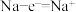 |
C.充电时,电池总反应为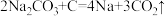 |
D.非水电解质可以是 的乙醇溶液 的乙醇溶液 |
您最近一年使用:0次
2022-10-10更新
|
259次组卷
|
3卷引用:四川省德阳市第五中学2022-2023学年高二下学期6月月考化学试题
名校
解题方法
2 . 利用反应6NO2+8NH3=7N2+12H2O设计的电池装置如图所示,该装置既能有效消除氮氧化物的排放减轻环境污染,又能充分利用化学能。下列说法正确的是( )

| A.电池工作时,OH—从左向右迁移 |
| B.电极A上发生氧化反应,电极A为正极 |
| C.当有0.1molNO2被处理时,外电路中通过电子0.4mol |
| D.电极B的电极反应式为2NO2+8e-+8H+=N2+4H2O |
您最近一年使用:0次
2019-12-31更新
|
1364次组卷
|
6卷引用:四川省眉山市彭山区第一中学2023-2024学年高二上学期开学考试化学试题
名校
3 . 图示为发表于《科学进展》的一种能够捕捉CO2的电化学装置,下列说法正确的是
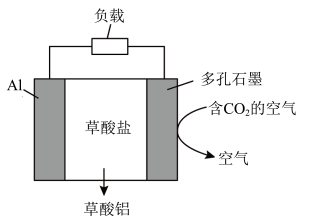

| A.Al电极是阴极 |
B.正极的电极反应为2CO2+2e-= |
| C.每生成1mol的草酸铝,外电路中转移3mol电子 |
D.在捕捉二氧化碳的过程中, 不断移向石墨电极附近 不断移向石墨电极附近 |
您最近一年使用:0次
2023-08-08更新
|
275次组卷
|
3卷引用:四川省仁寿第一中学校南校区2023-2024学年高三上学期开学考试化学试题
名校
4 . 某化学兴趣小组为了探索Zn电极在原电池中的作用,设计并进行了以下一系列实验。
已知:Zn与Al的化学性质基本相似, 。
。
回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为___________ 。
②每转移0.1 mol电子,此时负极材料减少的质量为___________ g。
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为___________ 。
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
②石墨电极上发生___________ (填“氧化”或“还原”)反应。
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为___________ 。
②外电路中电子的流动方向为___________ 。
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为___________ 。
已知:Zn与Al的化学性质基本相似,
 。
。回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为
②每转移0.1 mol电子,此时负极材料减少的质量为
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将
②石墨电极上发生
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为
②外电路中电子的流动方向为
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为
您最近一年使用:0次
2023-04-18更新
|
360次组卷
|
7卷引用:四川省峨眉第二中学校2022-2023学年高一下学期4月月考化学试题
名校
解题方法
5 . “海泥电池”既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理。电池工作原理如图所示。其中微生物代谢产物显酸性。下列说法不正确的是
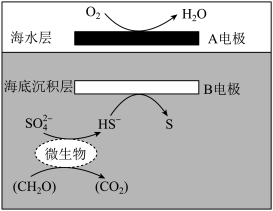

| A.A电极附近可沉积Mg(OH)2 |
| B.H+ 从海底沉积层通过交接面向海水层移动 |
C.微生物作用下发生反应:2CH2O + +H+=2CO2+HS−+2H2O +H+=2CO2+HS−+2H2O |
| D.除去3.0 g CH2O,A电极消耗标准状况下0.56 LO2 |
您最近一年使用:0次
2024-01-02更新
|
223次组卷
|
2卷引用:四川省成都市石室中学2023-2024学年高三上学期期中考试理科综合
解题方法
6 . 化学电源在生产生活中有着广泛的应用,请回答下列问颕:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_____ (填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如图两个对比实验(除图Ⅱ中增加导线和铜片外,其余条件完全相同)。经过相同时间后,温度计示数:图I_____ 图Ⅱ(填“高于”、“等于”或“低于”),产生气体的速率:图I_____ 图Ⅱ(填“大于”、“等于”或“小于”)。
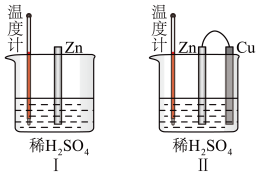
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是_____ (填化学式),电解质溶液是_____ (填化学式)溶液。
②正极上发生的电极反应为_____ 。
③若导线上转移的电子为1mol,则消耗的金属铜的质量为_____ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是
| A.Ba(OH)2+2NH4Cl=BaCl2+2NH3↑+2H2O | B.Cu+Ag+=Ag+Cu2+ |
| C.Zn+H2SO4=ZnSO4+H2↑ | D.CaO+H2O=Ca(OH)2 |

(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=2Fe2++Cu2+”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是
②正极上发生的电极反应为
③若导线上转移的电子为1mol,则消耗的金属铜的质量为
您最近一年使用:0次
名校
7 . 肼-空气燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示,设 为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是
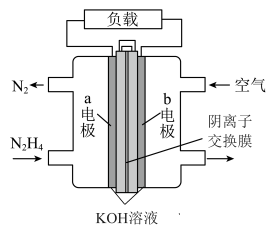
 为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是
| A.b电极为正极 |
B.a电极的电极反应式为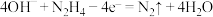 |
C.理论上当燃料电池消耗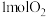 时,电路中转移4 时,电路中转移4 个电子 个电子 |
| D.工作一段时间后,KOH溶液的浓度基本不变 |
您最近一年使用:0次
2023-04-27更新
|
221次组卷
|
3卷引用:四川省资阳市乐至中学2022-2023学年高一下学期期中考试化学试题
名校
8 . 银锌电池是一种常见的化学电源,电池反应为:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其构造示意图如图所示。下列说法不正确的是
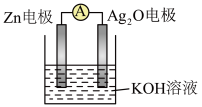

| A.Zn电极的电极反应式:Zn-2e-+2OH-=Zn(OH)2 |
| B.Ag2O电极发生还原反应 |
| C.电池工作时,电子由锌电极流出经过外电路流向Ag2O电极 |
| D.放电前后电解质溶液的pH保持不变 |
您最近一年使用:0次
2023-04-29更新
|
255次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
9 . 人类的一切活动都离不开能量,人们不仅利用化学反应获得新物质,也需从化学反应中获得能量。回答下列问题:
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为___________ 。
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =___________ ,能正确表示该过程的能量变化的是___________ (填标号)。
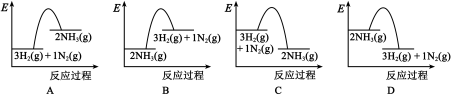
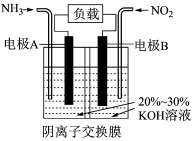
Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。
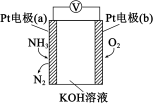
(3)正极为___________ (填“a”或“b”)电极,负极发生的电极反应式为___________ ,原电池总反应方程式为___________ 。
(4)溶液中OH−向电极___________ (填“a”或“b”)移动,电池工作一段时间后,溶液c(OH−)___________ (填“变大”“变小”或“不变”)。
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为___________ g。
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =

Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。

(3)正极为
(4)溶液中OH−向电极
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为
您最近一年使用:0次
2023-04-29更新
|
294次组卷
|
2卷引用:四川省成都市蓉城名校联盟2022-2023学年高一下学期期中联考化学试题
名校
解题方法
10 . 热电厂尾气经处理得到较纯的SO2,可用于原电池法生产硫酸。下列说法确的是
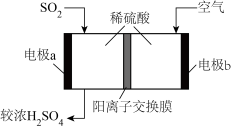
| A.电极b周围溶液pH变大 |
| B.溶液中H+由b极区向a极区迁移 |
C.电极a的电极反应式是SO2+2e-+2H2O=4H++SO |
| D.一段时间后,a极消耗的SO2与b极消耗的O2物质的量相等 |
您最近一年使用:0次
2022-07-02更新
|
439次组卷
|
6卷引用:四川省绵阳市南山中学实验学校2022-2023学年高一下学期6月月考化学试题
四川省绵阳市南山中学实验学校2022-2023学年高一下学期6月月考化学试题湖南省郴州市2022-2023学年高一下学期期末考试(选择考)化学试题安徽师范大学附属中学2023-2024学年高二上学期开学考试化学试题江西省宜春市丰城市第九中学2023-2024学年高二上学期开学考试化学(B卷)试题江苏省南京五中2021-2022学年高一下学期期末考试化学试题(已下线)综合期末压轴85+18题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)



