名校
1 . 微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式为Zn+2OH−−2e−===Zn(OH)2,Ag2O+H2O+2e−===2Ag+2OH−。下列叙述中正确的是
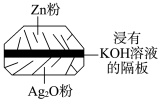

| A.在使用过程中,电解质KOH不断被消耗 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D.Zn是负极,Ag2O是正极 |
您最近一年使用:0次
2019-05-02更新
|
217次组卷
|
5卷引用:云南省中央民族大学附属中学昆明五华实验学校2023-2024学年高二上学期期中考试化学试题
名校
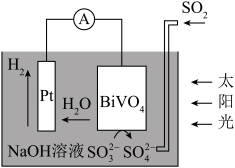
2 . 中科院科学家设计出一套利用 和太阳能综合制氢的方案,其基本工作原理如图所示。下列说法正确的是
和太阳能综合制氢的方案,其基本工作原理如图所示。下列说法正确的是
 和太阳能综合制氢的方案,其基本工作原理如图所示。下列说法正确的是
和太阳能综合制氢的方案,其基本工作原理如图所示。下列说法正确的是
A.该电化学装置中, 电极为负极 电极为负极 |
B.该电化学装置中, 电极的电势低于 电极的电势低于 电极的电势 电极的电势 |
C.电子流向: 电极→ 电极→ 电极 电极 |
D. 电极上的反应式为 电极上的反应式为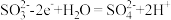 |
您最近一年使用:0次
名校
3 . 纸电池是一种有广泛应用的“软电池”,如图所示,这种碱性纸电池采用薄层纸片作为载体和传导体,纸的两面分别附着锌和二氧化锰。下列有关该纸电池的说法不合理的是


| A.Zn为负极,发生还原反应 |
| B.电池工作时,电子由MnO2流向Zn |
| C.正极反应:MnO2+e-+H2O=MnO(OH)+OH- |
| D.电池总反应:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH) |
您最近一年使用:0次
名校
4 . Ⅰ.燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。
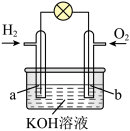
(1)负极是_________ (填“a”或“b”),该电极上发生_________ (填“氧化”或“还原”)反应。
(2)b极发生的电极反应式是__________________ 。
(3)标准状况下,消耗 时,转移的电子数为
时,转移的电子数为_________ 。
Ⅱ. 时,向
时,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入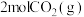 和
和 使之发生反应
使之发生反应 ,测得各物质的物质的量浓度变化如图所示:
,测得各物质的物质的量浓度变化如图所示:
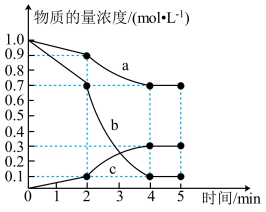
(4)由图可知, 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线_________ (填“a”“b”或“c”);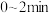 内的平均反应速率
内的平均反应速率 为
为_________ 。
(5)已知:反应至 时,改变了某一反应条件。由图可知,
时,改变了某一反应条件。由图可知, 内
内 的生成速率
的生成速率_________ (填“大于”“小于”或“等于”) 内
内 的生成速率。
的生成速率。
(6) 时,
时, 的转化率(反应时消耗
的转化率(反应时消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比)为
的物质的量的百分比)为_________ ,此时容器内气体总压强与反应前容器内气体总压强之比为_________ 。

(1)负极是
(2)b极发生的电极反应式是
(3)标准状况下,消耗
 时,转移的电子数为
时,转移的电子数为Ⅱ.
 时,向
时,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入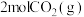 和
和 使之发生反应
使之发生反应 ,测得各物质的物质的量浓度变化如图所示:
,测得各物质的物质的量浓度变化如图所示:
(4)由图可知,
 的浓度随时间的变化为曲线
的浓度随时间的变化为曲线 内的平均反应速率
内的平均反应速率 为
为(5)已知:反应至
 时,改变了某一反应条件。由图可知,
时,改变了某一反应条件。由图可知, 内
内 的生成速率
的生成速率 内
内 的生成速率。
的生成速率。(6)
 时,
时, 的转化率(反应时消耗
的转化率(反应时消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比)为
的物质的量的百分比)为
您最近一年使用:0次
名校
5 . Ⅰ.给你提供纯锌、纯铜片和500mL0.2mol·L-1的H2SO4溶液、导线、1000mL量筒。试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。
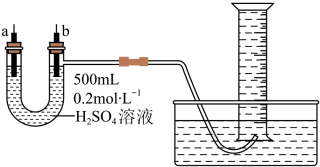
(1)如图所示,装置气密性良好,且1000mL量筒中已充满了水,则开始实验时,首先要_______ 。
(2)a电极材料为_______ ;b电极材料为_______ ,b电极反应式为_______ 。
(3)当量筒中收集672mL气体时(已折算到标准状况下),通过导线的电子的物质的量为_______ 。
Ⅱ.某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
(4)则A极是电池的_______ 极;电子从该极_______ (填“流入”或“流出”)。

(1)如图所示,装置气密性良好,且1000mL量筒中已充满了水,则开始实验时,首先要
(2)a电极材料为
(3)当量筒中收集672mL气体时(已折算到标准状况下),通过导线的电子的物质的量为
Ⅱ.某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
(4)则A极是电池的
您最近一年使用:0次
2023-07-29更新
|
57次组卷
|
2卷引用:云南省龙陵县第一中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . 含氮化合物在农业、工业、国防等领域都有着广泛的应用。氮元素部分常见物质间的相互转化如图所示。
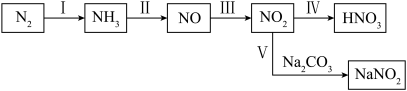
回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:_____ ;过程Ⅳ不断通入空气,理论上能使 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到_____ 吨质量分数为63%的硝酸。
(2)某温度下,在容积恒定为 的密闭容器中充入
的密闭容器中充入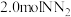 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示
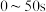 内的平均反应速率
内的平均反应速率
_____ ,250s时, 的转化率为
的转化率为_____ 。
Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:

(3)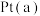 电极是电池的
电极是电池的_____ (填“正”或“负”)极。
(4)电解质溶液中的 向
向_____ (填“a”或“b”)极移动。
(5)该电池的负极反应式为_____

回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:
 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到(2)某温度下,在容积恒定为
 的密闭容器中充入
的密闭容器中充入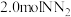 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示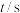 | 0 | 50 | 150 | 250 | 350 |
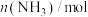 | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
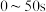 内的平均反应速率
内的平均反应速率
 的转化率为
的转化率为Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是
 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
(3)
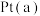 电极是电池的
电极是电池的(4)电解质溶液中的
 向
向(5)该电池的负极反应式为
您最近一年使用:0次
名校
7 . 科学家从天然产物中筛选物质开发出了一款完全可食用、可充电的电池。维生素B2为负极,从水果皮中提取的槲皮素为正极,NaHSO4水溶液为电解质溶液,如图所示。电池的性能测试显示电压为0.6~0.8V,水电解所需最低电压为1.23V。下列说法错误的是
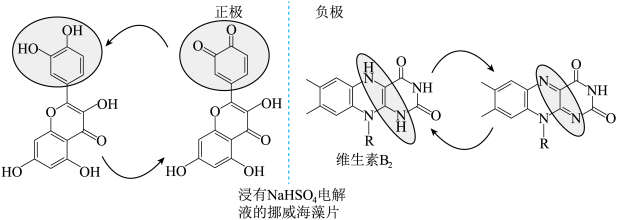

A.放电过程中海藻片中 向维生素B2电极迁移 向维生素B2电极迁移 |
B.放电时负极反应: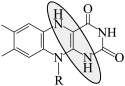 -2e-→ -2e-→ +2H+ +2H+ |
C.充电时总反应: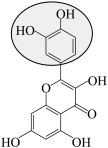 + +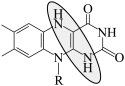 = = + +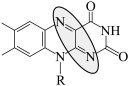 |
| D.该电池即使儿童误食也不会导致体内水电解而损害身体 |
您最近一年使用:0次
名校
解题方法
8 . Ⅰ.“绿水青山就是金山银山”,利用电池原理治理污染是今后科研的重要课题。
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为_____ 极。
②请用离子方程式分析H2S气体去除的原理:___________ 。
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和 :
: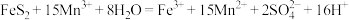 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
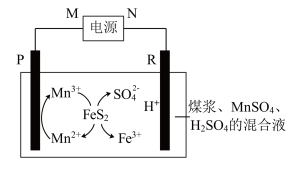
(2)电解池刚开始工作时,R上的电极反应式为_____ 。
(3)若电路中转移 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为_____ g(不考虑其他反应,下同),产生的气体的体积为______ L(已换算成标准状况)。
(4)电解过程中,混合溶液中的pH将_____ (填“变大”“变小”或“不变”),原因是___________ 。
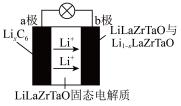
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接_____ (填“M”或“N”)极。
(1)硫化氢是一种具有臭鸡蛋气味的有毒气体,我国最近在太阳能光电催化——化学耦合分解硫化氢的研究中获得新进展,相关装置如图所示。

①a为
②请用离子方程式分析H2S气体去除的原理:
Ⅱ.为了减少对环境的污染,煤在直接燃烧前要进行脱硫处理。电解脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和
 :
: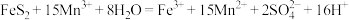 。已知:两电极为完全相同的惰性电极。
。已知:两电极为完全相同的惰性电极。
(2)电解池刚开始工作时,R上的电极反应式为
(3)若电路中转移
 电子,则此时消耗的
电子,则此时消耗的 的质量为
的质量为(4)电解过程中,混合溶液中的pH将
(5)Garnet型固态电解质被认为是锂离子电池最佳性能固态电解质。LiLaZrTaO材料是目前能达到最高电导率的Garnet型电解质。某Garnet型可充电锂离子电池放电时工作原理如图所示,若用该电池作为电解脱硫的外加电源,则b极应接

您最近一年使用:0次
9 . “海泥电池”既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理。电池工作原理如图所示,其中微生物代谢产物显酸性。下列说法正确的是
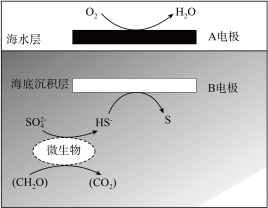

| A.A电极为负极 |
| B.H+从海水层通过交接面向海底沉积层移动 |
| C.高温下微生物蛋白质变性失活,故升温不一定能提高电池的效率 |
| D.除去3.0gCH2O,A电极消耗2.24LO2 |
您最近一年使用:0次
名校
解题方法
10 . 出土于陕西的两千多年前的越王剑(主要成分为铁),现藏于广州博物馆,该剑剑格左右侧皆以鸟虫书体铸刻“王戊”二字,剑色为水银古,时至如今,依然锋利。剑脊含铜量较多,韧性好,不易折断;刃部含锡高,硬度强,可见其性能优异,锻造技术优良。已知:剑在地下因构成原电池发生了腐蚀,导致生锈( )。下列叙述错误的是
)。下列叙述错误的是
 )。下列叙述错误的是
)。下列叙述错误的是| A.铁与铜、锡构成原电池时,铁为负极 |
B.铁发生的电极反应为 |
| C.生活中,为了防止铁板被腐蚀,可以在铁板上镀铜或者镀锌,镀锌效果更好 |
| D.铜碳合金在强酸性条件下不会发生析氢腐蚀 |
您最近一年使用:0次



