含氮化合物在农业、工业、国防等领域都有着广泛的应用。氮元素部分常见物质间的相互转化如图所示。
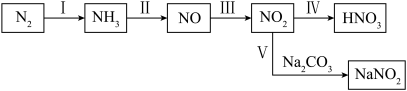
回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:_____ ;过程Ⅳ不断通入空气,理论上能使 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到_____ 吨质量分数为63%的硝酸。
(2)某温度下,在容积恒定为 的密闭容器中充入
的密闭容器中充入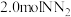 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示
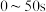 内的平均反应速率
内的平均反应速率
_____ ,250s时, 的转化率为
的转化率为_____ 。
Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:

(3)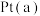 电极是电池的
电极是电池的_____ (填“正”或“负”)极。
(4)电解质溶液中的 向
向_____ (填“a”或“b”)极移动。
(5)该电池的负极反应式为_____

回答相关问题。
Ⅰ.
(1)图示中标示出了以氨为原料制备硝酸的全过程,写出过程Ⅱ的化学方程式:
 最终完全吸收,则1.7吨
最终完全吸收,则1.7吨 理论上可以得到
理论上可以得到(2)某温度下,在容积恒定为
 的密闭容器中充入
的密闭容器中充入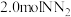 和
和 ,一段时间后反应达平衡状态,实验数据如下表所示
,一段时间后反应达平衡状态,实验数据如下表所示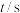 | 0 | 50 | 150 | 250 | 350 |
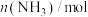 | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
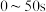 内的平均反应速率
内的平均反应速率
 的转化率为
的转化率为Ⅱ.近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是
 )和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
)和水分子通过。其工作原理的示意图如图所示,请回答下列问题:
(3)
 电极是电池的
电极是电池的(4)电解质溶液中的
 向
向(5)该电池的负极反应式为
更新时间:2023-06-27 16:32:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】电子工业中,人们常用 溶液腐蚀覆铜板来制作印刷电路板,并回收
溶液腐蚀覆铜板来制作印刷电路板,并回收 和综合利用
和综合利用 溶液。实验室模拟流程如图所示:
溶液。实验室模拟流程如图所示:
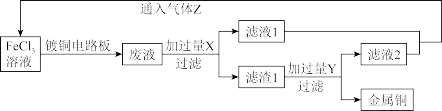
回答下列问题:
(1)写出 溶液腐蚀覆铜板的离子方程式
溶液腐蚀覆铜板的离子方程式_______ 。
(2)滤渣1成分的化学式为_______ ;试剂Y为_______ 。
(3)设计实验检验滤液2中所含金属阳离子的方法_______ 。
(4)气体Z为 ,可替代
,可替代 的试剂为_______(填序号)。
的试剂为_______(填序号)。
(5)若废液中含 、
、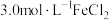 、
、 ,取
,取 该废液,按上述步骤回收铜,为充分回收铜,最少应加入X的质量为
该废液,按上述步骤回收铜,为充分回收铜,最少应加入X的质量为_______ g。
 溶液腐蚀覆铜板来制作印刷电路板,并回收
溶液腐蚀覆铜板来制作印刷电路板,并回收 和综合利用
和综合利用 溶液。实验室模拟流程如图所示:
溶液。实验室模拟流程如图所示:
回答下列问题:
(1)写出
 溶液腐蚀覆铜板的离子方程式
溶液腐蚀覆铜板的离子方程式(2)滤渣1成分的化学式为
(3)设计实验检验滤液2中所含金属阳离子的方法
(4)气体Z为
 ,可替代
,可替代 的试剂为_______(填序号)。
的试剂为_______(填序号)。| A.硝酸 | B.酸性高锰酸钾 | C.过氧化氢 | D.氧气 |
 、
、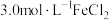 、
、 ,取
,取 该废液,按上述步骤回收铜,为充分回收铜,最少应加入X的质量为
该废液,按上述步骤回收铜,为充分回收铜,最少应加入X的质量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业,是一种浅黄色、遇水易分解的固体,但溶于浓硫酸后并不分解。某实验小组将SO2通入浓硫酸和浓硝酸的混合溶液中制备亚硝酰硫酸,并测定产品的纯度。
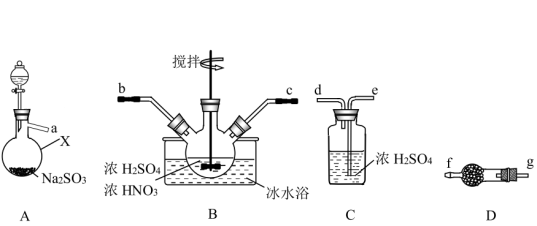
(1)仪器X的名称为_______ ;按气流从左到右的顺序,上述仪器的连接顺序为(填仪器接口字母)_______ ;装置D的作用是_______ 。
(2)装置B中发生反应的化学方程式为___________ 。开始时反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其可能原因是___________ 。
(3)装置B中维持反应体系温度不高于20℃的原因是___________ 。
(4)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00mL0.10mol·L-1的KMnO4溶液和适量稀H2SO4,摇匀,再将溶液加热至60—70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20mol·L-1的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①滴定终点的现象为___________ 。
②该产品的纯度为___________ (保留小数点后一位,NOSO4H的摩尔质量为127g·mol-1)。
③若配制KMnO4标准溶液时仰视刻度线定容,则测定的NOSO4H的纯度___________ (填“偏高”、“偏低”或“无影响”)。

(1)仪器X的名称为
(2)装置B中发生反应的化学方程式为
(3)装置B中维持反应体系温度不高于20℃的原因是
(4)测定产品的纯度:称取4.5g产品放入锥形瓶中,加入100.00mL0.10mol·L-1的KMnO4溶液和适量稀H2SO4,摇匀,再将溶液加热至60—70℃(使生成的HNO3挥发逸出),冷却至室温,然后用0.20mol·L-1的Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为25.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①滴定终点的现象为
②该产品的纯度为
③若配制KMnO4标准溶液时仰视刻度线定容,则测定的NOSO4H的纯度
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】回答下列问题
Ⅰ.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

(1)a、b、c三点溶液的pH大小关系:___________ 。
(2)a、b、C三点 的电离程度大小关系:
的电离程度大小关系:___________ 。
(3)a.b、c三点溶液用 NaOH溶液中和,消耗NaOH溶液体积大小关系:
NaOH溶液中和,消耗NaOH溶液体积大小关系:___________ 。
Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A.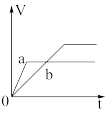 B.
B. 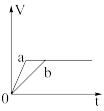 C.
C. 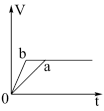 D.
D. 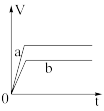
(4)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的 溶液,产生
溶液,产生 的体积V(L)与时间t(min)的关系是
的体积V(L)与时间t(min)的关系是___________ 。
(5)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的 溶液,产生
溶液,产生 的体积V(L)与时间t(min)的关系是
的体积V(L)与时间t(min)的关系是___________ 。
(6)将(5)中的 溶液改成
溶液改成 溶液,其他条件不变,则图象是
溶液,其他条件不变,则图象是___________ 。
Ⅲ.工业废水中常含有一定量的 和
和 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
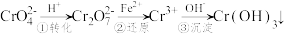
其中第①步存在平衡: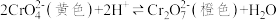
(7)向平衡体系滴加少量浓 ,则溶液显
,则溶液显___________ 色。
(8)能说明第①步反应达平衡状态的是___________ 。
a. 和
和 的浓度相同 b.
的浓度相同 b. c.溶液的颜色不变
c.溶液的颜色不变
(9)第②步中,还原1mol 离子,需要
离子,需要___________ mol的 。
。
Ⅰ.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

(1)a、b、c三点溶液的pH大小关系:
(2)a、b、C三点
 的电离程度大小关系:
的电离程度大小关系:(3)a.b、c三点溶液用
 NaOH溶液中和,消耗NaOH溶液体积大小关系:
NaOH溶液中和,消耗NaOH溶液体积大小关系:Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A.
 B.
B.  C.
C.  D.
D. 
(4)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的
 溶液,产生
溶液,产生 的体积V(L)与时间t(min)的关系是
的体积V(L)与时间t(min)的关系是(5)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的
 溶液,产生
溶液,产生 的体积V(L)与时间t(min)的关系是
的体积V(L)与时间t(min)的关系是(6)将(5)中的
 溶液改成
溶液改成 溶液,其他条件不变,则图象是
溶液,其他条件不变,则图象是Ⅲ.工业废水中常含有一定量的
 和
和 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为: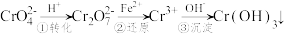
其中第①步存在平衡:
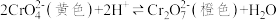
(7)向平衡体系滴加少量浓
 ,则溶液显
,则溶液显(8)能说明第①步反应达平衡状态的是
a.
 和
和 的浓度相同 b.
的浓度相同 b. c.溶液的颜色不变
c.溶液的颜色不变(9)第②步中,还原1mol
 离子,需要
离子,需要 。
。
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
它可以分为两步,反应分别如下:
①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g),ΔH1=-205.1kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2=__ 。
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的是__ (填字母代号)。
a.降低温度 B.加入催化剂 c.缩小容器体积 D.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
问:①反应开始时正、逆反应速率的大小:v(正)__ (填“>”、“<”或“=”)v(逆)。
②平衡时n(CH3OCH3)=__ ,平衡时CO的转化率=__ 。
(1)利用水煤气合成二甲醚的总反应为:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1
CH3OCH3(g)+CO2(g);ΔH=-246.4kJ·mol-1它可以分为两步,反应分别如下:
①4H2(g)+2CO(g)=CH3OCH3(g)+H2O(g),ΔH1=-205.1kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g);ΔH2=
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速率和CO转化率的是
a.降低温度 B.加入催化剂 c.缩小容器体积 D.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入3molH2、3molCO、1molCH3OCH3、1molCO2,在一定温度和压强下发生反应:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。
CH3OCH3(g)+CO2(g),经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率的大小:v(正)
②平衡时n(CH3OCH3)=
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F、G、H八种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E,B与G,D与H分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5个,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上八种元素中非金属所形成的最简单气态氢化物稳定性最弱的是_________ (填化学式),E、F、H 所形成的简单离子的半径由大到小的顺序为_________ (用离子符号表示)
(2)一定条件下,A的单质气体与C的单质气体充分反应生成W气体,W的结构式_____ 。由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_____ 。固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为________________ 。
(3)G是非金属元素,其单质在电子工业中有重要应用,请写出G的最高价氧化物与B的单貭在高温下发生置换反应的化学反应方程式____________________ 。
(4)10L的密闭容器中,通入2mol的HD2气体和1molD2的气体单质,一定条件下反应后生成HD3气体,当反应达到平衡时,单质D的浓度为0.01mol·L-1,同时放出约177KJ的热量,则平衡时HD2的转化率为____________ ;该反应的热化学方程式____________ 。
(1)以上八种元素中非金属所形成的最简单气态氢化物稳定性最弱的是
(2)一定条件下,A的单质气体与C的单质气体充分反应生成W气体,W的结构式
(3)G是非金属元素,其单质在电子工业中有重要应用,请写出G的最高价氧化物与B的单貭在高温下发生置换反应的化学反应方程式
(4)10L的密闭容器中,通入2mol的HD2气体和1molD2的气体单质,一定条件下反应后生成HD3气体,当反应达到平衡时,单质D的浓度为0.01mol·L-1,同时放出约177KJ的热量,则平衡时HD2的转化率为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】工业上用CO2、CO和H2在催化剂下制取甲烷、甲醇、乙烯等有重要的意义。
(1)已知 ①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ•mol-1
②2H2(g)+O2(g)=2H2O(l) △H=-572kJ•mol-1
③H2O(g)=H2O(l) △H=-44kJ•mol-1 CO2(g)+4H2(g) CH4(g)+2H2O(g) △H=a kJ•mol-1
CH4(g)+2H2O(g) △H=a kJ•mol-1
则a=___________
(2)①利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g) CH3OH(g)。在体积为2 L的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g)。在体积为2 L的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是___________
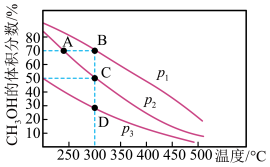
A.该反应的ΔH<0,且p1<p2
B.若p1时最初充入1 mol CO,经过5 min达到B点的平衡状态,此段时间v(CH3OH)=1.75 mol·L-1·min-1
C.在C点时,CO转化率为75%
D.A、B、C、D的平衡常数大小关系:A=B>C>D
②CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g)
CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图一所示。
a.反应Ⅰ自发进行的条件是___________ (选填“高温”或“低温”)
b.由图可知温度升高CO的产率上升,其主要原因可能是___________ 。
c.由图可知获取CH3OH最适宜的温度是___________ 。
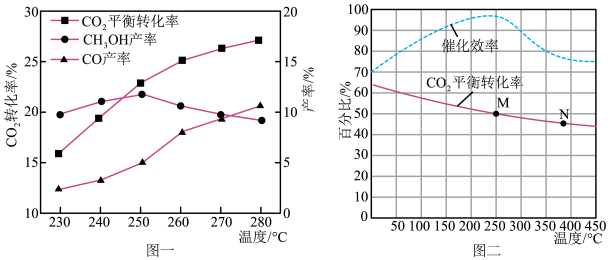
(3)以CO2为原料催化加氢合成低碳烯烃的反应方程式:2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH。在常压下,FeCoMnK/BeO 作催化剂,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应,测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图二所示。
C2H4(g)+4H2O(g) ΔH。在常压下,FeCoMnK/BeO 作催化剂,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应,测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图二所示。
①250 ℃下,上述反应达到平衡时容器体积为V L,则此温度下该反应的平衡常数为___________ (用含a、V的代数式表示)。
②反应开始时在0.1 MPa条件下,以n(H2)∶n(CO2)=3∶1的投料比充入体积固定的密闭容器中,发生反应:2CO2(g)+6H2(g) C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量分数如图三所示。
C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量分数如图三所示。
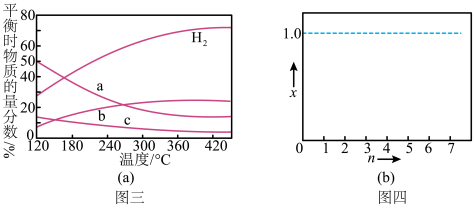
若氢气和二氧化碳的物质的量之比为n∶1(n≥3)进行投料,温度控制为120 ℃,相应平衡体系中乙烯的产率为x,在图四中绘制x随n(n≥3)变化的示意图___________ (标出曲线的起点坐标)。
(1)已知 ①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ•mol-1
②2H2(g)+O2(g)=2H2O(l) △H=-572kJ•mol-1
③H2O(g)=H2O(l) △H=-44kJ•mol-1 CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H=a kJ•mol-1
CH4(g)+2H2O(g) △H=a kJ•mol-1则a=
(2)①利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)
 CH3OH(g)。在体积为2 L的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g)。在体积为2 L的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
A.该反应的ΔH<0,且p1<p2
B.若p1时最初充入1 mol CO,经过5 min达到B点的平衡状态,此段时间v(CH3OH)=1.75 mol·L-1·min-1
C.在C点时,CO转化率为75%
D.A、B、C、D的平衡常数大小关系:A=B>C>D
②CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g)
CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图一所示。
a.反应Ⅰ自发进行的条件是
b.由图可知温度升高CO的产率上升,其主要原因可能是
c.由图可知获取CH3OH最适宜的温度是

(3)以CO2为原料催化加氢合成低碳烯烃的反应方程式:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ΔH。在常压下,FeCoMnK/BeO 作催化剂,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应,测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图二所示。
C2H4(g)+4H2O(g) ΔH。在常压下,FeCoMnK/BeO 作催化剂,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应,测得温度对CO2的平衡转化率和催化剂催化效率影响情况如图二所示。①250 ℃下,上述反应达到平衡时容器体积为V L,则此温度下该反应的平衡常数为
②反应开始时在0.1 MPa条件下,以n(H2)∶n(CO2)=3∶1的投料比充入体积固定的密闭容器中,发生反应:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量分数如图三所示。
C2H4(g)+4H2O(g),不同温度下平衡时的四种气态物质的物质的量分数如图三所示。
若氢气和二氧化碳的物质的量之比为n∶1(n≥3)进行投料,温度控制为120 ℃,相应平衡体系中乙烯的产率为x,在图四中绘制x随n(n≥3)变化的示意图
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】把A、B、C、D四种金属按表中装置进行实验。
根据实验现象回答问题:
(1)装置乙中正极的电极反应式是___ 。
(2)装置丙中溶液的酸性___ (填“变大”“变小”或“不变”)。
(3)四种金属活泼性由强到弱的顺序是___ 。
| 装置 | 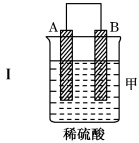 |  | 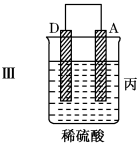 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置乙中正极的电极反应式是
(2)装置丙中溶液的酸性
(3)四种金属活泼性由强到弱的顺序是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.一定温度下在某定容容器中发生反应:2A(g)+3B(g)=2C(g),开始时,A的浓度为2mol·L-1,B的浓度为4mol·L-1,2min后,A的浓度减少0.8mol·L-1,则:
(1)v(B)=_______ ,v(C)=_______ 。
(2)在2min末,C的浓度是_______ ,B的浓度是_______ 。
Ⅱ.如图所示的原电池装置中:

(1)_______ (填“铜”或“锌”)作负极。
(2)正极的电极反应式为_______ 。
(3)电子的流向_______ 。
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻_______ g。
(1)v(B)=
(2)在2min末,C的浓度是
Ⅱ.如图所示的原电池装置中:

(1)
(2)正极的电极反应式为
(3)电子的流向
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】化学电源发展日新月异,在生产生活中发挥着巨大作用.
Ⅰ.一种高铁电池的总反应式为 。请回答下列问题:
。请回答下列问题:
(1)负极反应式为:__________ 。
(2)放电时,___________ (填“正”或“负”)极附近溶液的碱性增强;
Ⅱ.下图是甲烷—氧气燃料电池原理示意图,回答下列问题.__________ ;
(4)a极的电极反应式为__________ ;
(5)标准状况下,消耗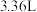 甲烷,电路中转移的电子数目为
甲烷,电路中转移的电子数目为___________ ;
(6)若将该燃料电池中的 溶液换成稀
溶液换成稀 ,在此条件下
,在此条件下 参与的电极反应两步完成:第一步:
参与的电极反应两步完成:第一步:__________ ;第二步:
Ⅰ.一种高铁电池的总反应式为
 。请回答下列问题:
。请回答下列问题:(1)负极反应式为:
(2)放电时,
Ⅱ.下图是甲烷—氧气燃料电池原理示意图,回答下列问题.
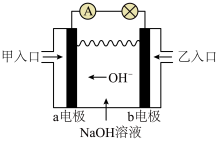
(4)a极的电极反应式为
(5)标准状况下,消耗
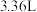 甲烷,电路中转移的电子数目为
甲烷,电路中转移的电子数目为(6)若将该燃料电池中的
 溶液换成稀
溶液换成稀 ,在此条件下
,在此条件下 参与的电极反应两步完成:第一步:
参与的电极反应两步完成:第一步:
您最近半年使用:0次



