解题方法
1 .  等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
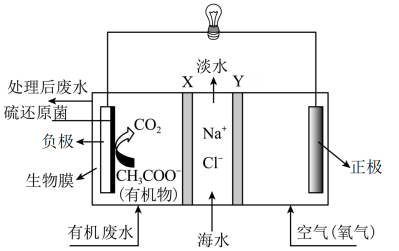
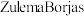 等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
等设计的一种微生物脱盐池的装置如图所示,下列说法正确的是
| A.该装置可以在高温下工作 |
B. 依次为阴离子、阳离子交换膜 依次为阴离子、阳离子交换膜 |
C.负极反应式为 |
| D.该装置工作时,电能转化为化学能 |
您最近一年使用:0次
名校
解题方法
2 . 下列有关电化学装置的说法中,不正确的是


| A.图a装置工作后,甲中溶液变为红色 |
| B.图b装置工作一段时间后,可以实现铁件表面镀铜 |
| C.图c装置工作一段时间后,溶液的pH减小 |
| D.图d装置充电时,铅电极应与外加电源的负极相连 |
您最近一年使用:0次
名校
解题方法
3 .  可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
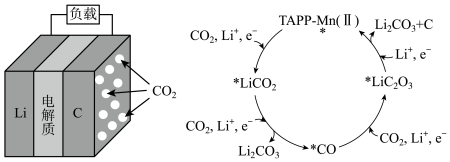
 可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
| A.放电时,电流由C电极流出,经负载流入Li电极 |
B. 电池可以使用 电池可以使用 水溶液做离子导体 水溶液做离子导体 |
C.放电时, 由Li电极向C电极迁移 由Li电极向C电极迁移 |
D.充电时,阳极反应为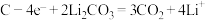 |
您最近一年使用:0次
2024-01-26更新
|
514次组卷
|
4卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
4 . 能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
(1)为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有专家提出利用太阳能促进燃料循环使用的构想,如图所示:
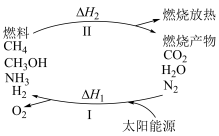
过程Ⅰ的能量转化形式为___________ 能转化为___________ 能。
(2)有机物M经过太阳光照射可转化成N,转化过程如下:
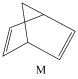

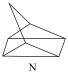 ΔH=+88.6kJ/mol
ΔH=+88.6kJ/mol
则M、N中,较稳定的是___________ 。
(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。其过程如图所示:
太阳能→热能→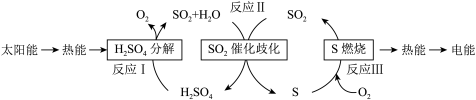
反应Ⅰ:2H2SO4(l) 2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
反应Ⅲ:S(s)+O2(g) SO2(g) ΔH3=-297kJ/mol
SO2(g) ΔH3=-297kJ/mol
写出反应Ⅱ的热化学方程式:___________ 。
(4)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是___________(填标号)。
(5)如图所示的装置中,X、Y都是惰性电极。将电路接通后,向乙装置中滴入无色酚酞溶液,Fe极附近显红色。
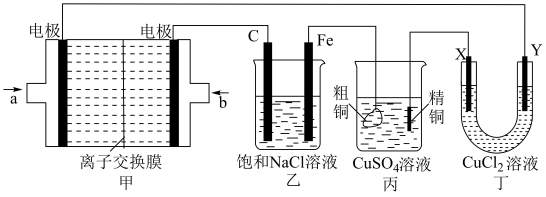
①甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,电极a上的电极反应式是___________ 。
②乙装置中,总反应的离子方程式是___________ 。
③若丙装置中精铜电极的质量增加了6.4g,则甲装置中标准状况下消耗的CH4的体积为___________ 。
(1)为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有专家提出利用太阳能促进燃料循环使用的构想,如图所示:

过程Ⅰ的能量转化形式为
(2)有机物M经过太阳光照射可转化成N,转化过程如下:


 ΔH=+88.6kJ/mol
ΔH=+88.6kJ/mol则M、N中,较稳定的是
(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。其过程如图所示:
太阳能→热能→

反应Ⅰ:2H2SO4(l)
 2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol反应Ⅲ:S(s)+O2(g)
 SO2(g) ΔH3=-297kJ/mol
SO2(g) ΔH3=-297kJ/mol写出反应Ⅱ的热化学方程式:
(4)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是___________(填标号)。
| A.C(s)+CO2(g)=2CO(g) ΔH>0 |
| B.4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH<0 |
| C.NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l) ΔH<0 |
| D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0 |
(5)如图所示的装置中,X、Y都是惰性电极。将电路接通后,向乙装置中滴入无色酚酞溶液,Fe极附近显红色。

①甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,电极a上的电极反应式是
②乙装置中,总反应的离子方程式是
③若丙装置中精铜电极的质量增加了6.4g,则甲装置中标准状况下消耗的CH4的体积为
您最近一年使用:0次
名校
5 . 下列装置能够形成原电池且铜为负极的是
A.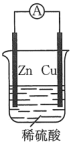 | B.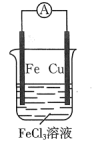 | C.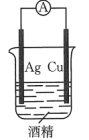 | D. |
您最近一年使用:0次
名校
解题方法
6 . 巴蜀中学化学实验小组利用下图所示微生物电池将污水中苯酚(C6H6O)转化为无毒无害的物质并产生电能(M、N 均为石墨电极)。下列说法错误的是
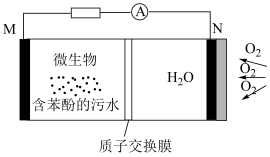

| A.该电池不适宜在高温环境下工作 |
B.M极的电极反应式为: |
C.每消耗标准状况下22.4L  时,理论上能处理约含 13.4g苯酚的废水 时,理论上能处理约含 13.4g苯酚的废水 |
| D.电池工作过程中,正极区的pH降低 |
您最近一年使用:0次
解题方法
7 . 下列有关方程式的书写,错误的是
A.工业上用铂电极电解饱和食盐水制备氯气: |
B.钢铁吸氧腐蚀的正极反应: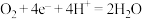 |
C.一种锂离子电池,其负极材料为嵌锂石墨 ,负极放电原理: ,负极放电原理: |
D. 检验溶液中 检验溶液中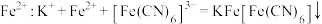 |
您最近一年使用:0次
名校
解题方法
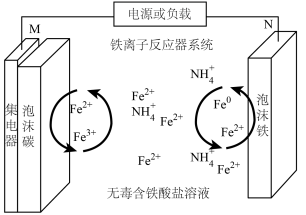
8 . 我国某大学科研团队提出用多孔泡沫铁、高度膨化的纳米泡沫碳(CFs)和添加了 的
的 溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是
溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是
 的
的 溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是
溶液构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是
A. 可增加电解质溶液的导电性 可增加电解质溶液的导电性 |
B.充电时,阳极的电极反应式为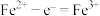 |
| C.放电时,电极N为负极 |
D.放电时,每转移 ,参与反应的铁元素的总质量为112g ,参与反应的铁元素的总质量为112g |
您最近一年使用:0次
2024-01-11更新
|
249次组卷
|
4卷引用:河南省创新发展联盟2023-2024学年高二上学期第四次联考化学试题
名校
9 . 自重轻、体积小、容量大、使用安全、环保是新型电池的典型特点,回答下列问题:
I.“阿波罗”飞船中使用的氢氧燃料电池部分结构如图所示。
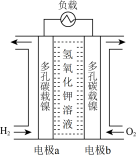
(1)电池的正极为电极___________ (填“a”或“b”),其表面上发生的电极反应为___________ (填电极反应式)。
(2)“神舟”飞船是中国自行研制的,具有自主知识产权的载人飞船,其返回舱使用的是银锌蓄电池组。银锌电池结构如图所示,放电时总反应为 。电池放电时负极质量
。电池放电时负极质量___________ (填“增大”、“减小”或“不变”),电池放电时电解质溶液的
___________ (填“增大”、“减小”或“不变”)。

Ⅱ.非水系锂氧(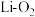 )电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许
)电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许 通过。
通过。

(3)放电时,电池的总反应为___________ ;电解液a不选用 水溶液的原因可能是
水溶液的原因可能是___________ 。
(4)不考虑其他副反应,若放电前两电极质量完全相同,放电时,电路中转移1mole-,正、负电极的质量之差为___________ g(假设生成的不溶物全覆盖在电极表面,生成的可溶物全部扩散至电解液中,参与电极反应的物质均过量)。(相对原子质量:Li~7 O~16 )
I.“阿波罗”飞船中使用的氢氧燃料电池部分结构如图所示。

(1)电池的正极为电极
(2)“神舟”飞船是中国自行研制的,具有自主知识产权的载人飞船,其返回舱使用的是银锌蓄电池组。银锌电池结构如图所示,放电时总反应为
 。电池放电时负极质量
。电池放电时负极质量

Ⅱ.非水系锂氧(
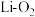 )电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许
)电池因其高能量密度而成为一种有前景的先进电池技术,其放电电池示意图以及正极示意图分别为图1和图2,隔膜a只允许 通过。
通过。
(3)放电时,电池的总反应为
 水溶液的原因可能是
水溶液的原因可能是(4)不考虑其他副反应,若放电前两电极质量完全相同,放电时,电路中转移1mole-,正、负电极的质量之差为
您最近一年使用:0次
名校
解题方法
10 . 为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
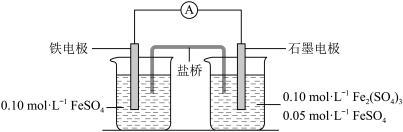
回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol/LFeSO4溶液,需要的仪器有药匙、玻璃棒、_______ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E.
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择___________ (物质化学式)作为电解质。
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入___________ 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+ )增加了0.02 mol/L。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=___________ 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为___________ ,铁电极的电极反应式为___________ 。因此,验证了Fe2+氧化性小于___________ ,还原性小于___________ 。
(6)实验前需要对铁电极表面活化。在FeSO4 溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是___________ 。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol/LFeSO4溶液,需要的仪器有药匙、玻璃棒、
A.
 B.
B.  C.
C.  D.
D.  E.
E.
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s-1·v-1) | 阴离子 | u∞×108/(m2·s-1·v-1) |
| Li+ | 4.07. |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+ )增加了0.02 mol/L。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为
(6)实验前需要对铁电极表面活化。在FeSO4 溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是
您最近一年使用:0次



