1 . 利用电解质溶液的浓度对电极电势的影响,可设计浓差电池。某热再生浓差电池放电时的工作原理如图所示,通入 发生反应
发生反应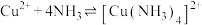 ,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
 发生反应
发生反应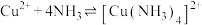 ,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是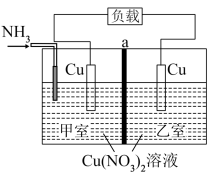
| A.放电时,甲室Cu电极电势高于乙室 |
B.充电时, 经阴离子交换膜a由乙室向甲室迁移 经阴离子交换膜a由乙室向甲室迁移 |
| C.放电时,外电路有0.2mol电子通过时,乙室溶液质量减少6.4g |
D.电池的总反应为: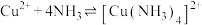 , , |
您最近一年使用:0次
解题方法
2 . 利用 制取氢气过程的示意图如图。下列说法
制取氢气过程的示意图如图。下列说法不正确 的是
 制取氢气过程的示意图如图。下列说法
制取氢气过程的示意图如图。下列说法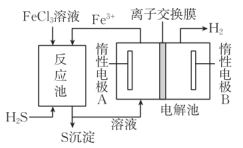
A.惰性电极A的电极反应: |
| B.惰性电极B接电源负极,发生还原反应 |
| C.反应池中反应物需要采用气、液逆流方式,目的是增大反应物接触面积并充分吸收气体 |
D.装置中应选用质子交换膜,电解时, 向惰性电极B移动 向惰性电极B移动 |
您最近一年使用:0次
名校
3 . 利用如图所示的装置电解 溶液,并检验产物性质,其中a为浸泡了紫色石蕊溶液的纸条,b为湿润的有色布条。下列说法正确的是
溶液,并检验产物性质,其中a为浸泡了紫色石蕊溶液的纸条,b为湿润的有色布条。下列说法正确的是
 溶液,并检验产物性质,其中a为浸泡了紫色石蕊溶液的纸条,b为湿润的有色布条。下列说法正确的是
溶液,并检验产物性质,其中a为浸泡了紫色石蕊溶液的纸条,b为湿润的有色布条。下列说法正确的是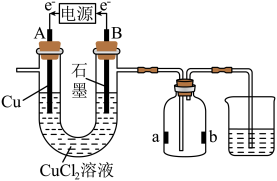
A.A为阴极,发生还原反应得到 |
| B.电解一段时间,a纸条变成红色并持续到实验结束 |
| C.b布条褪色,证明氯气有漂白性 |
D.U形管中 完全消耗后,反应停止,B极不会继续产生气体 完全消耗后,反应停止,B极不会继续产生气体 |
您最近一年使用:0次
2024-05-30更新
|
189次组卷
|
3卷引用:2024届浙江省高三下学期5月份大联考化学试题
名校
4 . 关于阿伏加德罗常数 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.32g Cu与足量S充分反应,转移电子数为0.5 |
B.电解精炼铜时,当电路中通过 个电子时,阳极溶解32g铜 个电子时,阳极溶解32g铜 |
C.0.1mol环戊烯醇( ),含有极性键的数目为0.8 ),含有极性键的数目为0.8 |
D.铜催化下1mol 2-丙醇全部转化为丙酮,得到电子的数目为2 |
您最近一年使用:0次
名校
解题方法
5 . 利用电化学方法富集海水中的锂,其工作原理如下图所示。工作步骤如下:①向MnO2所在腔室通入海水,启动电源1,使海水中的 进入MnO2而形成
进入MnO2而形成 ;②关闭电源1和海水通道,启动电源2,同时向电极2上通入空气。下列说法
;②关闭电源1和海水通道,启动电源2,同时向电极2上通入空气。下列说法不正确 的是
 进入MnO2而形成
进入MnO2而形成 ;②关闭电源1和海水通道,启动电源2,同时向电极2上通入空气。下列说法
;②关闭电源1和海水通道,启动电源2,同时向电极2上通入空气。下列说法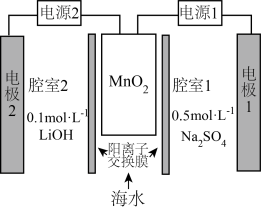
| A.上述过程中,电极1和电极2分别作阳极和阴极 |
B.启动电源1时,阴极上的电极反应: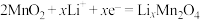 |
C.启动电源2时, 中的 中的 脱出进入腔室2 脱出进入腔室2 |
D.当有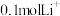 脱出时,电极2上产生1.12L(标准状况下)的H2 脱出时,电极2上产生1.12L(标准状况下)的H2 |
您最近一年使用:0次
6 . 下列说法正确的是
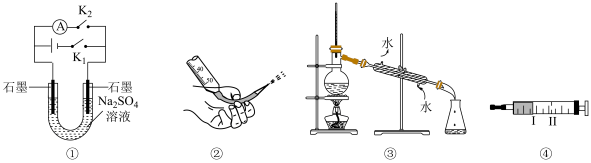
A.图①闭合 一段时间,再打开 一段时间,再打开 闭合 闭合 可制得简易燃料电池,左侧石墨为电池正极 可制得简易燃料电池,左侧石墨为电池正极 |
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡 溶液滴定管尖嘴内的气泡 |
| C.图③用于分离沸点相差很小的液体混合物 |
D.图④研究压强对 平衡的影响,将活塞从Ⅰ拉到Ⅱ,气体压强减小,平衡逆向移动,颜色加深 平衡的影响,将活塞从Ⅰ拉到Ⅱ,气体压强减小,平衡逆向移动,颜色加深 |
您最近一年使用:0次
解题方法
7 . 周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: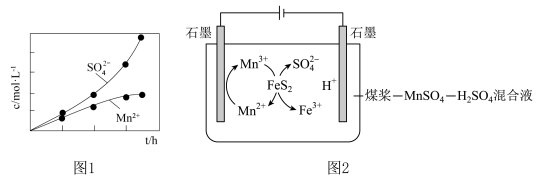
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
您最近一年使用:0次
解题方法
8 . 某实验小组利用下列装置来降低某硬水中 、
、 和
和 的含量,
的含量,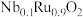 和
和 为极板催化剂。下列说法不正确的是
为极板催化剂。下列说法不正确的是
 、
、 和
和 的含量,
的含量,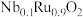 和
和 为极板催化剂。下列说法不正确的是
为极板催化剂。下列说法不正确的是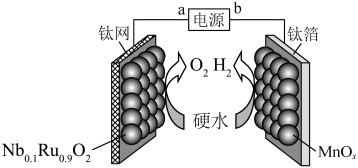
| A.a端电势高于b端电势 |
B.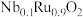 可加快 可加快 失去电子的速率 失去电子的速率 |
C.其它条件不变,适当减小两极的极板间距, 、 、 沉淀速率增大 沉淀速率增大 |
D.阳极区收集的气体中只含有 |
您最近一年使用:0次
名校
解题方法
9 . 沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
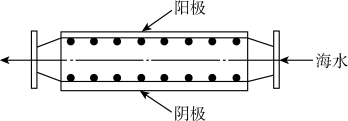
| A.阳极发生反应是Cl-被氧化 |
| B.管道中可以生成氧化灭杀附着生物的NaClO |
| C.阴极生成的电极反应:2H2O+2e-=2OH-+H2↑ |
| D.阳极表面形成的Mg(OH)2等积垢需要定期清理 |
您最近一年使用:0次
名校
解题方法
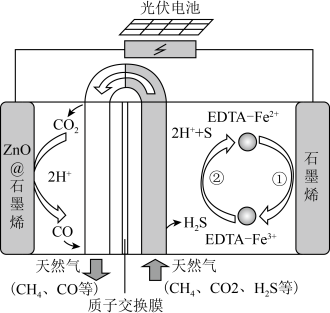
10 . 最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
该装置工作时,下列叙述错误的是
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
该装置工作时,下列叙述错误的是
| A.阴极的电极反应:CO2+2H++2e-=CO+H2O |
| B.若生成3.2gS,理论上通过两极电量都为0.4F(C)(F为法拉第常数) |
| C.石墨烯上的电势比ZnO@石墨烯上的高 |
| D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性 |
您最近一年使用:0次



