周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: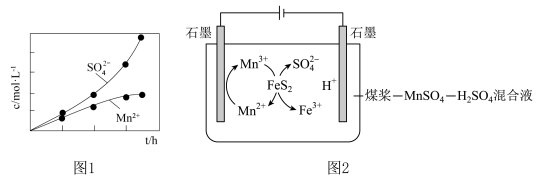
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
更新时间:2024-05-04 16:41:28
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】乙醇是生活中常见的有机物,能发生多种反应,请回答下列问题:
(1)乙醇分子中官能团的名称是___________ (填“羟基”或“羧基”)。
(2)乙醇在铜做催化剂的条件下可被___________ (填“氧化”或“还原”)为乙醛。反应中反应物的总能量高于生成物的总能量,说明该反应是___________ (填“吸热反应”或“放热反应”)。
(3)乙醇也可与乙酸发生反应: C2H5OH+CH3COOH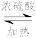 CH3COOC2H5+H2O
CH3COOC2H5+H2O
①该反应需要加热并加入浓硫酸,目的是___________ (填“加快”或“减慢”反应速率。)
②在一定条件下,当反应达到平衡状态时,正反应速率____ 逆反应速率(填“>”“<”或“=”)。
(1)乙醇分子中官能团的名称是
(2)乙醇在铜做催化剂的条件下可被
(3)乙醇也可与乙酸发生反应: C2H5OH+CH3COOH
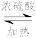 CH3COOC2H5+H2O
CH3COOC2H5+H2O①该反应需要加热并加入浓硫酸,目的是
②在一定条件下,当反应达到平衡状态时,正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应速率及平衡在生产生活中有重要作用。
已知反应
(1)小组同学发现反应速率总是如下图所示,其中 时间内速率变快的主要原因可能是:①该反应放热②
时间内速率变快的主要原因可能是:①该反应放热②___________

(2) 后反应速率逐渐减小的原因是
后反应速率逐渐减小的原因是___________ 。
已知反应

(1)小组同学发现反应速率总是如下图所示,其中
 时间内速率变快的主要原因可能是:①该反应放热②
时间内速率变快的主要原因可能是:①该反应放热②
(2)
 后反应速率逐渐减小的原因是
后反应速率逐渐减小的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】用碳棒作电极,在H+、Na+、Cu2+、Ag+、Cl-、NO 、SO
、SO 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
(1)当阴极析出金属,阳极放出O2时,电解质是_______ ;
(2)当阴极放出H2,阳极放出O2时,电解质是_______ ;
(3)当阴极放出H2,阳极放出Cl2时,电解质是_______ ;
(4)通过电子的物质的量与阴极析出的金属、阳极析出的气体的物质的量之比为4∶2∶1时,电解质的化学式是_______
 、SO
、SO 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:(1)当阴极析出金属,阳极放出O2时,电解质是
(2)当阴极放出H2,阳极放出O2时,电解质是
(3)当阴极放出H2,阳极放出Cl2时,电解质是
(4)通过电子的物质的量与阴极析出的金属、阳极析出的气体的物质的量之比为4∶2∶1时,电解质的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长,利用该电池电解处理含 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
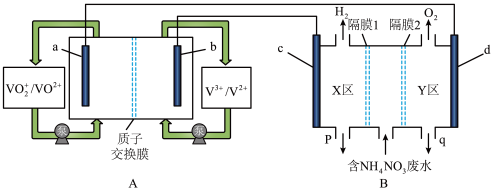
回答下列问题:
(1)a电极为_______ (填“正极”或“负极”),其电极反应式为_______ 。
(2)隔膜1为_______ 交换膜(填“阴离子”或“阳离子”),q口流出液含有的溶质为_______ (填化学式),d电极的电极反应式为_______ 。
(3)B装置中产生的气体总量为336 mL(标准状况下)时,通过质子交换膜的 的物质的量为
的物质的量为_______ mol。
 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。
回答下列问题:
(1)a电极为
(2)隔膜1为
(3)B装置中产生的气体总量为336 mL(标准状况下)时,通过质子交换膜的
 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电化学在物质制备、新材料和环境保护等方面具有独到的应用优势。
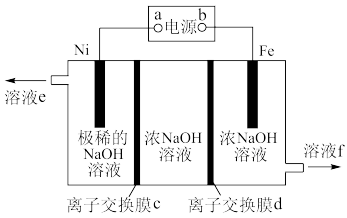
(1)高铁酸钠(Na2FeO4)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备Na2FeO4的工作原理如图所示,a是电源的______ 极(填“正”或“负”)。阳极电极的电极反应式为_____ ,其中离子交换膜c是______ (阳离子交换膜或阴离子交换膜)。
(2)燃煤烟气中的SO2可用如图装置进行处理。
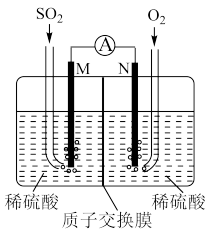
M极发生的电极反应式为_____ ,当外电路通过0.2mol电子时,质子交换膜左侧溶液质量的变化______ g。
(1)高铁酸钠(Na2FeO4)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备Na2FeO4的工作原理如图所示,a是电源的

(2)燃煤烟气中的SO2可用如图装置进行处理。

M极发生的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)依据反应: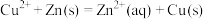 设计的原电池如图所示。
设计的原电池如图所示。
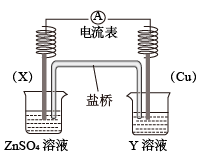
①电极X的材料是________ ;Y溶液可以是________ 溶液。
②电池放电过程中,盛有饱和 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是________ (填离子符号)。
(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:_________ 。
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:
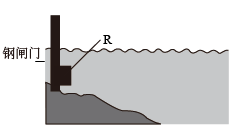
其中连接在铁闸门上的固体材料R可以采用________ (填写字母序号)。
a.铜 b.钠 c.锌 d.石墨
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
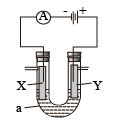
①若X、Y都是惰性电极,a是饱和 溶液,则电解的总反应式为
溶液,则电解的总反应式为________________ 。
②当电路中流通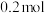 电子时,整个装置共放出气体
电子时,整个装置共放出气体________ L(标准状况下)。
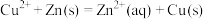 设计的原电池如图所示。
设计的原电池如图所示。
①电极X的材料是
②电池放电过程中,盛有饱和
 琼脂溶胶的盐桥中,向
琼脂溶胶的盐桥中,向 溶液扩散的离子是
溶液扩散的离子是(2)钢铁发生电化学腐蚀可分为析氢腐蚀和吸氧腐蚀,可以采用电化学手段进行防护。
①写出钢铁在酸性较强的环境中发生电化学腐蚀的正极反应式:
②为了减缓水库铁闸门被腐蚀的速率,可以采用下图所示的方案:

其中连接在铁闸门上的固体材料R可以采用
a.铜 b.钠 c.锌 d.石墨
(3)电解原理在工业上有着广泛的用途,如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。

①若X、Y都是惰性电极,a是饱和
 溶液,则电解的总反应式为
溶液,则电解的总反应式为②当电路中流通
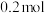 电子时,整个装置共放出气体
电子时,整个装置共放出气体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请按要求回答下列问题。

(1)根据图1回答①②:
①打开K2,闭合K1。A极现象___ ,B极的电极反应式为___ 。
②打开K1,闭合K2。A极可观察到的现象是__ 。
(2)根据图2回答③④:③电解反应的离子方程式为__ 。
④实验完成后,铜电极增重ag,石墨电极产生标准状况下的气体体积__ L。

(1)根据图1回答①②:
①打开K2,闭合K1。A极现象
②打开K1,闭合K2。A极可观察到的现象是
(2)根据图2回答③④:③电解反应的离子方程式为
④实验完成后,铜电极增重ag,石墨电极产生标准状况下的气体体积
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求完成:
(1)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0 mol·L-1,若忽略氨水浓度的变化,溶液中的c(OH-)约为_______ mol·L-1;0.1 mol ·L-1的(NH4)2SO3溶液显________ (填“酸”“碱性”或“中性”)。
(2)某研究性学习小组将下列装置按如图连接,C、D、E、F、X、Y都是惰性电极,甲、乙、丙中电解质溶液含溶质均为1 mol。将电源接通后,向乙中滴入酚猷溶液,在F极附近显红色。试回答下列问题:
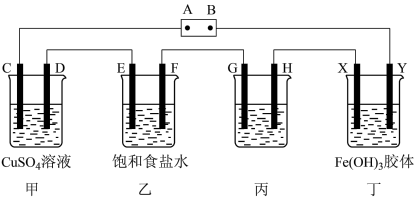
①电源A极的名称是__________ 。
②乙装置中电解反应的总化学方程式:___________ 。
③当电路中通过4 mole-时,要使甲中溶液种类和浓度均复原,可向电解后溶液中加入_______ (填某一种物质的化学式和物质的量)。
④装置丁中的现象是_______ 。
(1)已知25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0 mol·L-1,若忽略氨水浓度的变化,溶液中的c(OH-)约为
(2)某研究性学习小组将下列装置按如图连接,C、D、E、F、X、Y都是惰性电极,甲、乙、丙中电解质溶液含溶质均为1 mol。将电源接通后,向乙中滴入酚猷溶液,在F极附近显红色。试回答下列问题:

①电源A极的名称是
②乙装置中电解反应的总化学方程式:
③当电路中通过4 mole-时,要使甲中溶液种类和浓度均复原,可向电解后溶液中加入
④装置丁中的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】
(1)17Cl的电子排布式___________ ;价层电子排布图_________ ;Cl-的电子排布式_______________ 。
(2)26Fe的电子排布式__________ ;26Fe2+ 电子排布式_________ ;26Fe3+电子排布式_____________ 。
(3)第三周期中,第一电离能最小的元素是_________ ,第一电离能最大的元素是_________ 。
(4)在元素周期表中,电负性最大的元素是_________ ,第二、三周期P 轨道半充满的元素是_________ 。
(1)17Cl的电子排布式
(2)26Fe的电子排布式
(3)第三周期中,第一电离能最小的元素是
(4)在元素周期表中,电负性最大的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)元素原子的价电子构型为3s23p3,它属于第________ 周期,是______ 族,元素符号是________ 。
(2)在HCl分子中,由H原子的一个____ 轨道与Cl原子的一个_____ 轨道形成一个____ 键;在Cl2分子中两个Cl原子以2个____ 轨道形成一个 ____ 键。
(2)在HCl分子中,由H原子的一个
您最近一年使用:0次

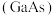 是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为
是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为 。
。 中
中 键的数目为
键的数目为

