解题方法
1 . 周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: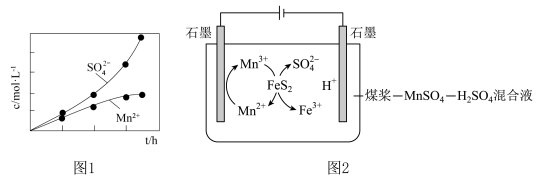
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
您最近一年使用:0次
名校
解题方法
2 . 我国应对气候变化工作成效显著,北京冬奥会是首个实现“碳中和”的世界级体育盛会,我国承诺2030年前实现“碳达峰”,2060年前实现“碳中和”。如何高效利用 是重要的研究课题。
是重要的研究课题。
I.光合作用
(1)植物光合作用中能量的转化形式为_____ 。
(2)“人工树叶”电化学装置如图1所示(以稀硫酸为电解质溶液),该装置能将CO2和H2O转化为糖类(用C6H12O6表示)和O2。
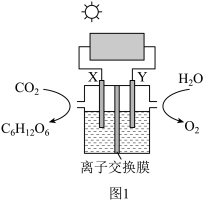
①Y为_____ 极,该极上发生的电极反应式为_____ 。
②室温下,该装置工作一段时间后,电解质溶液的pH_____ (填“升高”“降低”或“不变”)。
Ⅱ.电化学方法可将CO2有效地转化为CH3COOH,装置如图2所示
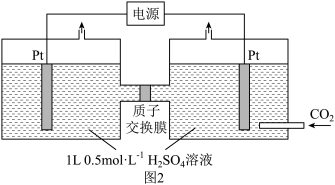
(3)阴极电极反应式为_____ ;电解时,H+通过质子交换膜向_____ 移动(填“左”或“右”)。
 是重要的研究课题。
是重要的研究课题。I.光合作用

(1)植物光合作用中能量的转化形式为
(2)“人工树叶”电化学装置如图1所示(以稀硫酸为电解质溶液),该装置能将CO2和H2O转化为糖类(用C6H12O6表示)和O2。

①Y为
②室温下,该装置工作一段时间后,电解质溶液的pH
Ⅱ.电化学方法可将CO2有效地转化为CH3COOH,装置如图2所示

(3)阴极电极反应式为
您最近一年使用:0次
解题方法
3 . 己二腈 是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(
是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈( ),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为:
),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为: 。模拟工业电合成己二腈的装置如图所示。
。模拟工业电合成己二腈的装置如图所示。

回答下列问题:
(1)阳极的电极反应式:___________ 。
(2)离子交换膜是___________ (填“阳离子”或“阴离子”)交换膜。
(3)丙烯腈在阴极转化为己二腈分三步:请用离子方程式表述相关过程。
第一步:___________ 。
第二步:
第三步:___________ 。
 是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(
是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈( ),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为:
),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为: 。模拟工业电合成己二腈的装置如图所示。
。模拟工业电合成己二腈的装置如图所示。
回答下列问题:
(1)阳极的电极反应式:
(2)离子交换膜是
(3)丙烯腈在阴极转化为己二腈分三步:请用离子方程式表述相关过程。
第一步:
第二步:

第三步:
您最近一年使用:0次
名校
4 . 镍氢电池广泛用于油电一体的混合动力汽车,该电池材料的回收利用也成为研究热点。
Ⅰ.某品牌镍氢电池的总反应为 ,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
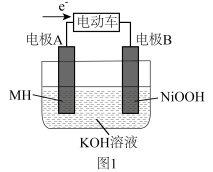
(1)混合动力车上坡时利用电池放电提供能源。
①电极A是_______ (填“正极”或“负极”)。
②正极的电极反应式为_______ 。
(2)混合动力车下坡时利用动能回收给电池充电,此时电极A附近的pH_______ (填“变大”“不变”或“变小”)
Ⅱ.该品牌废旧镍氢电池回收过程中,金属镍的转化过程如下:

转化过程中所用 和NaOH溶液通过电解
和NaOH溶液通过电解 溶液获得,装置如图2。
溶液获得,装置如图2。
已知:阴离子交换膜可选择性透过阴离子,阳离子交换膜可选择性透过阳离子。

(3)图2中,电极C为电解池的_______ (填“阴极”或“阳极”)。
(4)产生 的是
的是_______ (填“甲池”“乙池”或“丙池”),结合化学用语说明产生 的原理:
的原理:_______ 。
(5)回收该品牌废旧镍氢电池过程中,在阴极收集到气体134.4L(标准状况下),理论上最多可回收得到 (摩尔质量为
(摩尔质量为 )的质量为
)的质量为_______ 。
Ⅰ.某品牌镍氢电池的总反应为
 ,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
(1)混合动力车上坡时利用电池放电提供能源。
①电极A是
②正极的电极反应式为
(2)混合动力车下坡时利用动能回收给电池充电,此时电极A附近的pH
Ⅱ.该品牌废旧镍氢电池回收过程中,金属镍的转化过程如下:

转化过程中所用
 和NaOH溶液通过电解
和NaOH溶液通过电解 溶液获得,装置如图2。
溶液获得,装置如图2。已知:阴离子交换膜可选择性透过阴离子,阳离子交换膜可选择性透过阳离子。

(3)图2中,电极C为电解池的
(4)产生
 的是
的是 的原理:
的原理:(5)回收该品牌废旧镍氢电池过程中,在阴极收集到气体134.4L(标准状况下),理论上最多可回收得到
 (摩尔质量为
(摩尔质量为 )的质量为
)的质量为
您最近一年使用:0次
2023-01-06更新
|
779次组卷
|
7卷引用:浙江省杭州师范大学附属中学2023-2024学年高二上学期期末考试化学试题
22-23高二上·浙江·期末
解题方法
5 . 甲烷燃料电池采用铂作为电极材料,两个电极上分别通入CH4和O2, 电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。

回答下列问题。
(1)甲烷燃料电池工作时,其负极电极反应为_______ 。
(2)闭合开关K后,a、b电极上均有气体产生,写出b电极反应式_______ 。
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为_______ L(标准状况)。 (写出必要过程)

回答下列问题。
(1)甲烷燃料电池工作时,其负极电极反应为
(2)闭合开关K后,a、b电极上均有气体产生,写出b电极反应式
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为
您最近一年使用:0次
6 . 按图所示装置进行实验(C1、C2为石墨棒),并回答下列问题:
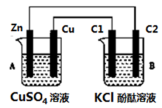
(1)判断装置的名称:A池为___________ ,B池为___________ 。
(2)锌极为___________ 极,电极反应式为___________ ;石墨棒C1为___________ 极,电极反应式为___________ ;
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为___________ 克。

(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为
您最近一年使用:0次
解题方法
7 . 电解法测定铜的相对原子质量的装置如图所示,调节电阻使电流稳定在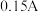 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:

电解前:铜a与铜b的质量分别 和
和 :
:
电解后:铜a与铜b的质量分别 和
和 。
。
已知: 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。
则测得的铜元素的相对原子质量为___________ (计算结果保留3位有效数字),写出简要计算过程___________ 。
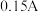 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:
电解前:铜a与铜b的质量分别
 和
和 :
:电解后:铜a与铜b的质量分别
 和
和 。
。已知:
 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。则测得的铜元素的相对原子质量为
您最近一年使用:0次
名校
8 . 电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________ ,阴极反应式为________ 。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是_____ (填序号)。
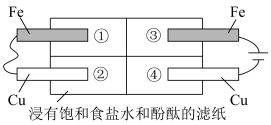
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。

①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________ (填化学式),电极反应式为________ 。电解过程中,阴极区Na2SO4的物质的量________ (填“增大”、“减小”或“不变”)。
②若电解精炼镍则阳极材料为_______ ,铁钉镀锌时连接电源负极的是_______ (填名称)
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度
 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入
②若电解精炼镍则阳极材料为
您最近一年使用:0次
2021-10-22更新
|
88次组卷
|
3卷引用:浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题
9 . 研究电化学原理与应用有非常重要的意义。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是_______ (回答一条即可)。
(2)铅蓄电池是最常见的二次电池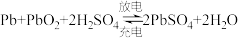 。
。
①充电时阴极反应为_______ 。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为_______ (假设溶液体积不变,产物无损耗)。
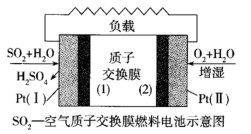
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式_______ 。
(4)高铁酸钠( )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
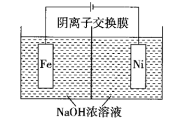
装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在_______ (填“阴极室”或“阳极室”);铁电极发生的反应为_______ 。
(1)与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是
(2)铅蓄电池是最常见的二次电池
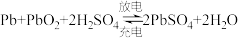 。
。①充电时阴极反应为
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的pH为
(3)二氧化硫—空气质子交换膜燃料电池实现了制硫酸发电、环保三位一体的结合,原理如图所示。Pt(II)上的电极反应式

(4)高铁酸钠(
 )易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为
)易溶于水,是一种新型多功能水处理剂,可以用电解法制取,离子反应为 ,工作原理如图所示。
,工作原理如图所示。
装置通电后,铁电极附近生成紫红色的
 ,镍电极有气泡产生。电解一段时间后,
,镍电极有气泡产生。电解一段时间后, 降低的区域在
降低的区域在
您最近一年使用:0次
10 . 某同学设计实验探究不同电极和电解液对电解水的影响。分别采用石墨和铁钉作为电解材料,电解硫酸和氢氧化钠溶液。预电解2分钟后收集3~8分钟内产生的气体,实验结果如下表所示:
已知氢气和氧气在水中溶解度分别为19 mol·L-1和31 mol·L-1,根据上述测定结果,回答下列问题:
(1)本实验可用如图所示装置收集并测量气体的体积。请简述读取气体体积的操作方法___________ 。

(2)该同学为探究①②中阳极气体偏少的原因(偏离V阳:V阴=1:2),又进行如下实验: 。
a.电解结束后对两电极气体同时减压,发现电极表面再次冒出气泡,相比而言,阳极冒出气体更多。
b.取②实验中少数阳极溶液,分为两份,一份加入稀盐酸溶液,生成无色气体,另一份滴加氯化钡溶液,生成白色沉淀;而取③实验中少数阳极溶液重复上述实验,无类似现象。
c.取①实验中少量阳极溶液,滴加硫酸锰溶液,逐渐变紫红色。
根据a、b、c实验得出的结论___________ 。
(3)另一同学发现③中气体体积比V阳:V阴≈1:2,说明铁作阳极未失去电子产生亚铁离子,其可能的原因是___________ 。
(4)比较实验结果,选择电解水的条件是___________ 。
| 编号 | 电极 | 电解液 | 阳极气体体积/mL | 阴极气体体积/mL | 实验现象 |
| ① | 石墨 | 0.5 mol·L-1硫酸 | 5.55 | 21.88 | 两电极表面产生气泡,阳极管底积有黑色粉末 |
| ② | 石墨 | 1 mol·L-1氢氧化钠 | 5.00 | 16.08 | 两电极表面产生气泡,阳极溶液变黄色 |
| ③ | 铁钉 | 1 mol·L-1氢氧化钠 | 9.13 | 18.22 | 两电极表面产生气泡 |
已知氢气和氧气在水中溶解度分别为19 mol·L-1和31 mol·L-1,根据上述测定结果,回答下列问题:
(1)本实验可用如图所示装置收集并测量气体的体积。请简述读取气体体积的操作方法

(2)该同学为探究①②中阳极气体偏少的原因(偏离V阳:V阴=1:2),又进行如下实验: 。
a.电解结束后对两电极气体同时减压,发现电极表面再次冒出气泡,相比而言,阳极冒出气体更多。
b.取②实验中少数阳极溶液,分为两份,一份加入稀盐酸溶液,生成无色气体,另一份滴加氯化钡溶液,生成白色沉淀;而取③实验中少数阳极溶液重复上述实验,无类似现象。
c.取①实验中少量阳极溶液,滴加硫酸锰溶液,逐渐变紫红色。
根据a、b、c实验得出的结论
(3)另一同学发现③中气体体积比V阳:V阴≈1:2,说明铁作阳极未失去电子产生亚铁离子,其可能的原因是
(4)比较实验结果,选择电解水的条件是
您最近一年使用:0次



