解题方法
1 . 周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: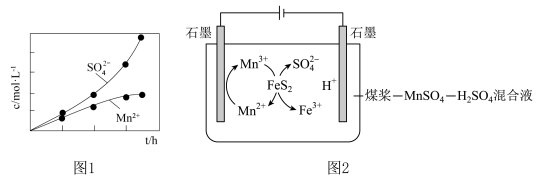
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
您最近一年使用:0次
2 . 按图所示装置进行实验(C1、C2为石墨棒),并回答下列问题:
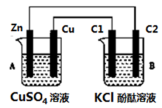
(1)判断装置的名称:A池为___________ ,B池为___________ 。
(2)锌极为___________ 极,电极反应式为___________ ;石墨棒C1为___________ 极,电极反应式为___________ ;
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为___________ 克。

(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为
您最近一年使用:0次
解题方法
3 . 电解法测定铜的相对原子质量的装置如图所示,调节电阻使电流稳定在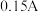 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:

电解前:铜a与铜b的质量分别 和
和 :
:
电解后:铜a与铜b的质量分别 和
和 。
。
已知: 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。
则测得的铜元素的相对原子质量为___________ (计算结果保留3位有效数字),写出简要计算过程___________ 。
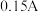 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:
电解前:铜a与铜b的质量分别
 和
和 :
:电解后:铜a与铜b的质量分别
 和
和 。
。已知:
 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。则测得的铜元素的相对原子质量为
您最近一年使用:0次
19-20高二·浙江·期中
解题方法
4 . 某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。

(1)图1中,电解一段时间后,气球b中的气体是_______ (填化学式),U形管_______ (填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84"消毒液的有效成分(NaClO),则c为电源的_______ 极;该发生器中反应的总离子方程式为_______ 。
(3)“盐水动力”玩具车的电池以镁片、活性炭为电极, 向极板上滴加食盐水后电池便可工作,电池反应式为2Mg+O2+2H2O =2Mg(OH)2,正极电极反应式为_______ ,当有2mol Mg损耗时,转移_______ mol电子。

(1)图1中,电解一段时间后,气球b中的气体是
(2)利用图2制作一种环保型消毒液发生器,电解可制备“84"消毒液的有效成分(NaClO),则c为电源的
(3)“盐水动力”玩具车的电池以镁片、活性炭为电极, 向极板上滴加食盐水后电池便可工作,电池反应式为2Mg+O2+2H2O =2Mg(OH)2,正极电极反应式为
您最近一年使用:0次
2020高三·全国·专题练习
5 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。KIO3也可采用“电解法”制备,装置如图所示。回答下列问题:

①写出电解时阴极的电极反应式______ 。
②电解过程中通过阳离子交换膜的离子主要为_________ ,其迁移方向是_____________ 。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
6 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
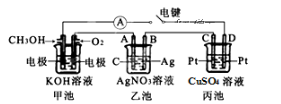
(1)丙池为________ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式为____________________ 。
(2)乙池中A电极为________ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为_________________________ 。
(3)当乙池中B极质量增重10.8g时,甲池中理论上消耗 的体积为
的体积为________ mL(标准状况)。
(4)丙池中,C上的电极反应式为____________________ 。如果起始时盛有1000mL  的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为________ 。

(1)丙池为
(2)乙池中A电极为
(3)当乙池中B极质量增重10.8g时,甲池中理论上消耗
 的体积为
的体积为(4)丙池中,C上的电极反应式为
 的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
7 . 完成下列填空
(1)纯水中存在电离平衡: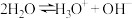 。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式
。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式______ 。
(2)金属钠可以从水中置换氢。在铁作催化剂时,金属钠也可以和液氨反应产生氢气和一种离子化合物X,写出化合物X的电子________ 。
(3)已知25℃时, 的燃烧热为1366
的燃烧热为1366 ,写出其燃烧热的热化学方程式:
,写出其燃烧热的热化学方程式:_______ 。
(4)硫化氢是一种气态废弃物,可电解 和
和 混合溶液后通入
混合溶液后通入 气体,
气体, 转化为可利用的硫过程为
转化为可利用的硫过程为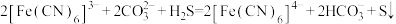 。请写出电解时阴极的电极反应式:
。请写出电解时阴极的电极反应式:___________ 。
(5)苯酚钠水溶液中通入少量 的化学方程式
的化学方程式________ 。
(6)有机物分子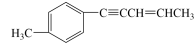 中最多有
中最多有________ 原子在一条直线上;
(7)3,3-二甲基-2-溴丁烷在 乙醇溶液中共热发生的反应方程式:
乙醇溶液中共热发生的反应方程式:____________ 。
(1)纯水中存在电离平衡:
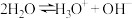 。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式
。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式(2)金属钠可以从水中置换氢。在铁作催化剂时,金属钠也可以和液氨反应产生氢气和一种离子化合物X,写出化合物X的电子
(3)已知25℃时,
 的燃烧热为1366
的燃烧热为1366 ,写出其燃烧热的热化学方程式:
,写出其燃烧热的热化学方程式:(4)硫化氢是一种气态废弃物,可电解
 和
和 混合溶液后通入
混合溶液后通入 气体,
气体, 转化为可利用的硫过程为
转化为可利用的硫过程为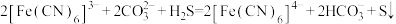 。请写出电解时阴极的电极反应式:
。请写出电解时阴极的电极反应式:(5)苯酚钠水溶液中通入少量
 的化学方程式
的化学方程式(6)有机物分子
 中最多有
中最多有(7)3,3-二甲基-2-溴丁烷在
 乙醇溶液中共热发生的反应方程式:
乙醇溶液中共热发生的反应方程式:
您最近一年使用:0次
9-10高二下·浙江台州·阶段练习
解题方法
8 . 从H+、Cu2+、Na+、SO42-、Cl-等五种离子中选择适当的离子组成电解质,使之符合下列要求。
(1)以碳棒为电极,电解时电解质质量减小,水量不变,应选用的电解质是________________________________ ;
(2)以碳棒为电极,电解时电解质质量不变,水量减少,应选用的电解质是________________________________ ;
(3)以碳棒为阳极,铁棒为阴极,电解时电解质质量和水量都减少,则应选用的电解质是_________________________________ 。
(1)以碳棒为电极,电解时电解质质量减小,水量不变,应选用的电解质是
(2)以碳棒为电极,电解时电解质质量不变,水量减少,应选用的电解质是
(3)以碳棒为阳极,铁棒为阴极,电解时电解质质量和水量都减少,则应选用的电解质是
您最近一年使用:0次



