名校
1 . 电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________ ,阴极反应式为________ 。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是_____ (填序号)。
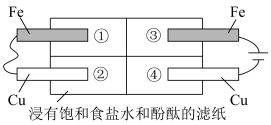
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。

①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________ (填化学式),电极反应式为________ 。电解过程中,阴极区Na2SO4的物质的量________ (填“增大”、“减小”或“不变”)。
②若电解精炼镍则阳极材料为_______ ,铁钉镀锌时连接电源负极的是_______ (填名称)
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度
 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入
②若电解精炼镍则阳极材料为
您最近一年使用:0次
2021-10-22更新
|
88次组卷
|
3卷引用:浙江省舟山市舟山中学2022-2023学年高二上学期阶段性质量监测化学试题



