名校
1 . 电絮凝技术(EC)是一种集混凝、气浮、电化学于一体的新兴水处理技术,实验表明电絮凝技术能除去废水中96%以上的磷(主要以PO 形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
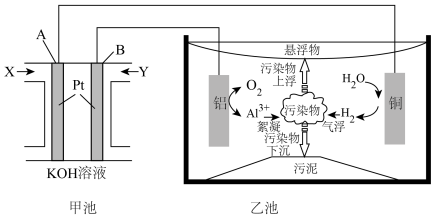
回答下列问题:
(1)燃料电池中OH-向___________ 极(填A或B)移动。写出A电极反应式___________ 。
(2)乙池中铜电极发生___________ 反应(填“氧化”或“还原”)。
(3)乙池铝电极上存在两个竞争反应,电极反应式分别为___________ ,___________ 。
(4)乙池由于电解过程中产生能吸附水中油污等污染物。用离子方程式说明净水的原因为___________ 。
 形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
回答下列问题:
(1)燃料电池中OH-向
(2)乙池中铜电极发生
(3)乙池铝电极上存在两个竞争反应,电极反应式分别为
(4)乙池由于电解过程中产生能吸附水中油污等污染物。用离子方程式说明净水的原因为
您最近一年使用:0次
名校
解题方法
2 . 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

请回答下列问题:
(1)A极是电源的___________ ,一段时间后,甲中溶液颜色___________ ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________ ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、E电极均只有一种单质生成时,对应单质的物质的量之比为______ 。
(3)现用丙装置给铜件镀银,则G应是___________ (填“镀层金属”或“镀件”),电镀液是___________ 溶液。当乙中溶液的pH是12时(此时乙溶液体积为 ),丙中镀件上析出银的质量为
),丙中镀件上析出银的质量为___________ ,甲中溶液的
___________ (填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为___________ 。

请回答下列问题:
(1)A极是电源的
(2)若甲、乙装置中的C、E电极均只有一种单质生成时,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则G应是
 ),丙中镀件上析出银的质量为
),丙中镀件上析出银的质量为
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 按照要求回答下列问题。
(1)工业上,在强碱性条件下用电解法除去废水中的 ,装置如图1所示,依次发生的反应有:
,装置如图1所示,依次发生的反应有:
i.
ii.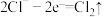
iii.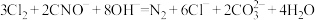

①a为电源_______ 极。
②通电过程中溶液pH不断_______ (填“增大”“减小”或“不变”)。
③除去1mol ,外电路中至少需要转移
,外电路中至少需要转移_______ mol电子。
④为了使电解池连续工作,需要不断补充_______ 。
(2)用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图2所示(电极材料为石墨)。
,其原理如图2所示(电极材料为石墨)。

①图中a极要连接电源的_______ (填“正”或“负”)极,C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:_______ 。
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图3所示。
的反应原理如图3所示。

①作负极的物质是_______ 。
②正极的电极反应式是_______ 。
(1)工业上,在强碱性条件下用电解法除去废水中的
 ,装置如图1所示,依次发生的反应有:
,装置如图1所示,依次发生的反应有:i.

ii.
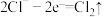
iii.
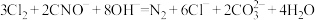

①a为电源
②通电过程中溶液pH不断
③除去1mol
 ,外电路中至少需要转移
,外电路中至少需要转移④为了使电解池连续工作,需要不断补充
(2)用NaOH溶液吸收烟气中的
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图2所示(电极材料为石墨)。
,其原理如图2所示(电极材料为石墨)。
①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:
(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图3所示。
的反应原理如图3所示。
①作负极的物质是
②正极的电极反应式是
您最近一年使用:0次
名校
4 . 2021年12月9日,神舟十三号航天员翟志刚、王亚平和叶光富在中国空间站太空授课,空间站内氧气和二氧化碳的循环利用引发了同学们强烈的好奇心。请根据有关信息回答下列问题。
(1)空间站主要利用电解生活废水及尿液实现氧气再生,阳极的电极反应式为______ 。
(2)叶光富介绍,有望在空间站利用CO2与H2反应生成水和燃料,实现呼吸产生的CO2与电解水产生的H2的高效循环利用。二氧化碳与氢气制甲醇的总反应可表示为:CO2(g)+3H2(g)→CH3OH(g)+H2O(g) △H。
该反应一般通过如下步骤来实现:
i.CO2(g)+H2(g)→CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+2H2(g)→CH3OH(g) △H2=-90kJ•mol-1
①总反应的△H=_____ kJ•mol-1;若反应i为慢反应,下列示意图中能体现上述反应能量变化的是_____ (填标号),判断的理由是_____ 。
A. B.
B.
C.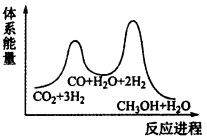 D.
D.
②甲醇是燃料电池的重要原料,若电解质为H2SO4溶液,则负极的电极反应式为_____ 。
(3)利用电化学原理可以将H2O和CO2转化为O2和燃料(C3H8O),实验装量如图所示,则H+移向_____ 极(填“a”或“b”)。

(1)空间站主要利用电解生活废水及尿液实现氧气再生,阳极的电极反应式为
(2)叶光富介绍,有望在空间站利用CO2与H2反应生成水和燃料,实现呼吸产生的CO2与电解水产生的H2的高效循环利用。二氧化碳与氢气制甲醇的总反应可表示为:CO2(g)+3H2(g)→CH3OH(g)+H2O(g) △H。
该反应一般通过如下步骤来实现:
i.CO2(g)+H2(g)→CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+2H2(g)→CH3OH(g) △H2=-90kJ•mol-1
①总反应的△H=
A.
 B.
B.
C.
 D.
D.
②甲醇是燃料电池的重要原料,若电解质为H2SO4溶液,则负极的电极反应式为
(3)利用电化学原理可以将H2O和CO2转化为O2和燃料(C3H8O),实验装量如图所示,则H+移向

您最近一年使用:0次
2023-01-08更新
|
196次组卷
|
2卷引用:黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题
22-23高二上·全国·课后作业
解题方法
5 . 请按要求回答下列问题。
(1)根据图1回答①②:
A电极可观察到的现象是_______ ;B电极的电极反应式为_______ 。
②打开K1,合并K2。
A电极可观察到的现象是_______ ;B电极的电极反应式为_______ ;
(2)根据图2回答③④:_______ ,电解反应的离子方程式为_______ ;
④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积为_______ L。
(1)根据图1回答①②:

A电极可观察到的现象是
②打开K1,合并K2。
A电极可观察到的现象是
(2)根据图2回答③④:

④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积为
您最近一年使用:0次
解题方法
6 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。
Ⅰ.用图甲所示装置进行第一组实验时:
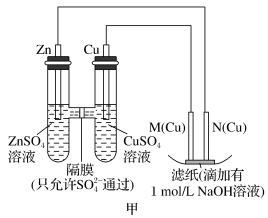
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______(填字母)。
(2)实验过程中,
_______ (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象是_______ 。
Ⅱ.该小组同学用图乙所示装置打算进行二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根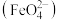 在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
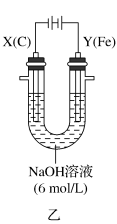
(3)电解过程中,X极处溶液的 浓度
浓度_______ (填“增大”“减小”或“不变)。
(4)电解过程中,Y极发生的电极反应为 和
和_______ 。
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为_______ mL(均已折算为标准状况时气体体积)。
(6)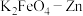 也可以组成碱性电池,
也可以组成碱性电池, 在电池中作为正极材料,其电池反应总反应式为
在电池中作为正极材料,其电池反应总反应式为 ,该电池正极发生的电极反应式为
,该电池正极发生的电极反应式为_______ 。
Ⅰ.用图甲所示装置进行第一组实验时:

(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______(填字母)。
| A.石墨 | B.镁 | C.银 | D.铂 |

Ⅱ.该小组同学用图乙所示装置打算进行二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根
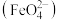 在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
(3)电解过程中,X极处溶液的
 浓度
浓度(4)电解过程中,Y极发生的电极反应为
 和
和(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为
(6)
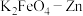 也可以组成碱性电池,
也可以组成碱性电池, 在电池中作为正极材料,其电池反应总反应式为
在电池中作为正极材料,其电池反应总反应式为 ,该电池正极发生的电极反应式为
,该电池正极发生的电极反应式为
您最近一年使用:0次
解题方法
7 . 降低能耗是氯碱工业发展的重要方向。我国利用氯碱厂生产的H2作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
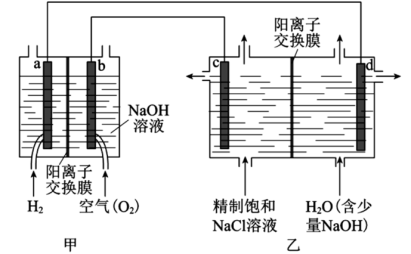
(1)a极为_______ (填“正”或“负”)极,c 极为_______ (填“阴”或“阳”)极。
(2)乙装置中电解饱和NaCl溶液的化学方程式为_______ ;反应一段时间后,d极产生1mol气体时,乙装置中转移电子_______ mol。
(3)下列说法正确的是_______ (填字母序号)。
A.甲装置可实现化学能向电能的转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(4)实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为_______ 。

(1)a极为
(2)乙装置中电解饱和NaCl溶液的化学方程式为
(3)下列说法正确的是
A.甲装置可实现化学能向电能的转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(4)实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为
您最近一年使用:0次
2022-01-17更新
|
208次组卷
|
4卷引用:黑龙江省齐齐哈尔市三立高级中学2021-2022学年高二下学期开学考试化学试题
名校
解题方法
8 . 根据下图,回答下列问题:

(1)若闭合S1,装置属于___________ 。
(2)若闭合S2,装置属于___________ ,锌极上的反应为___________ 。
(3)若闭合S3,总反应为___________ 。

(1)若闭合S1,装置属于
(2)若闭合S2,装置属于
(3)若闭合S3,总反应为
您最近一年使用:0次
解题方法
9 . 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为___________ 。
② Y电极上的电极反应式为___________
③该反应的总反应方程式是:___________
(2)如要用电镀方法铁上镀铜,电解液a选用CuSO4溶液,则
① X电极的材料是___________ ,电极反应式是___________ 。
② Y电极的材料是___________ ,电极反应式是___________ 。

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为
② Y电极上的电极反应式为
③该反应的总反应方程式是:
(2)如要用电镀方法铁上镀铜,电解液a选用CuSO4溶液,则
① X电极的材料是
② Y电极的材料是
您最近一年使用:0次
名校
解题方法
10 . 某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
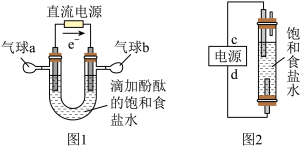
(1)图 1 中,电解一段时间后,气球 b 中的气体是___ (填化学式),U 形管___ (填“左”或“右”)边的溶液变红。
(2)利用图 2 制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则 c 为电源的_____ 极;该发生器中反应的总离子方程式为_____ 。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上。该工艺的相关物质运输与转化关系如图 3 所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
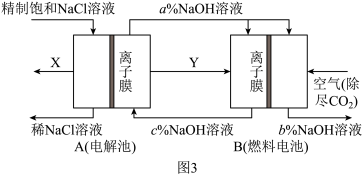
燃料电池 B 中的电极反应式分别为负极_____ , 正极____ 。

(1)图 1 中,电解一段时间后,气球 b 中的气体是
(2)利用图 2 制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则 c 为电源的
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上。该工艺的相关物质运输与转化关系如图 3 所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

燃料电池 B 中的电极反应式分别为负极
您最近一年使用:0次
2021-03-26更新
|
218次组卷
|
4卷引用:黑龙江省齐齐哈尔市第八中学2020-2021学年高二上学期期中考试化学试题
黑龙江省齐齐哈尔市第八中学2020-2021学年高二上学期期中考试化学试题黑龙江省友谊县高级中学2022-2023学年高二上学期期末考试(新教材)化学试题(已下线)练习9 电解池-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)浙江省湖州市德清县第三中学2020-2021学年高二下学期返校考试化学试题



