1 . 已知:锂钴电池总反应: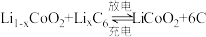 ,过程如图:
,过程如图:
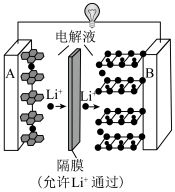
(1) 中,Co元素的化合价为
中,Co元素的化合价为___________ ;锂电池发生火灾时,和氧气发生反应的主要物质是___________ (填“正”或“负”)极材料;充电时阳极的反应方程式是___________ 。
(2)锂电池成本高昂,废弃后需回收其中的锂和钴元素,先将上述锂电池进行放电处理,拆卸后,再将正极材料 涂覆在铝箔上,进行电解,浸出
涂覆在铝箔上,进行电解,浸出 和
和 ,装置如图所示,该条件下副反应忽略不计。
,装置如图所示,该条件下副反应忽略不计。
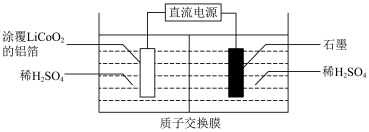
①拆卸前,将锂电池放电处理有利于锂在正极的回收,其原因是___________ 。
②石墨电极连接电源的___________ 极(填“正”或“负”)。
③结合电极反应,指出阴极室的pH变化并解释原因:___________ 。
(3)当前,三元正极材料——镍钴锰酸锂应用广泛,其化学式可写作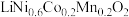 。可用
。可用 、
、 、
、 、
、 与空气混合加热烧结制得,写出制备的化学方程式:
与空气混合加热烧结制得,写出制备的化学方程式:___________ (设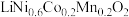 的计量系数为1)。
的计量系数为1)。
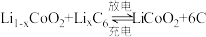 ,过程如图:
,过程如图:
(1)
 中,Co元素的化合价为
中,Co元素的化合价为(2)锂电池成本高昂,废弃后需回收其中的锂和钴元素,先将上述锂电池进行放电处理,拆卸后,再将正极材料
 涂覆在铝箔上,进行电解,浸出
涂覆在铝箔上,进行电解,浸出 和
和 ,装置如图所示,该条件下副反应忽略不计。
,装置如图所示,该条件下副反应忽略不计。
①拆卸前,将锂电池放电处理有利于锂在正极的回收,其原因是
②石墨电极连接电源的
③结合电极反应,指出阴极室的pH变化并解释原因:
(3)当前,三元正极材料——镍钴锰酸锂应用广泛,其化学式可写作
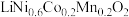 。可用
。可用 、
、 、
、 、
、 与空气混合加热烧结制得,写出制备的化学方程式:
与空气混合加热烧结制得,写出制备的化学方程式: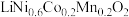 的计量系数为1)。
的计量系数为1)。
您最近一年使用:0次
名校
解题方法
2 . 完成下列问题。
(1)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
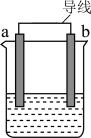
①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为_______ ,当电路中有0.2mol电子通过时,负极的质量减少_______ g。
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置_______ (填“能”或“不能”)形成原电池
(2)将锌片和银片浸入硫酸铜溶液中组成原电池,两电极间连接一个电流表。
①锌片上发生的电极反应为_______ ;
②银片上发生的电极反应为_______ 。
③溶液中的 向
向_______ (填“Zn”或者“Ag”)移动。
(3)当在a附近有气泡产生,b电极逐渐溶解,则____ (a或b)作负极。
(1)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。

①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置
(2)将锌片和银片浸入硫酸铜溶液中组成原电池,两电极间连接一个电流表。
①锌片上发生的电极反应为
②银片上发生的电极反应为
③溶液中的
 向
向(3)当在a附近有气泡产生,b电极逐渐溶解,则
您最近一年使用:0次
名校
3 . 如图是一个化学过程的示意图,回答下列问题:
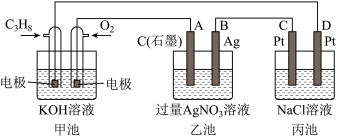
(1)甲池是_______ 装置,电极B的名称是_______ 。
(2)甲装置中通入 的电极反应
的电极反应_______ ,丙装置中D极的产物是_______ (写化学式)。
(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的
_______ 。(已知:NaCl溶液足量,电解后溶液体积为200mL)。乙池的PH值将_______ (填“变大”、“变小”或“不变”)
(4)若要使乙池恢复电解前的状态,应向乙池中加入_______ (写物质化学式)。

(1)甲池是
(2)甲装置中通入
 的电极反应
的电极反应(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的

(4)若要使乙池恢复电解前的状态,应向乙池中加入
您最近一年使用:0次
名校
解题方法
4 . 如图所示的装置进行电解。通电一会儿,发现湿润的淀粉 试纸的C端变为蓝色。
试纸的C端变为蓝色。
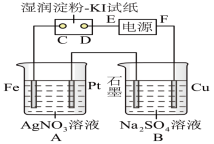
(1)E为电源的_______ 极
(2)A中发生反应的化学方程式为_______ 。
(3)在B中观察到的现象是_______ 。
(4)D端的电极反应式为_______ 。
(5)若用惰性电极电解
 的
的 溶液,若阳极产生
溶液,若阳极产生 (标况下)的气体,此时溶液中pH为
(标况下)的气体,此时溶液中pH为_______ (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入_______ (填字母序号)。
A. B.
B. C.
C. D.
D.
(6)铅蓄电池是一种广泛使用的二次电池,其放电时的正极的电极反应式为____ 。
 试纸的C端变为蓝色。
试纸的C端变为蓝色。
(1)E为电源的
(2)A中发生反应的化学方程式为
(3)在B中观察到的现象是
(4)D端的电极反应式为
(5)若用惰性电极电解

 的
的 溶液,若阳极产生
溶液,若阳极产生 (标况下)的气体,此时溶液中pH为
(标况下)的气体,此时溶液中pH为A.
 B.
B. C.
C. D.
D.
(6)铅蓄电池是一种广泛使用的二次电池,其放电时的正极的电极反应式为
您最近一年使用:0次
解题方法
5 . 装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的________ 极,C极的电极反应式为_____________ ,
(2)一段时间后丁中X极附近的颜色逐渐____________ (填“变深”或“变浅”)。
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为_____________ 。
(4)现用丙装置给铜件镀银,则H应该是______ (填“铜”或“银”),电镀液是__________ 溶液。常温下,当乙中溶液的c(OH-)=0.1mol·L-1时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为____________ g。
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为____ mol。

(1)B极是电源的
(2)一段时间后丁中X极附近的颜色逐渐
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(4)现用丙装置给铜件镀银,则H应该是
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为
您最近一年使用:0次
名校
解题方法
6 . 如图所示3套实验装置,分别回答下列问题。
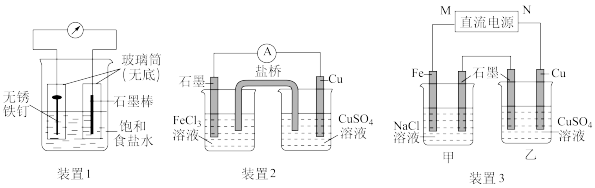
(1)装置1石墨棒电极反应式为___________ 。
(2)装置2一段时间后右池溶液中c(Cu2+)___________ (填“增大”、“减小”或“不变”),若该装置的盐桥中盛装的是NH4NO3的琼脂溶液,则盐桥中的___________ 离子(填“ ”或“
”或“ ”)向硫酸铜溶液迁移。
”)向硫酸铜溶液迁移。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。观察到乙烧杯的石墨电极上有气泡生成。
①电源的M端为___________ 极;甲烧杯中铁电极的电极反应式为___________ 。
②乙烧杯中电解反应的离子方程式为___________ 。
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为___________ mL。

(1)装置1石墨棒电极反应式为
(2)装置2一段时间后右池溶液中c(Cu2+)
 ”或“
”或“ ”)向硫酸铜溶液迁移。
”)向硫酸铜溶液迁移。(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。观察到乙烧杯的石墨电极上有气泡生成。
①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为
您最近一年使用:0次
名校
解题方法
7 . 如图所示,A为电源,B为浸透饱和食盐水和酚酞的滤纸,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1,断开K2,通电后,d端显红色,则电源a端为______ 极,若c、d为惰性电极,c端的电极反应是______ ;检验c端产物的方法______ 。
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0. lmol,断开K1,闭合K2通电一段时间后, 阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是______ 。

(3)D装置中反应的化学方程式______ 。

(1)闭合K1,断开K2,通电后,d端显红色,则电源a端为
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0. lmol,断开K1,闭合K2通电一段时间后, 阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

(3)D装置中反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题
(1)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到更多H2SO4,其原理如图所示(电板材料为石墨)。

①图中a板要连接电源的___________ (填“正”或“负”)板,上图中硫酸的质量分数比较a%___________ b%(填“>”“﹤”或“=”)。
② 在b极上的电极反应式为
在b极上的电极反应式为___________ 。
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如下图所示。该电池在正极生成 的电极反应式为
的电极反应式为___________ ,A物质是___________ 。

(3)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如下图是一个电化学过程的示意图。请填空:

①充电时,原电池的负极与电源___________ 极相连,B极的电极反应式为___________ 。
②放电时,负极的电极反应式为___________ 。
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2___________ L(标准状况下)。
(1)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到更多H2SO4,其原理如图所示(电板材料为石墨)。

①图中a板要连接电源的
②
 在b极上的电极反应式为
在b极上的电极反应式为(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,电池装置如下图所示。该电池在正极生成
 的电极反应式为
的电极反应式为
(3)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如下图是一个电化学过程的示意图。请填空:

①充电时,原电池的负极与电源
②放电时,负极的电极反应式为
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2
您最近一年使用:0次
名校
解题方法
9 . 电解原理在化学领域应用广泛
如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是_______ ;
②电解一段时间后,该反应总离子方程式_______ ;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ 电解一段时间后,CuSO4溶液浓度_______ (填“增大”、减小”或“不变”)。
(3)若X、Y都是惰性电极,a是溶质为Cu(NO3)2和X(NO3)3,且均为0.1 mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图2所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是_______ 。

如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是
②电解一段时间后,该反应总离子方程式
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是
(3)若X、Y都是惰性电极,a是溶质为Cu(NO3)2和X(NO3)3,且均为0.1 mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图2所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

您最近一年使用:0次
2021-11-17更新
|
854次组卷
|
5卷引用:吉林省长春市第二实验中学2021-2022学年高二上学期期中考试化学试题
吉林省长春市第二实验中学2021-2022学年高二上学期期中考试化学试题(已下线)第六单元 化学反应与能量(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)4.2.1 电解原理-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)4.3.2 电解原理的应用-2021-2022学年高二化学课后培优练(人教版选修4)河北省唐山十县一中联盟2022-2023学年高二上学期期中考试化学试题
名校
解题方法
10 . 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得e电极上收集到气体在标准状况下体积为4.48L,乙中c电极质量增加。据此回答问题:
①电源的N端为___________ 极。
②电极b上发生的电极反应为___________ 。
③电解前后甲溶液pH___________ ;乙溶液pH___________ ;丙溶液pH___________ 。(填“变大”、“变小”或“不变”)。
(2)写出乙溶液中的电解反应方程式:___________ 需加入___________ g___________ (填物质名称)恢复原溶液。

(1)接通电源,经过一段时间后,测得e电极上收集到气体在标准状况下体积为4.48L,乙中c电极质量增加。据此回答问题:
①电源的N端为
②电极b上发生的电极反应为
③电解前后甲溶液pH
(2)写出乙溶液中的电解反应方程式:
您最近一年使用:0次
2021-07-16更新
|
272次组卷
|
2卷引用:吉林省梅河口市第五中学2021-2022学年高二上学期第一次月考化学试题



