1 . 完成下列小题
(1)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:_____ 。
②电解过程中丙池中发生的总反应方程式为:_____ 。
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为_____ g。
(2)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:_____ 。
②两池工作时,电池的电极M应与电解池的_____ (填a或b)极相连接;1、2、3膜为阴膜的是:_____ 。
③产品室中发生的离子反应为:_____
(1)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:
②电解过程中丙池中发生的总反应方程式为:
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为
(2)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:
②两池工作时,电池的电极M应与电解池的
③产品室中发生的离子反应为:
您最近一年使用:0次
名校
2 . 下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,要实现铁电极上镀银。请回答下列问题:
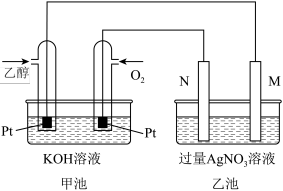
(1)M电极的材料是_____ ,电极名称是_____ ,N的电极反应式为_____ ,加入乙醇的铂电极的电极反应式_____ 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为_____ L(标准状况下);若此时乙池溶液的体积为400mL,则常温下乙池中溶液的pH为_____ 。若要使乙池中AgNO3溶液复原,可以加下列物质中的_____ 。
A.Ag B.Ag2O C.AgNO3

(1)M电极的材料是
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
A.Ag B.Ag2O C.AgNO3
您最近一年使用:0次
名校
3 . 当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下列问题:
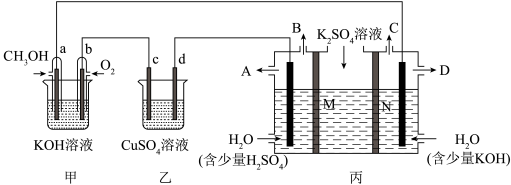
(1)甲装置是___________ (填“原电池”或“电解池”),写出a极的电极反应___________ 。
(2)乙池中c极的电极反应___________ 。
(3)当b极消耗标准状况下的O2112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=___________ 。
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为___________ (写化学式),M为___________ 离子交换膜(填“阴”或“阳”)。

(1)甲装置是
(2)乙池中c极的电极反应
(3)当b极消耗标准状况下的O2112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为
您最近一年使用:0次
2023-03-27更新
|
353次组卷
|
3卷引用:江西省丰城中学2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
4 . 某小组同学设想利用燃料电池和电解池组合,设计一种制备硫酸和氨的装置,相关的物质及工作原理示意图如图。a、b、c、d均为惰性电极,电解池中d上有可催化N2放电的纳米颗粒,固体氧化物电解质只允许O2-在其中迁移。
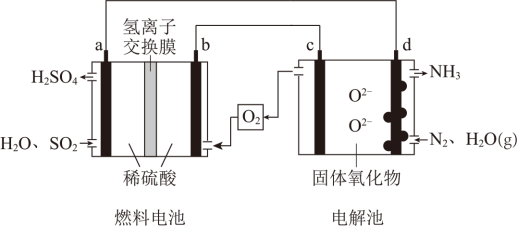
(1)燃料电池制备硫酸。
①a为_____ (填“正极”或“负极”),电极反应式为_____ 。
②H+的迁移方向为______ (填“a→b”或“b→a”)。
③电池总反应的化学方程式为______ 。
(2)电解池制备氨。下列关于电解过程的说法正确的是_____ 。
A.d上,N2被还原
B.c的电极反应:2O2--4e-=O2↑
C.固体氧化物中O2-的迁移方向为d→c
(3)燃料电池中每消耗48gSO2,在电解池中,理论上产生的NH3在标准状况下的体积为_____ L。

(1)燃料电池制备硫酸。
①a为
②H+的迁移方向为
③电池总反应的化学方程式为
(2)电解池制备氨。下列关于电解过程的说法正确的是
A.d上,N2被还原
B.c的电极反应:2O2--4e-=O2↑
C.固体氧化物中O2-的迁移方向为d→c
(3)燃料电池中每消耗48gSO2,在电解池中,理论上产生的NH3在标准状况下的体积为
您最近一年使用:0次
2023-01-07更新
|
410次组卷
|
5卷引用:江西省丰城中学2022-2023学年高二下学期入学考试化学试题
名校
5 . 氨是一种理想的氢载体,几乎可以用于所有类型的内燃机,在以后有望取代部分液体化石燃料。一种在酸性介质中电催化合成氨的示意图如图:____ (填“电”或“化学”,下同)能转化为____ 能。
(2)电极乙为____ (填“正极”、“负极”、“阴极”或“阳极”),该电极的电极反应式为____ 。随着电催化合成的进行,左室溶液的pH会____ (填“变大”、“变小”或“不变”)。
(3)当有0.3molH+通过质子交换膜时。标准状况下产生NH3的体积为_____ L,生成O2的质量为____ g。
(4)目前已实现以铝作为负极,石墨烯负载钯作为正极,采用Al2Cl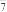 离子型液体(非水溶液)构建Al—N2电池体系。制备的AlN可在碱性溶液中转化为NH3·H2O,从而实现氨的合成,请写出放电过程中,AlN转化为NH3·H2O的离子方程式:
离子型液体(非水溶液)构建Al—N2电池体系。制备的AlN可在碱性溶液中转化为NH3·H2O,从而实现氨的合成,请写出放电过程中,AlN转化为NH3·H2O的离子方程式:____ 。
(5)气体扩散层和选用Al2Cl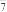 离子型液体都可有效防止阴极产生
离子型液体都可有效防止阴极产生____ (填物质名称)。

(2)电极乙为
(3)当有0.3molH+通过质子交换膜时。标准状况下产生NH3的体积为
(4)目前已实现以铝作为负极,石墨烯负载钯作为正极,采用Al2Cl
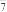 离子型液体(非水溶液)构建Al—N2电池体系。制备的AlN可在碱性溶液中转化为NH3·H2O,从而实现氨的合成,请写出放电过程中,AlN转化为NH3·H2O的离子方程式:
离子型液体(非水溶液)构建Al—N2电池体系。制备的AlN可在碱性溶液中转化为NH3·H2O,从而实现氨的合成,请写出放电过程中,AlN转化为NH3·H2O的离子方程式:(5)气体扩散层和选用Al2Cl
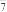 离子型液体都可有效防止阴极产生
离子型液体都可有效防止阴极产生
您最近一年使用:0次
2022-02-22更新
|
125次组卷
|
2卷引用:江西省宜春市丰城中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
6 . A、B、C为三种强电解质,它们在水中电离出的离子如下表所示:
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
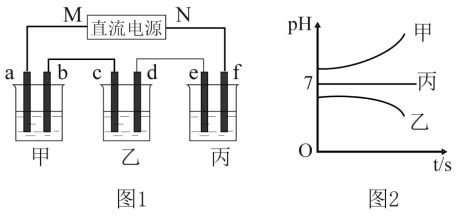
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。据此回答下列问题:
(1)M为电源的___ (填“正”或“负”)极,电极b上发生的电极反应为___ 。
(2)写出乙烧杯中的电池反应方程式:_____ 。
(3)若经过这一段时间后,要使丙恢复到原来的状态,需要进行的操作是___ 。
(4)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为______ ;反应进行一段时间后溶液C的pH将______ (填“升高”“降低”或“基本不变”)。
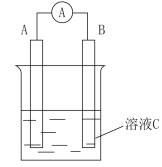
(5)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO -4e-=4CO2,正极反应式为
-4e-=4CO2,正极反应式为___ 。
阳离子 | 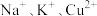 |
阴离子 | 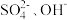 |
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。

接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。据此回答下列问题:
(1)M为电源的
(2)写出乙烧杯中的电池反应方程式:
(3)若经过这一段时间后,要使丙恢复到原来的状态,需要进行的操作是
(4)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为

(5)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO
 -4e-=4CO2,正极反应式为
-4e-=4CO2,正极反应式为
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题

(1)用惰性电极电解足量硫酸铜溶液,其阴极反应式为___________ ;
(2)铅蓄电池是可充放电的二次电池,其放电时正极反应式为___________ ;
(3)碱性条件下甲醇燃料电池的负极反应式为___________ ;
(4)连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图1所示,a电极反应为___________
(5)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图2装置处理有机废水(以含CH3COO-的溶液为例)。a电极反应式为___________ 。

(1)用惰性电极电解足量硫酸铜溶液,其阴极反应式为
(2)铅蓄电池是可充放电的二次电池,其放电时正极反应式为
(3)碱性条件下甲醇燃料电池的负极反应式为
(4)连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图1所示,a电极反应为
(5)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图2装置处理有机废水(以含CH3COO-的溶液为例)。a电极反应式为
您最近一年使用:0次
2021-11-26更新
|
528次组卷
|
5卷引用:江西省景德镇一中2022-2023学年高一下学期期中考试(19班)化学试题
江西省景德镇一中2022-2023学年高一下学期期中考试(19班)化学试题福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题(已下线)周末培优4 新型电池的电化学原理问题-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)4.2.1 电解原理-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第四章 电化学基础 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)
名校
解题方法
8 . 有机电合成是用电化学的方法进行有机合成的技术。下图是在KI-CH3OK-CH3OH体系中,以石墨为电极电解2-丁酮(C4H8O)制备有机物3-碘-2-丁酮(C4H7OI)的原理图。回答相应问题。

(1)石墨A连接电源的___________ 极。
(2)石墨B上发生的电极反应式为___________ 。
(3)反应①的方程式为___________ 。
(4)整个过程的总反应离子方程式为___________ 。
(5)当电路中通过0.2mol电子时,会生成物质D的质量为___________ 。

(1)石墨A连接电源的
(2)石墨B上发生的电极反应式为
(3)反应①的方程式为
(4)整个过程的总反应离子方程式为
(5)当电路中通过0.2mol电子时,会生成物质D的质量为
您最近一年使用:0次
解题方法
9 . 某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:


①图中X溶液是___________ ;
②石墨电极上发生的电极反应式为___________ ;
(2)将上述反应设计成的电解池如图乙所示,图丙中的①②③分别表示乙烧杯中某种金属阳离子的物质的量与电子转移的物质的量的变化关系,请回答下列问题:
①M是___________ 极;
②图丙中的②线是___________ 的变化。
③当电子转移为2 mol时,向乙烧杯中加入___________ L 5 mol·L-1 NaOH溶液才能使Cu2+沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O Na2FeO4+3H2↑,则电解时阳极的电极反应式是
Na2FeO4+3H2↑,则电解时阳极的电极反应式是___________ 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为___________ 。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:


①图中X溶液是
②石墨电极上发生的电极反应式为
(2)将上述反应设计成的电解池如图乙所示,图丙中的①②③分别表示乙烧杯中某种金属阳离子的物质的量与电子转移的物质的量的变化关系,请回答下列问题:
①M是
②图丙中的②线是
③当电子转移为2 mol时,向乙烧杯中加入
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O
 Na2FeO4+3H2↑,则电解时阳极的电极反应式是
Na2FeO4+3H2↑,则电解时阳极的电极反应式是②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为
您最近一年使用:0次
20-21高二上·江西南昌·期中
解题方法
10 . 我国科学家设计了一种锂离子电池,并用此电池来电解含有Na2SO3的工业废水,可获得硫酸等物质,该过程示意图如图:
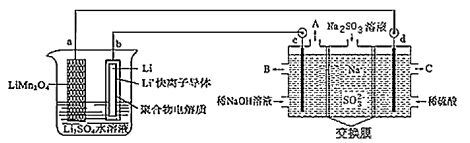
(1)锂离子电池工作时,a极发生_______ (填“氧化”或“还原”)反应, Li+移向_____ (填“a”或“b”)极, 写出b极的电极反应__________ 。
(2)电解池中物质A的化学式是_________ ,其中右侧交换膜的作用是______ ,写出 d极的电极反应___________ 。
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是____ mol。

(1)锂离子电池工作时,a极发生
(2)电解池中物质A的化学式是
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是
您最近一年使用:0次



