解题方法
1 . 周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: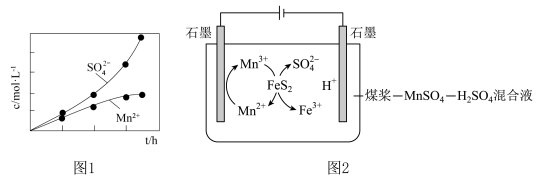
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
您最近一年使用:0次
名校
解题方法
2 . 我国应对气候变化工作成效显著,北京冬奥会是首个实现“碳中和”的世界级体育盛会,我国承诺2030年前实现“碳达峰”,2060年前实现“碳中和”。如何高效利用 是重要的研究课题。
是重要的研究课题。
I.光合作用
(1)植物光合作用中能量的转化形式为_____ 。
(2)“人工树叶”电化学装置如图1所示(以稀硫酸为电解质溶液),该装置能将CO2和H2O转化为糖类(用C6H12O6表示)和O2。
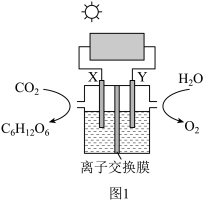
①Y为_____ 极,该极上发生的电极反应式为_____ 。
②室温下,该装置工作一段时间后,电解质溶液的pH_____ (填“升高”“降低”或“不变”)。
Ⅱ.电化学方法可将CO2有效地转化为CH3COOH,装置如图2所示
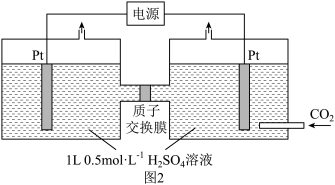
(3)阴极电极反应式为_____ ;电解时,H+通过质子交换膜向_____ 移动(填“左”或“右”)。
 是重要的研究课题。
是重要的研究课题。I.光合作用

(1)植物光合作用中能量的转化形式为
(2)“人工树叶”电化学装置如图1所示(以稀硫酸为电解质溶液),该装置能将CO2和H2O转化为糖类(用C6H12O6表示)和O2。

①Y为
②室温下,该装置工作一段时间后,电解质溶液的pH
Ⅱ.电化学方法可将CO2有效地转化为CH3COOH,装置如图2所示

(3)阴极电极反应式为
您最近一年使用:0次
解题方法
3 . 己二腈 是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(
是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈( ),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为:
),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为: 。模拟工业电合成己二腈的装置如图所示。
。模拟工业电合成己二腈的装置如图所示。

回答下列问题:
(1)阳极的电极反应式:___________ 。
(2)离子交换膜是___________ (填“阳离子”或“阴离子”)交换膜。
(3)丙烯腈在阴极转化为己二腈分三步:请用离子方程式表述相关过程。
第一步:___________ 。
第二步:
第三步:___________ 。
 是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(
是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈( ),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为:
),再用丙烯腈电合成己二腈(已知丙烯腈难溶于水,易溶于有机溶剂),总反应式为: 。模拟工业电合成己二腈的装置如图所示。
。模拟工业电合成己二腈的装置如图所示。
回答下列问题:
(1)阳极的电极反应式:
(2)离子交换膜是
(3)丙烯腈在阴极转化为己二腈分三步:请用离子方程式表述相关过程。
第一步:
第二步:

第三步:
您最近一年使用:0次
名校
4 . 镍氢电池广泛用于油电一体的混合动力汽车,该电池材料的回收利用也成为研究热点。
Ⅰ.某品牌镍氢电池的总反应为 ,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
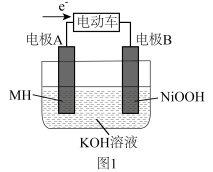
(1)混合动力车上坡时利用电池放电提供能源。
①电极A是_______ (填“正极”或“负极”)。
②正极的电极反应式为_______ 。
(2)混合动力车下坡时利用动能回收给电池充电,此时电极A附近的pH_______ (填“变大”“不变”或“变小”)
Ⅱ.该品牌废旧镍氢电池回收过程中,金属镍的转化过程如下:

转化过程中所用 和NaOH溶液通过电解
和NaOH溶液通过电解 溶液获得,装置如图2。
溶液获得,装置如图2。
已知:阴离子交换膜可选择性透过阴离子,阳离子交换膜可选择性透过阳离子。

(3)图2中,电极C为电解池的_______ (填“阴极”或“阳极”)。
(4)产生 的是
的是_______ (填“甲池”“乙池”或“丙池”),结合化学用语说明产生 的原理:
的原理:_______ 。
(5)回收该品牌废旧镍氢电池过程中,在阴极收集到气体134.4L(标准状况下),理论上最多可回收得到 (摩尔质量为
(摩尔质量为 )的质量为
)的质量为_______ 。
Ⅰ.某品牌镍氢电池的总反应为
 ,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
,其中,MH为吸附了氢原子的储氢合金。图1为该电池放电时的工作原理示意图。
(1)混合动力车上坡时利用电池放电提供能源。
①电极A是
②正极的电极反应式为
(2)混合动力车下坡时利用动能回收给电池充电,此时电极A附近的pH
Ⅱ.该品牌废旧镍氢电池回收过程中,金属镍的转化过程如下:

转化过程中所用
 和NaOH溶液通过电解
和NaOH溶液通过电解 溶液获得,装置如图2。
溶液获得,装置如图2。已知:阴离子交换膜可选择性透过阴离子,阳离子交换膜可选择性透过阳离子。

(3)图2中,电极C为电解池的
(4)产生
 的是
的是 的原理:
的原理:(5)回收该品牌废旧镍氢电池过程中,在阴极收集到气体134.4L(标准状况下),理论上最多可回收得到
 (摩尔质量为
(摩尔质量为 )的质量为
)的质量为
您最近一年使用:0次
2023-01-06更新
|
793次组卷
|
7卷引用:浙江省杭州师范大学附属中学2023-2024学年高二上学期期末考试化学试题
22-23高二上·浙江·期末
解题方法
5 . 甲烷燃料电池采用铂作为电极材料,两个电极上分别通入CH4和O2, 电解质溶液为KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验,如下图所示。

回答下列问题。
(1)甲烷燃料电池工作时,其负极电极反应为_______ 。
(2)闭合开关K后,a、b电极上均有气体产生,写出b电极反应式_______ 。
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为_______ L(标准状况)。 (写出必要过程)

回答下列问题。
(1)甲烷燃料电池工作时,其负极电极反应为
(2)闭合开关K后,a、b电极上均有气体产生,写出b电极反应式
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上最多能产生氯气的体积为
您最近一年使用:0次
6 . 按图所示装置进行实验(C1、C2为石墨棒),并回答下列问题:
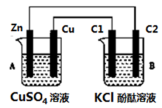
(1)判断装置的名称:A池为___________ ,B池为___________ 。
(2)锌极为___________ 极,电极反应式为___________ ;石墨棒C1为___________ 极,电极反应式为___________ ;
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为___________ 克。

(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出标况下224 mL气体时,锌的质量变化值为
您最近一年使用:0次
解题方法
7 . 电化学降解治理水中硝酸盐的污染,在酸性条件下,电解的原理如图所示
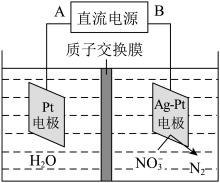
(1)A极为________ 极;
(2)阴极电极反应式为_________________ 。

(1)A极为
(2)阴极电极反应式为
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
8 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
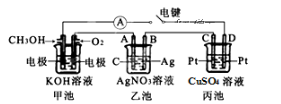
(1)丙池为________ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式为____________________ 。
(2)乙池中A电极为________ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为_________________________ 。
(3)当乙池中B极质量增重10.8g时,甲池中理论上消耗 的体积为
的体积为________ mL(标准状况)。
(4)丙池中,C上的电极反应式为____________________ 。如果起始时盛有1000mL  的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为________ 。

(1)丙池为
(2)乙池中A电极为
(3)当乙池中B极质量增重10.8g时,甲池中理论上消耗
 的体积为
的体积为(4)丙池中,C上的电极反应式为
 的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
足量),一段时间后,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入4g氧化铜,则加入氧化铜之前溶液的pH变为
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
9 . 完成下列填空
(1)纯水中存在电离平衡: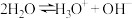 。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式
。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式______ 。
(2)金属钠可以从水中置换氢。在铁作催化剂时,金属钠也可以和液氨反应产生氢气和一种离子化合物X,写出化合物X的电子________ 。
(3)已知25℃时, 的燃烧热为1366
的燃烧热为1366 ,写出其燃烧热的热化学方程式:
,写出其燃烧热的热化学方程式:_______ 。
(4)硫化氢是一种气态废弃物,可电解 和
和 混合溶液后通入
混合溶液后通入 气体,
气体, 转化为可利用的硫过程为
转化为可利用的硫过程为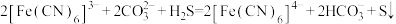 。请写出电解时阴极的电极反应式:
。请写出电解时阴极的电极反应式:___________ 。
(5)苯酚钠水溶液中通入少量 的化学方程式
的化学方程式________ 。
(6)有机物分子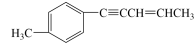 中最多有
中最多有________ 原子在一条直线上;
(7)3,3-二甲基-2-溴丁烷在 乙醇溶液中共热发生的反应方程式:
乙醇溶液中共热发生的反应方程式:____________ 。
(1)纯水中存在电离平衡:
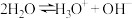 。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式
。像水一样,纯液氨中也存在着微弱的电离作用,请写出液氨的电离方程式(2)金属钠可以从水中置换氢。在铁作催化剂时,金属钠也可以和液氨反应产生氢气和一种离子化合物X,写出化合物X的电子
(3)已知25℃时,
 的燃烧热为1366
的燃烧热为1366 ,写出其燃烧热的热化学方程式:
,写出其燃烧热的热化学方程式:(4)硫化氢是一种气态废弃物,可电解
 和
和 混合溶液后通入
混合溶液后通入 气体,
气体, 转化为可利用的硫过程为
转化为可利用的硫过程为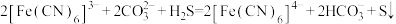 。请写出电解时阴极的电极反应式:
。请写出电解时阴极的电极反应式:(5)苯酚钠水溶液中通入少量
 的化学方程式
的化学方程式(6)有机物分子
 中最多有
中最多有(7)3,3-二甲基-2-溴丁烷在
 乙醇溶液中共热发生的反应方程式:
乙醇溶液中共热发生的反应方程式:
您最近一年使用:0次
18-19高二上·浙江·期末
名校
10 . 工业上可以通过电解NO制备NH4NO3,原理如图所示。写出电解过程阳极的电极反应式_________________________________________________ 。


您最近一年使用:0次



