解题方法
1 . 电解法测定铜的相对原子质量的装置如图所示,调节电阻使电流稳定在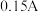 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:

电解前:铜a与铜b的质量分别 和
和 :
:
电解后:铜a与铜b的质量分别 和
和 。
。
已知: 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。
则测得的铜元素的相对原子质量为___________ (计算结果保留3位有效数字),写出简要计算过程___________ 。
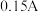 ,通电电解
,通电电解 。取下铜片,水洗、醇洗后晾干,精确称量如下:
。取下铜片,水洗、醇洗后晾干,精确称量如下:
电解前:铜a与铜b的质量分别
 和
和 :
:电解后:铜a与铜b的质量分别
 和
和 。
。已知:
 电子的电量为
电子的电量为 ,电路中通过的总电量
,电路中通过的总电量 (t单位为秒)。
(t单位为秒)。则测得的铜元素的相对原子质量为
您最近一年使用:0次
2020高三·全国·专题练习
2 . KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。KIO3也可采用“电解法”制备,装置如图所示。回答下列问题:

①写出电解时阴极的电极反应式______ 。
②电解过程中通过阳离子交换膜的离子主要为_________ ,其迁移方向是_____________ 。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
您最近一年使用:0次
填空题
|
适中(0.65)
|
名校
3 . 氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_______________ 。
(2)氨是制备氮肥、硝酸等的重要原料②③
①已知:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式________________ 。
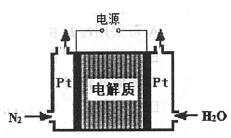
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式__________ 。
(3)反应:2NO(g)+O2(g) 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。
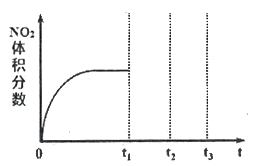
①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:____________ 。
②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g) N2O2(g) △H<0
N2O2(g) △H<0
II N2O2(g)+O2(g) 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因________ 。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=________________ 。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式
(2)氨是制备氮肥、硝酸等的重要原料②③
①已知:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/molN2(g)+O2(g)
 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol2H2(g)+O2(g)
 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol试写出表示氨的标准燃烧热的热化学方程式
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式
(3)反应:2NO(g)+O2(g)
 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:
②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g)
 N2O2(g) △H<0
N2O2(g) △H<0II N2O2(g)+O2(g)
 2NO2(g) △H<0
2NO2(g) △H<0已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=
您最近一年使用:0次
2017-03-11更新
|
965次组卷
|
3卷引用:2017届浙江省稽阳联谊学校高三3月选考化学试卷
名校
解题方法
4 . 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。

(1)若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:__________________________________ 。
②若在标准状况下有2.24 L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为__ mol。
(2)某小组在右室装有10 L 0.2 mol·L−1硝酸溶液,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L−1硝酸溶液需量取____ mL、密度为1.4 g·mL−1、质量分数为63%的浓硝酸。
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28 L H2。计算原气体中NO和NO2的体积比___ (假设尾气不含氮氧化物,写出计算过程)。

(1)若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式:
②若在标准状况下有2.24 L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为
(2)某小组在右室装有10 L 0.2 mol·L−1硝酸溶液,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。
①实验前,配制10 L 0.2 mol·L−1硝酸溶液需量取
②电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中含3 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28 L H2。计算原气体中NO和NO2的体积比
您最近一年使用:0次
2016-12-09更新
|
352次组卷
|
6卷引用:考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点
(已下线)考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点2016届江苏省苏中三市高三第二次调研测试化学试卷2016届江苏省南通市高三下学期第三次教学调研化学试卷2015-2016学年江苏省扬州中学高二下期中化学试卷2015-2016学年河北省定州中学高二下期中化学试卷辽宁省 丹东市第二中学、大石桥第三高级中学2023-2024学年高二上学期期末化学模拟试卷
11-12高三·浙江宁波·阶段练习
解题方法
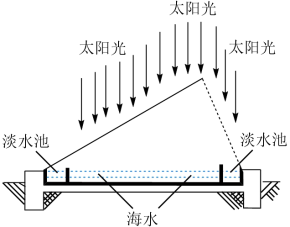
5 . 地球的海水总量约有1.4×1018t,是人类最大的资源库。
(1)如图利用海水得到淡水的方法为______ 。
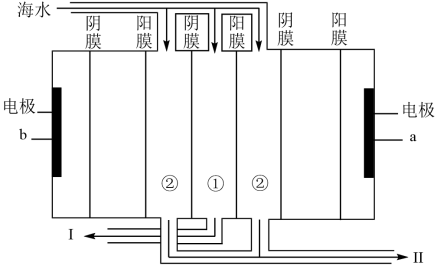
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图。a是电源的______ 极;Ⅰ口排出的是______ (填“淡水” 或“浓水”)。
(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、 Ca2+、Fe3+和SO ),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、 BaCl2、Na2CO3等),其中HCl的作用主要是
),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、 BaCl2、Na2CO3等),其中HCl的作用主要是______
(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为:______ (树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为:______ 。
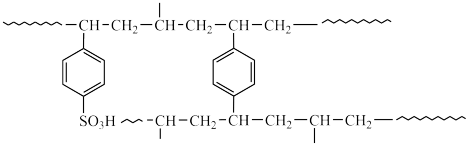
(5)离子交换树脂法是制备纯水(去离子水)的主要方法。某阳离子交换树酯的局部结构可写成(如图)。该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经______ 反应得到的。自来水与该离子交换树脂交换作用后显______ (填“酸性”、“碱性”或“中性”)。
(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大。如果硬度过大,饮用后对人体健康与日常生活有一定影响。暂时硬水的硬度是由______ (填阴离子符号)引起的,经______ (填操作名称)后可被去掉。永久硬水的硬度可由离子交换法去掉。
(1)如图利用海水得到淡水的方法为

(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图。a是电源的

(3)海水淡化后的浓水中含大量盐分(主要含有Mg2+、 Ca2+、Fe3+和SO
 ),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、 BaCl2、Na2CO3等),其中HCl的作用主要是
),排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。电解前需要把浓水精制,所需试剂主要包括:HCl、NaOH、 BaCl2、Na2CO3等),其中HCl的作用主要是(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在(以离子形式存在),每吨海水只含3.3毫克铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为:
(5)离子交换树脂法是制备纯水(去离子水)的主要方法。某阳离子交换树酯的局部结构可写成(如图)。该阳离子交换树脂是由单体苯乙烯和交联剂对二乙烯基苯聚合后再经

(6)中国《生活用水卫生标准》中规定,水的总硬度不能过大。如果硬度过大,饮用后对人体健康与日常生活有一定影响。暂时硬水的硬度是由
您最近一年使用:0次



