名校
1 . 卤族元素在性质上具有相似性与递变性。为了验证卤族部分元素递变规律,设计如图装置进行实验。请回答下列问题。
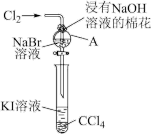
(1)A中发生反应的化学方程式是_______ 。
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为_______ 。
(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱_______ 。
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为_______ 。
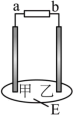
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是
(8)下图是用强光照射广口瓶中新制氯水时传感器所获得数据的图像,下列各项代表纵坐标的物理量,其中与图像不相符的是

(9)下列变化不需要破坏化学键的是

(1)A中发生反应的化学方程式是
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
| A.Cl-、Br-、I-的还原性逐渐增强 | B.Cl2、Br2、I2的熔点逐渐升高 |
| C.HCl、HBr、HI的酸性逐渐减弱 | D.HCl、HBr、HI的稳定性逐渐减弱 |
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应
 填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是

| A.b是阳极,a是阴极 | B.a是正极,b是负极 |
| C.乙是正极,甲是负极 | D.乙是阳极,甲是阴极 |

| A.溶液中氯离子的浓度 | B.溶液的 pH |
| C.瓶中氧气的体积分数 | D.溶液的导电能力 |
| A.液态水变为水蒸气 | B.HCl 气体溶于水 |
| C.NaHCO3 受热分解 | D.NaCl 熔化 |
您最近一年使用:0次
名校
2 . 某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。
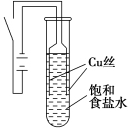
实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
*相同温度下CuCl的溶解度大于CuOH
下列说法错误的是

实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜(不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
下列说法错误的是
| A.反应结束后最终溶液呈碱性 |
| B.阴极上发生的电极反应为:2H2O + 2e-═ H2↑+ 2OH- |
| C.电解过程中氯离子移向阳极 |
| D.试管底部红色的固体具有还原性 |
您最近一年使用:0次
2015-05-13更新
|
1990次组卷
|
5卷引用:2016届贵州省贵阳六中高三上半期考试理综化学试卷
名校
3 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用石墨电极电解等浓度的足量FeCl3、CuCl2混合溶液 | 阴极有红色固体物质析出 | 金属活动性:Fe>Cu |
| B | 取适量NaHCO3固体于试管中,滴入少量水并用温度计检测 | 试管内温度上升,NaHCO3结块变为晶体 | NaHCO3溶于水放热 |
| C | 向AlCl3溶液中逐滴加入稀氨水至过量 | 产生白色沉淀,并逐渐增多,后慢慢溶解 | 碱性:NH3•H2O>Al(OH)3 |
| D | 向足量NaBr溶液中通入少量氯气,再加入淀粉KI溶液 | 溶液先变橙色,后变为蓝色 | 氧化性:Cl2>Br2>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-29更新
|
158次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
名校
解题方法
4 . 常用电解法处理工业废水中的乙醛。该过程中发生的电极反应为:
①4H2O+4e-=2H2↑+4OH-
②CH3CHO+3H2O-10e-=2CO2↑+10H+
③2H2O-4e-=O2↑+4H+
④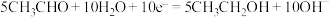
⑤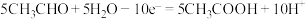
下列说法错误的是
①4H2O+4e-=2H2↑+4OH-
②CH3CHO+3H2O-10e-=2CO2↑+10H+
③2H2O-4e-=O2↑+4H+
④
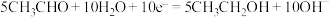
⑤
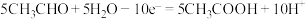
下列说法错误的是
| A.反应①⑤发生在阴极 |
| B.乙醛既体现氧化性又体现还原性 |
| C.当生成46g乙醇时,电路中转移2mol 电子 |
| D.电解过程中,电极附近溶液的pH: 阴极>阳极 |
您最近一年使用:0次
2021-03-18更新
|
619次组卷
|
4卷引用:山东省济南市第一中学2021-2022学年高二上学期期中考试化学试题
山东省济南市第一中学2021-2022学年高二上学期期中考试化学试题山东省青岛市2021届高三3月统一质量检测化学试题(已下线)小题17 新型电解池装置 ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)专题08 电化学及其应用-备战2022年高考化学真题及地市好题专项集训【山东专用】
解题方法
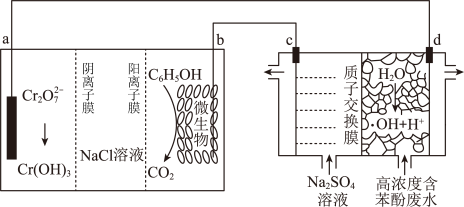
5 . 科学家设计了一种将苯酚( )氧化为
)氧化为 和
和 的原电池一电解池组合装置。装置如图所示,已知羟基自由基(
的原电池一电解池组合装置。装置如图所示,已知羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。下列说法正确的是
)是自然界中氧化性仅次于氟的氧化剂。下列说法正确的是
 )氧化为
)氧化为 和
和 的原电池一电解池组合装置。装置如图所示,已知羟基自由基(
的原电池一电解池组合装置。装置如图所示,已知羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。下列说法正确的是
)是自然界中氧化性仅次于氟的氧化剂。下列说法正确的是
| A.甲池为电解池,a电极为甲池的阴极 |
| B.高温下该装置也可以正常使用 |
C.电池工作时,NaCl溶液中 穿过阳离子交换膜移向b极区 穿过阳离子交换膜移向b极区 |
D.相同时间内,c、d两极产生气体的体积比(相同条件下)为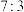 |
您最近一年使用:0次
真题
名校
6 . 氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正确 的是
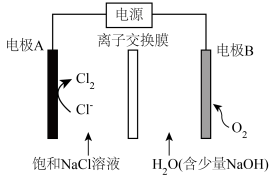
| A.电极A接电源正极,发生氧化反应 |
B.电极B的电极反应式为: |
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液 溶液 |
| D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗 |
您最近一年使用:0次
2023-06-21更新
|
10043次组卷
|
20卷引用:河北省迁安市2023-2024学年高三上学期期中考试化学试题
河北省迁安市2023-2024学年高三上学期期中考试化学试题广东省深圳市富源学校2023-2024学年高二上学期11月期中化学试题湖南省雅礼教育集团2023-2024学年高二下学期期中考试化学试题2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用(已下线)专题07 电化学及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第25讲电解池与金属的电化学腐蚀(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省广州市白云中学2023-2024学年高三上学期9月月考化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷河北省石家庄市河北正定中学2023-2024学年高二上学期第二次月考化学试题(已下线)专题08 电解池 金属的腐蚀与防护-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)2023-2024学年度第二学期高三化学零模试卷四川省遂宁市蓬溪中学校2023-2024学年高二下学期3月月考化学试题北京市师范大学附属实验中学2024届高三零模化学试题(已下线)FHgkyldyjhx12
名校
7 . 有关X、Y、Z、W四种金属的实验如下:
根据以上事实,下列判断或推测错误的是( )
| ① | 将X与Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| ② | 将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
| ③ | 用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出单质Z |
| A.Z的阳离子氧化性最强 |
| B.Z放入CuSO4溶液中一定有Cu析出 |
| C.W的还原性强于Y的还原性 |
| D.用Y、Z和稀硝酸可构成原电池,且Y作负极 |
您最近一年使用:0次
2019-06-01更新
|
270次组卷
|
4卷引用:安徽省滁州市明光中学2018-2019学年高一下学期期中考试化学试题
名校
解题方法
8 . 工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是
已知:①Ni2+在弱酸性溶液中发生水解;②氧化性:Ni2+ (高浓度)>H+> Ni2+(低浓度)
已知:①Ni2+在弱酸性溶液中发生水解;②氧化性:Ni2+ (高浓度)>H+> Ni2+(低浓度)
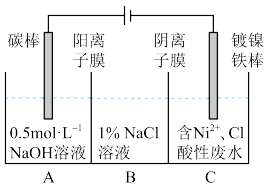
| A.碳棒上发生的电极反应:4OH- -4e- =O2↑+2H2O |
| B.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
| C.电解过程中,B室中NaCl溶液的物质的量浓度将不断减小 |
| D.为了提高Ni的产率,电解过程中需要控制废水pH |
您最近一年使用:0次
2022-11-10更新
|
995次组卷
|
67卷引用:2016-2017学年浙江省绍兴一中高二上期中化学试卷
2016-2017学年浙江省绍兴一中高二上期中化学试卷2016-2017学年四川省成都市第七中学高二下学期半期考试化学试卷【全国百强校】河北省石家庄市第一中学2018-2019学年高二上学期期中考试化学试题浙江省嘉兴市第一中学、湖州中学2019-2020学年高二上学期期中联考化学试题重庆一中2019-2020学年高二上学期期中考试化学试题重庆市沙坪坝区重庆市第七中学2020-2021高二上学期中考试化学试题四川省绵阳南山中学2021-2022学年高二下学期期中考试化学试题辽宁省实验中学2022-2023学年高二上学期期中阶段测试化学试题2015届浙江省台州中学高三上学期第三次统练考试理综试卷2015届浙江省台州中学高三上学期第三次统练理综化学试卷2015届福建省漳州市高三5月适应性考试化学试卷2015-2016学年山西省怀仁一中高二12月月考化学试卷2017届浙江省温州中学高三上10月高考模拟化学试卷2016-2017学年湖南省衡阳八中高二上月考五化学卷2016-2017学年湖北省华中师范大学第一附属中学高二上学期期末考试化学试卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷2017届江苏省泰州中学高三下学期期初考试化学试卷2016-2017学年湖南省衡阳市第八中学高一下学期理科实验班第一次月考理科综合化学试卷2017届重庆市万州区高三下学期“二诊”模拟考试化学试卷福建省三明市第一中学2016-2017学年高二下学期第二次月考化学试题辽宁省瓦房店市高级中学2017-2018学年高二上学期12月月考化学试题(已下线)黄金30题系列++高二化学(选修4)++++小题好拿分【基础版】山东省临沂市第十九中学2017-2018学年高二上学期第五次质量调研化学试题黑龙江省大庆第一中学2017-2018学年高二上学期期末(第四次月考)考试化学试题四川省什邡中学2017-2018学年高二春秋招班第三次月考化学试题(已下线)2018年9月23日 《每日一题》 一轮复习-每周一测高二人教版选修4 第四章 重难点专题练——原电池和电解池的综合应用甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题【全国百强校】河北省冀州市中学2018-2019学年高二上学期第六次月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二下学期第三次月考化学试题(已下线)2019年9月22日 《每日一题》 2020年高考一轮复习-每周一测河南省洛阳市第一高级中学2019-2020学年高二12月月考化学试题湖南省邵阳市邵东县创新实验学校2020届高三上学期第五次月考化学试题湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题17 带隔膜的电化学装置云南省曲靖二中2020届高三第一次月考理综化学试题(已下线)【南昌新东方】2018-2019莲塘一中 高三12月 014四川省成都市射洪县2018-2019学年高二下学期期末能力素质监测理综化学试题(英才班)鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第3节 电能转化为化学能——电解 课时2 电解原理的应用高中必刷题高二选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用(已下线)【浙江新东方】47人教版(2019)高二化学选择性必修1第四章 化学反应与电能 易错疑难集训(二)(已下线)第四章 检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)福建省福州市第四中学2021届高三上学期11月月考化学试题湖北省孝感市高级中学2020—2021学年高二下学期2月调研考试化学试题河北正定中学2020-2021学年高三第二次半月考化学试题河北省衡水市武强中学2022届高三上学期第一次月考化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点(已下线)期末综合测试卷01-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)第六单元 化学反应与能量(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)4.2.2 电解原理的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题30 电化学中的交换膜-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)辽宁省朝阳市建平县实验中学2021-2022学年高二上学期第三次月考化学试题江西省九江市第一中学2021-2022学年高二上学期第二次月考化学试题山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题江西省宜春市上高二中2021-2022学年高二下学期第四次月考试题(3月)化学试题云南省曲靖市罗平县第五中学2021-2022学年高二4月月考化学试题内蒙古喀喇沁旗锦山蒙古族中学2021-2022学年高二下学期开学考试化学试题河南省洛阳市宜阳县第一高级中学2022-2023学年高二上学期第五次能力达标测试化学试题吉林省四平市第一高级中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题08 新型化学电源(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)安徽省安庆市第七中学2021-2022学年高二下学期3月阶段性考试化学试题(已下线)选择题11-16陕西省西安市2023-2024学年高二上学期期末化学测试卷B河北省石家庄二中润德2023-2024学年高二上学期12月月考化学试题宁夏吴忠中学2023-2024学年高二上学期期末考试化学试题广东省汕头市金山中学2023-2024学年高二上学期期末考试 化学试题四川省什邡中学2023-2024学年高二下学期4月第一次月考化学试题
名校
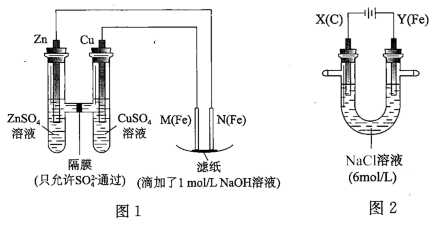
9 . 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__ (填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__ 。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__ (填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____ g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__ 。

请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
2019-06-28更新
|
411次组卷
|
21卷引用:云南省玉溪市江川区第二中学2020-2021学年高二下学期期中考试化学试题
云南省玉溪市江川区第二中学2020-2021学年高二下学期期中考试化学试题吉林省扶余市第一中学2017-2018学年高一下学期期末考试化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第四单元 电化学基础单元测试A卷云南省广南二中2018-2019学年高二6月考试化学试题云南省屏边县民族中学2019-2020学年高二上学期12月月考化学试题云南省河口县第一中学2019-2020学年高二上学期12月月考化学试题云南省镇康县第一中学2019-2020学年高二12月月考化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题2云南省迪庆州香格里拉中学2019-2020学年高二上学期期末考试化学试题云南省武定民族中学2019-2020学年高二上学期期末考试化学试题云南省普洱市镇沅县第一中学2019—2020学年高二上学期期末考试化学试题云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题云南省普洱市普洱第二中学2019—2020学年高二上学期期末考试化学试题贵州省三都水族自治县高级中学2019-2020学年高二上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题贵州省三穗县三中2019-2020学年高二上学期期末考试化学试题云南省曲靖市沾益县第二中学2019-2020学年高二上学期期末考试化学试题云南省昆明市寻甸县第三中学2019-2020学年高二上学期期末考试化学黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二上学期开学考试化学试题安徽省怀宁中学2020-2021学年高二上学期第二次质量检测(普通班)化学试题云南省玉龙县第一中学2021-2022学年高二下学期3月份考试化学试题
名校
10 . 科学家设计了一种可以循环利用人体呼出的CO2并提供O2的装置,总反应方程式为2CO2=2CO+O2。下列说法正确的是( )
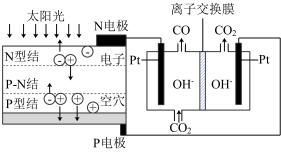

| A.由图分析N电极为电池的正极 |
| B.阴极的电极反应为CO2+H2O+2e-=CO+2OH- |
| C.OH-通过离子交换膜迁向左室 |
| D.反应完毕,该装置中电解质溶液的碱性增强 |
您最近一年使用:0次
2019-03-28更新
|
669次组卷
|
6卷引用:广东省佛山市第一中学2020届高三上学期期中考试理综化学试题



