解题方法
1 . 工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是行之有效的除去铬的方法之一。该法用Fe和石墨作电极电解含Cr2O 的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
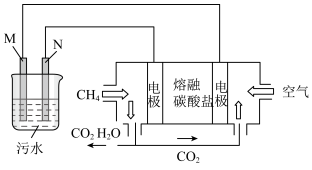
(1)Fe电极为_________ (填“M”或“N”);电解时_______ (填“能”或“不能”)否用Cu电极来代替Fe电极,理由是________________________________________________ 。
(2)阳极附近溶液中,发生反应的离子方程式是________________ ,阴极附近的沉淀有______ 。
(3)图中熔融盐燃料电池是以熔融碳酸盐为电解质、CH4为燃料、空气为氧化剂、稀土金属材料为电极的新型电池。已知,该熔融盐电池的负极的电极反应是CH4–8e–+4CO32–=5CO2+2H2O,则正极的电极反应式为__________________ 。
(4)实验过程中,若电解池阴极材料质量不变,产生4.48L(标准状况)气体时,熔融盐燃料电池消耗CH4的体积为____________________ L(标准状况)。
 的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的。某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如下图所示。
(1)Fe电极为
(2)阳极附近溶液中,发生反应的离子方程式是
(3)图中熔融盐燃料电池是以熔融碳酸盐为电解质、CH4为燃料、空气为氧化剂、稀土金属材料为电极的新型电池。已知,该熔融盐电池的负极的电极反应是CH4–8e–+4CO32–=5CO2+2H2O,则正极的电极反应式为
(4)实验过程中,若电解池阴极材料质量不变,产生4.48L(标准状况)气体时,熔融盐燃料电池消耗CH4的体积为
您最近半年使用:0次
2016-12-09更新
|
444次组卷
|
2卷引用:2014-2015河南省陕州中学高二下学期第二次精英对抗赛化学试卷
名校
2 . 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是


| A.电池工作时,正极反应式为: O2+2H2O+4e-===4OH- |
| B.电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 |
| C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D.忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2 |
您最近半年使用:0次
2016-12-09更新
|
763次组卷
|
13卷引用:河南省南阳市第一中学校2021届高三上期第五次考试化学试题
河南省南阳市第一中学校2021届高三上期第五次考试化学试题(已下线)2011届山东省济南外国语学校高三上学期第三次质量检测化学试卷(已下线)2011届江西省南昌市高三第三次模拟测试理综化学部分2014-2015吉林省延边二中高二12月阶段考试化学试卷山东省德州市夏津第一中学2019-2020学年高二上学期第一次月考化学试题云南省曲靖市罗平县第三中学2019-2020学年高二上学期期末考试化学试题山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题山东省莱芜一中2021届高三第一次考试化学试题湖南省长沙市周南中学2020-2021学年高二下学期入学考试化学试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题吉林省长春市第六中学2021-2022学年高二上学期第三学程考试(理)化学试题山西省太原师范学院附属中学2022-2023学年高二上学期12月月考化学试题山东省临沂第一中学2020-2021学年高三上学期第一次检测化学试题
名校
解题方法
3 . 如图所示装置中,a、b、c、d、e、f均为惰性电极,电解质溶液均足量。接通电源后,d极附近显红色。下列说法正确的是
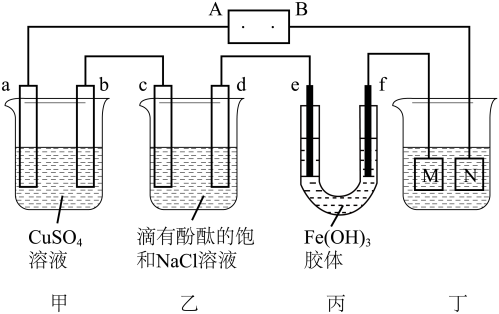

| A.电源B端是正极 |
| B.a、c电极均有单质生成,它们的物质的量之比为2∶1 |
| C.欲用丁装置给铜镀银,N应为Ag,电解质溶液为 AgNO3溶液 |
| D.f极附近变红,说明氢氧化铁胶粒带正电荷 |
您最近半年使用:0次
2016-12-09更新
|
657次组卷
|
4卷引用:河南省安阳市第一中学2023届高三第四次全真模拟化学试题
河南省安阳市第一中学2023届高三第四次全真模拟化学试题(已下线)2013届河北省石家庄市高中毕业班第二次模拟考试理综化学试卷(已下线)2014高考名师推荐化学--预测10陕西省西安市长安区第一中学2017-2018学年高二上学期期末考试化学(理)试题
解题方法
4 . 某兴趣小组利用如图所示装置进行实验。
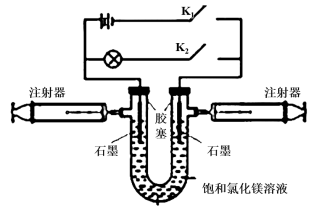
(1)断开K2、闭合K1,U形管内除电极上有气泡外,还可观察到的现象是_____ ;阳极电极反应式为________________ 。当电路中转移0.001mol电子时,右侧注射器最多可以收集到气体_______ mL(折算为标准状况)。
(2)断开K2、闭合K1一段时间,待注射器中充有一定量的气体后,断开K1、闭合K2,此时装置内化学能转化为电能。实现能量转化的化学方程式为_______________ ;
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上_______ (填“能”或“不能”)恢复原样。

(1)断开K2、闭合K1,U形管内除电极上有气泡外,还可观察到的现象是
(2)断开K2、闭合K1一段时间,待注射器中充有一定量的气体后,断开K1、闭合K2,此时装置内化学能转化为电能。实现能量转化的化学方程式为
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上
您最近半年使用:0次
2013·河南·一模
5 . 如图甲、乙是电化学实验装置。有关电极反应或计算错误的是:
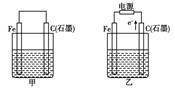

| A.若甲烧杯中盛有NaCl溶液,则石墨棒上的电极反应式为:O2+2H2O+4e-= 4OH- |
| B.若乙烧杯中盛有NaCl溶液,则乙中的总反应为:2Cl-+2H2O=2OH-+H2↑+Cl2↑ |
| C.若甲烧杯中盛有CuSO4溶液,则甲中铁棒上的电极反应式为:Fe-2e-=Fe2+ |
| D.若起始时乙中盛有200 mL pH=5的CuSO4溶液,一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入0.6 g CuO |
您最近半年使用:0次
名校
6 . 假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。下列说法错误的是
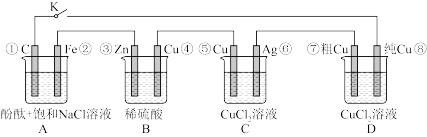

| A.当K闭合时,A装置发生吸氧腐蚀,在电路中做电源 |
| B.当K断开时,B装置锌片溶解,有氢气产生 |
| C.当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→② |
| D.当K闭合后,A、B装置中pH变大,C、D装置中pH不变 |
您最近半年使用:0次
2016-12-09更新
|
621次组卷
|
8卷引用:河南省信阳高级中学2023-2024学年高二上学期9月月考化学试题
河南省信阳高级中学2023-2024学年高二上学期9月月考化学试题(已下线)2014届浙江省杭州市七校高三上学期期中联考化学试卷辽宁省本溪市第一中学2017-2018学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第三中学2018届高三上学期第一次验收考试化学试题浙江省杭州市七校2017届高三下学期期中联考化学试题(已下线)2018年9月22日 《每日一题》 一轮复习-周末培优辽宁省丹东市2017-2018学年高二上学期期末质量监测化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期期末考试化学试题
名校
解题方法
7 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业的原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
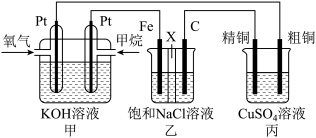
(1)甲烷燃料电池负极反应式为________________________ 。
(2)石墨(C)极的电极反应式为_______________________ 。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体的体积为________ L;丙装置中阴极析出铜的质量为________ g。
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。
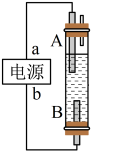
若用于制漂白液,a为电池的________ 极,电解质溶液最好用)________________
若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用________ 作电极。

(1)甲烷燃料电池负极反应式为
(2)石墨(C)极的电极反应式为
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体的体积为
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。

若用于制漂白液,a为电池的
若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用
您最近半年使用:0次
2016-12-09更新
|
933次组卷
|
9卷引用:河南省开封市五县2021-2022学年高二上学期期末考试化学试题
河南省开封市五县2021-2022学年高二上学期期末考试化学试题(已下线)2013届湖北省荆州市高三毕业班质量检查(Ⅰ)化学试卷(已下线)2014届高考化学二轮冲刺非选择题增分专练 基本概念、基本理论练习卷(已下线)2013-2014浙江省温州中学高一下学期期中化学试卷(已下线)二轮复习 专题10 电化学及其应用 押题专练(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(押题专练)河北省大名县第一中学2019-2020学年高二9月月考化学试题河北省邯郸大名一中2019-2020学年高二上学期第一次月考化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期期中考试化学试题
名校
8 . 某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)______________________________ 。设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过__________ mol电子。
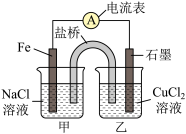
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为____________________ ,这是由于NH4Cl溶液显_______ (填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因________________________ ,用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式______________________ ,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为 ,试写出该反应的离子方程式
,试写出该反应的离子方程式____________________________________ 。
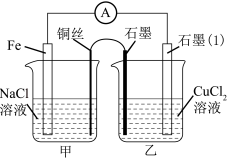
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是________________ ,电极反应为___________________ ;乙装置中石墨(1)为________ 极(填“正”“负”“阴”或“阳”),乙装置中与铜丝相连石墨电极上发生的反应式为___________ ,产物常用______________ 检验,反应的离子方程式为__________________ 。
。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示)

(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为
 ,试写出该反应的离子方程式
,试写出该反应的离子方程式(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是
。

您最近半年使用:0次
2016-12-09更新
|
887次组卷
|
8卷引用:河南省郑州市宇华实验学校2023-2024学年高三上学期开学(摸底)考试化学试题
河南省郑州市宇华实验学校2023-2024学年高三上学期开学(摸底)考试化学试题(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题六课时跟踪训练--原电池 化学电源山西省朔州市应县第一中学2017-2018学年高二上学期月考(四)化学试题(已下线)解密09 电化学(教师版)——备战2018年高考化学之高频考点解密(已下线)2018年9月16日 《每日一题》一轮复习- 每周一测(已下线)2019年9月15日 《每日一题》2020年一轮复习 —— 每周一测吉林省长春外国语学校2021-2022学年高三上学期期中考试化学试题
9 . 市场上经常见锂离子电池,它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为:
Li + 2Li0.35NiO2 2Li0.85NiO2。下列说法不正确的是
2Li0.85NiO2。下列说法不正确的是
Li + 2Li0.35NiO2
 2Li0.85NiO2。下列说法不正确的是
2Li0.85NiO2。下列说法不正确的是 | A.放电时,负极的电极反应式:Li — e-= Li+ |
| B.该电池不能用水溶液作为电解质 |
| C.充电时,Li0.5NiO2既发生氧化反应又发生还原反应 |
| D.放电过程中Li+向负极移动 |
您最近半年使用:0次
2016-12-09更新
|
298次组卷
|
16卷引用:2015-2016学年河南省安阳三十六中高二上学期期中考试化学试卷
2015-2016学年河南省安阳三十六中高二上学期期中考试化学试卷2009年普通高等学校招生统一考试理综试题化学部分(浙江卷)2009高考真题汇编-碱金属元素及其化合物(已下线)2010年天津一中高二下学期期中考试化学试题(已下线)2010—2011学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2014届海南省琼海市嘉积中学高三上学期教学质量监测化学试卷2016届黑龙江省哈尔滨师大附属中学高三上12月月考化学试卷2016-2017学年吉林省长春实验中学高二上9月月考化学卷(已下线)同步君 选修4 第4章 第2节 化学电源高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源2020年安徽省全省教学质量检测统一考试(练习检测一)四川省南充市白塔中学2019-2020学年高二下学期开学考试化学试题(已下线)【南昌新东方】江西省九江第一中学2018-2019学年高二上学期第二次月考化学试题福建省仙游县第二中学2022-2023学年高二上学期期中考试(选考班)化学试题
2009·宁夏·高考真题
真题
名校
10 . 请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______ (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________ (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
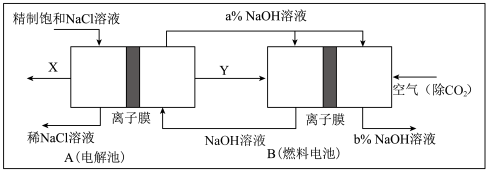
①图中X、Y分别是_____ 、_______ (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________ ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______ ;负极:_____ ;
③这样设计的主要节(电)能之处在于(写出2处)____________ 、____________ 。
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是
②分别写出燃料电池B中正极、负极上发生的电极反应正极:
③这样设计的主要节(电)能之处在于(写出2处)
您最近半年使用:0次
2016-12-09更新
|
192次组卷
|
7卷引用:2011-2012学年河南省平顶山市高一上学期期末调研考试化学试卷
(已下线)2011-2012学年河南省平顶山市高一上学期期末调研考试化学试卷2009年普通高等学校招生统一考试理综试题化学部分(宁夏卷)2009年高考真题汇编-卤 素(已下线)2010年陕西省五校高三第一次模拟考试理综化学试题2016-2017学年江苏省如东高级中学高一下学期第一次(3月)阶段检测化学试卷2020年安徽省全省教学质量检测统一考试(练习检测一)云南省普洱市景东彝族自治县第一中学2019-2020学年高二下学期期中考试理综化学试题



