名校
1 . 科学家设计了一种具有石墨正极的高容量可充电 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
 电池,原理如图所示。氯化铝(
电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(LiFSI)为溶剂。下列叙述正确的是
)中,以氟化物(LiFSI)为溶剂。下列叙述正确的是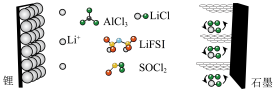
A.放电时,电解质溶液可以是 水溶液 水溶液 |
B.放电时,石墨极的电极反应式为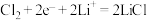 |
| C.充电时,石墨极与电源负极连接 |
D.充电时,转移 个电子时锂电极理论上消耗14g锂 个电子时锂电极理论上消耗14g锂 |
您最近一年使用:0次
2024-02-25更新
|
195次组卷
|
6卷引用:湖南省张家界市2023-2024学年高三上学期期末联考化学试题
名校
解题方法
2 . 双盐 电池由
电池由 替代了
替代了 在正极材料中的嵌入,解决了
在正极材料中的嵌入,解决了 扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
 电池由
电池由 替代了
替代了 在正极材料中的嵌入,解决了
在正极材料中的嵌入,解决了 扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是
扩散缓慢、锂离子电池锂枝晶生长等问题,其充、放电过程如图所示。下列说法正确的是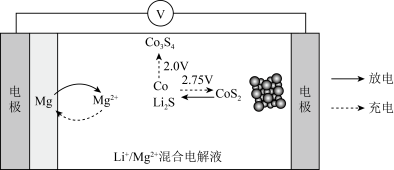
A.放电时, 电极的电势高于 电极的电势高于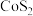 电极 电极 |
| B.充电时,若充电电压为2.0V,可能造成电池性能衰减 |
C.放电时,每转移2  ,正极质量减少14g ,正极质量减少14g |
D.充电时,充电电压为2.75V时,负极区的反应为: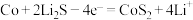 |
您最近一年使用:0次
2024-02-17更新
|
802次组卷
|
4卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
名校
解题方法
3 . 科研人员新研发了一种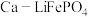 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为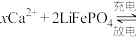
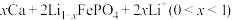 。下列说法不正确的是
。下列说法不正确的是
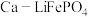 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为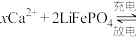
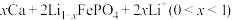 。下列说法不正确的是
。下列说法不正确的是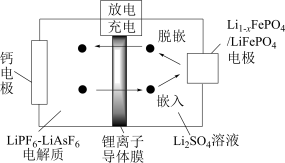
A.当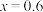 时, 时, 中的 中的 和 和 个数之比为2:3 个数之比为2:3 |
B.放电时,正极反应为 |
C.充电时,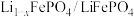 电极发生 电极发生 脱嵌, 脱嵌, 从右室移向左室 从右室移向左室 |
| D.充电时,理论上左室电解质的质量减轻4g,电路中有0.2mol电子转移 |
您最近一年使用:0次
2024-01-21更新
|
229次组卷
|
4卷引用:湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷
解题方法
4 . 我国研究人员采用双极膜将酸性、碱性电解液隔离,实现了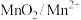 和
和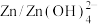 的两个溶解/沉积反应,研制出了新型高比能液流电池,其放电过程原理如图所示。下列说法正确的是
的两个溶解/沉积反应,研制出了新型高比能液流电池,其放电过程原理如图所示。下列说法正确的是
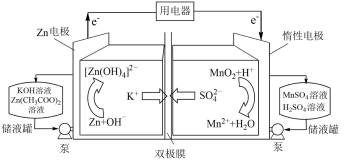
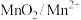 和
和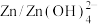 的两个溶解/沉积反应,研制出了新型高比能液流电池,其放电过程原理如图所示。下列说法正确的是
的两个溶解/沉积反应,研制出了新型高比能液流电池,其放电过程原理如图所示。下列说法正确的是
A.放电过程的正极电极反应式为 |
B.放电过程中,当1mol Zn参与反应时,理论上有4mol  发生迁移 发生迁移 |
C.充电过程中,阴极的电极反应式为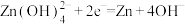 |
| D.充电过程中,右侧池中溶液pH逐渐增大 |
您最近一年使用:0次
名校
解题方法
5 . 近期,清华大学段吴泓副教授课题组首次利用糠醛创制了一种如图a所示的新型可充放电的“生物质电池”,该电池在充放电过程中可生产高附加值化学品糠醇和糠酸,其原理可用图b表示。下列说法正确的是

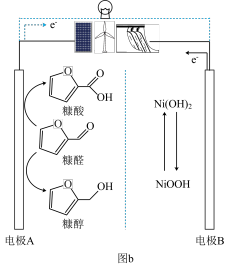


| A.该装置在生成糠醇时将化学能转化为电能 |
| B.放电时电极A发生还原反应 |
| C.充电时电极B附近碱性增强 |
D.若使用铅蓄电池为其充电,当 糠醛转化时, 糠醛转化时, 电极增重64g 电极增重64g |
您最近一年使用:0次
2024-01-07更新
|
513次组卷
|
3卷引用:2024届湖南省湘东九校联盟高三上学期第一次联考化学试题
名校
解题方法
6 . 羟基自由基( )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是

 )是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为
)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 和
和 的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
的原电池—电解池的组合装置,实现了发电、环保两位一体。下列说法错误的是
A.a极每 参与反应,有 参与反应,有 移向氯化钠溶液 移向氯化钠溶液 |
| B.相同条件下,电极b与c产生气体的体积比为7:3 |
| C.电极c为阴极,发生还原反应 |
D.d极区苯酚被氧化的化学方程式为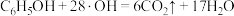 |
您最近一年使用:0次
解题方法
7 . 传统方法制备的氧化铝中往往含有氧化钠,氧化钠含量的高低直接影响氧化铝制品的抗压强度及电绝缘性,一种电渗析法生产低钠氧化铝的装置如图所示,将偏铝酸钠溶液加入阴极室,不含钠离子的缓冲液加入阳极室,最终在阳极室得到产品。下列说法正确的是
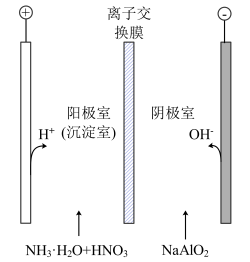

| A.氧化铝常用于制造耐高温材料,实验室可用氧化铝坩埚熔化NaOH |
| B.氧化钠、氧化铝都属于碱性氧化物 |
| C.中间的离子交换膜为阳离子交换膜 |
| D.理论上,阴极每产生2.24L气体(标准状况),阳极可得到10.2g氧化铝 |
您最近一年使用:0次
解题方法
8 . 某小组探究电解氯化铜的产物,设计如下实验(以石墨为电极):
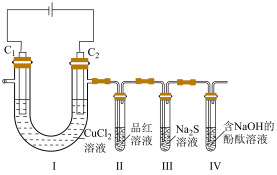
实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是

实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是
| A.根据Ⅲ试管中现象可知,氯的非金属性比硫强 |
B.一段时间后, 极附着一层红色固体物质 极附着一层红色固体物质 |
| C.上述实验中,试管Ⅱ和Ⅳ褪色原理不相同 |
| D.如果用铜极替代石墨也能得到与上述实验完全相同的实验现象 |
您最近一年使用:0次
2023-10-08更新
|
87次组卷
|
2卷引用:湖南省名校联考联合体2023-2024学年高三上学期第二次联考化学试题
名校
解题方法
9 . 2019年诺贝尔化学奖花落锂离子电池,美英日三名科学家获奖,他们创造了一个可充电的世界。像高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。
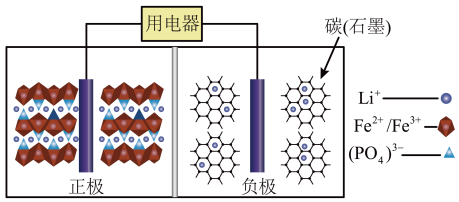
原理如下:(1-x)LiFePO4+xFePO4+LixCn LiFePO4+nC。下列说法不正确的是
LiFePO4+nC。下列说法不正确的是

原理如下:(1-x)LiFePO4+xFePO4+LixCn
 LiFePO4+nC。下列说法不正确的是
LiFePO4+nC。下列说法不正确的是| A.放电时,电子由负极经导线、用电器、导线到正极 |
| B.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4 |
| C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn |
| D.充电时,Li+向右移动,为了提高放电效率可用氯化锂溶液代替中间聚合物 |
您最近一年使用:0次
2023-10-03更新
|
477次组卷
|
3卷引用:湖南省邵东市第一中学2023-2024学年高三上学期第四次月考化学试题
名校
解题方法
10 .  是生产多晶硅的副产物.利用
是生产多晶硅的副产物.利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
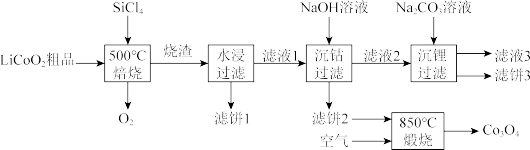
Ⅰ.回答下列问题:
(1) 价层电子排布式为
价层电子排布式为______ 。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因______ 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是
常用方法的名称是______ 。
(4)已知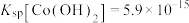 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为______  。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为______ 。
(5)导致 比
比 易水解的因素有
易水解的因素有______ (填标号).
a.Si-Cl键极性更大 b.Si的原子半径更大 c.Si-Cl键键能更大 d.Si有更多的价层轨道
Ⅱ.设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。
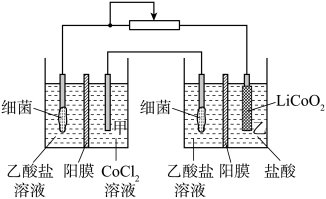
(6)装置工作时,甲室溶液pH逐渐______ ,乙室电极反应式为:______ 。
 是生产多晶硅的副产物.利用
是生产多晶硅的副产物.利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
Ⅰ.回答下列问题:
(1)
 价层电子排布式为
价层电子排布式为(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
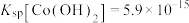 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大 c.Si-Cl键键能更大 d.Si有更多的价层轨道
Ⅱ.设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成
 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。
(6)装置工作时,甲室溶液pH逐渐
您最近一年使用:0次



