名校
解题方法
1 . 如图甲是利用一种微生物将化学能直接转化为电能的装置,图乙是利用微生物电池在铁上镀铜的装置,下列说法中正确的是( )
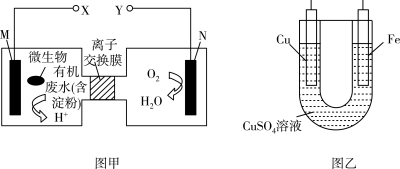

| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
| C.M极的电极反应式:(C6H10O5)n+7nH2O-24ne-=6nCO2↑+24nH+ |
| D.当N电极消耗0.25mol气体时,则铁电极增重16g |
您最近一年使用:0次
2020-08-06更新
|
155次组卷
|
9卷引用:重庆市巴蜀中学2019-2020学年高一下学期期末考试化学试题
名校
解题方法
2 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。
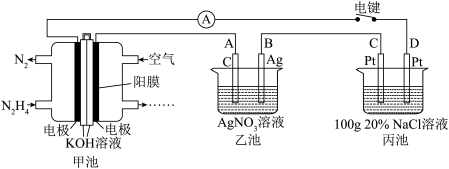
请回答下列问题 :
(1)甲池中,右室的KOH的作用是_________ 。当有l mol电子经过外电路时,左室中减少_______ mol 离子。
(2)乙池中A电极的名称为________ (填“正极”“负极”“阴极”或“阳极”),其电极反应式为________ ,电键闭合10min后,B极质量增加4.32g, 甲池中理论上消耗空气的体积为_____________ mL(标准状况下,假设O2占空气的体积分数为20%),若要使乙池中的电解质溶液完全恢复原状,则加入的试剂可以是:_________ 。
(3)电键闭合10 min 后, D电极附近的pH 将________ (填“增大”“减小”或“不变”);若C电极上产生的气体,用丙池反应后的溶液将其完全吸收,则生成的消毒液的有效成分的质量分数为____________ 。(用算式表示,不要求计算结果,但有单位的数据须带上单位。)

请回答下列问题 :
(1)甲池中,右室的KOH的作用是
(2)乙池中A电极的名称为
(3)电键闭合10 min 后, D电极附近的pH 将
您最近一年使用:0次
名校
解题方法
3 . 通信用磷酸铁锂电池具有比能量较高、高温性能突出、绿色环保等优点。它是以磷酸铁锂为正极的二次电池,放电时正极反应为: M 1-xFexPO4+e-+Li+=Li M1- x FexPO4, 其原理如图,下列说法正确的是


| A.放电时,电流由石墨电极流向磷酸铁锂电极 |
B.电池总反应为M 1-xFexPO4+ LiC6 LiM 1-xFexPO4+6C LiM 1-xFexPO4+6C |
| C.放电时 ,负极反应式为 Li C 6 – e- = Li++6C |
| D.充电时,Li+移向磷酸铁锂电极 |
您最近一年使用:0次
名校
4 . 针对下面四套实验装置图,下列说法正确的是


| A.图1装置牺牲镁保护铁 |
| B.用图2装置铁钉发生吸氧腐蚀腐蚀导致试管中水面上升 |
| C.图3装置中Mg作负极,Al作正极 |
| D.用图4装置对二次电池进行充电 |
您最近一年使用:0次
名校
5 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。

I.用图甲所示装置进行第一组实验时:
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______ (填字母)。
(2)实验过程中,
_______ (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象是_______ 。
II.该小组同学用图乙所示装置进行第二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根( )在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
)在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
(3)电解过程中,X极处溶液的OH-浓度_______ (填“增大”“减小”或“不变)。
(4)电解过程中,Y极发生的电极反应为_______ ,_______ 。
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为_______ mL(均已折算为标准状况时气体体积)。
(6)K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电池反应总反应式为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的电极反应式为_______ 。

I.用图甲所示装置进行第一组实验时:
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______ (填字母)。
| A.石墨 | B.镁 | C.银 | D.铂 |

II.该小组同学用图乙所示装置进行第二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(
 )在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
)在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:(3)电解过程中,X极处溶液的OH-浓度
(4)电解过程中,Y极发生的电极反应为
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为
(6)K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电池反应总反应式为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的电极反应式为
您最近一年使用:0次
2018-07-08更新
|
630次组卷
|
5卷引用:【全国百强校】重庆市巴蜀中学2017-2018学年高一下学期期末考试化学试题
名校
6 . 甲、乙两池电极材料都是铁棒与碳棒(如图)。诸回答下列问题:

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的_____ 棒;乙池中的____ 棒。
②在乙池中阳极的电极反应是____________ 。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中总反应的离子方程式:___________________ 。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为______________ 。

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的
②在乙池中阳极的电极反应是
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中总反应的离子方程式:
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为
您最近一年使用:0次



