1 . 电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
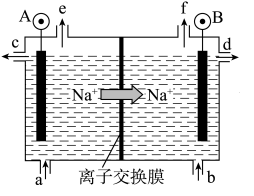
精制饱和食盐水在b口加入的物质为___________ (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
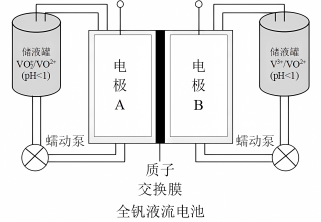
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________ 。
②当完成储能时,阴极溶液的颜色是___________
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
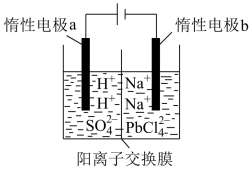
①写出电解时阴极的电极反应式___________
②电解过程中通过阳离子交换膜的离子主要为___________
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向___________ 极室(填“阴”或者“阳”)加入___________ (填化学式)。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

精制饱和食盐水在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
| 离子种类 | VO | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近半年使用:0次
名校
解题方法
2 . 工业上常用 溶液除去烟气中的
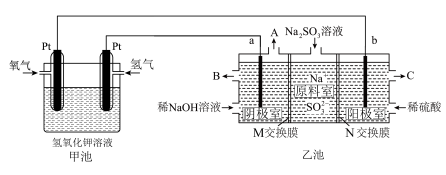
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。_______ 极(填“正”或“负”),写出通入氢气的电极反应式_______ 。
(2)①乙池中阳极室 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为_______ (填“阳”或“阴”)离子交换膜,写出阳极室的电极反应式_______ 。
②阴极室中 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的_______ (用离子符号或化学式填空,下同)得电子反应生成_______ ,其浓度减小,使溶液中_______ 浓度增大,为了保持阴极室溶液中阴阳离子电荷平衡,_______ 从原料室向阴极室迁移,从而使阴极室中 的浓度增大。
的浓度增大。
(3)在标准状况下,若甲池中有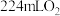 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成_______ 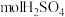 。
。
(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上, 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为_______ 。
 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。
(2)①乙池中阳极室
 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为②阴极室中
 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的 的浓度增大。
的浓度增大。(3)在标准状况下,若甲池中有
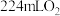 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成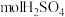 。
。(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上,
 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为
您最近半年使用:0次
2024-01-21更新
|
133次组卷
|
2卷引用:福建省永春第一中学2023-2024学年高一下学期4月月考化学试题
解题方法
3 .  是主要的大气污染气体,利用电化学原理是治理污染的重要方法。
是主要的大气污染气体,利用电化学原理是治理污染的重要方法。
(1)工业上用 吸收尾气中
吸收尾气中 使之转化为
使之转化为 ,再以
,再以 为原料设计原电池,然后电解(惰性电极)
为原料设计原电池,然后电解(惰性电极) 制取
制取 ,从而达到治理污染的目的,装置如下:
,从而达到治理污染的目的,装置如下:
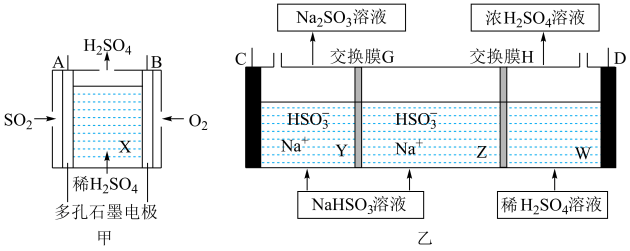
①图甲中A电极的电极名称为__________ 极,图甲中B极的电极反应为__________ 。
②交换膜G为__________ (填“阴离子”或“阳离子”)交换膜。
③图乙中阳极的电极反应式为__________ 。
(2)可以利用联合法吸收大气污染物,图丙是同时吸收 和NO的示意图。
和NO的示意图。
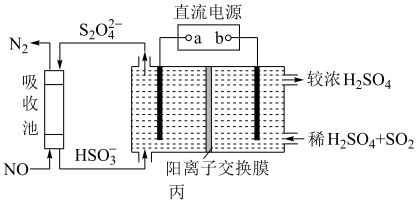
①b是直流电源的__________ 。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为__________ 。
③吸收池中发生反应的氧化剂与还原剂的物质的量之比为__________ 。
 是主要的大气污染气体,利用电化学原理是治理污染的重要方法。
是主要的大气污染气体,利用电化学原理是治理污染的重要方法。(1)工业上用
 吸收尾气中
吸收尾气中 使之转化为
使之转化为 ,再以
,再以 为原料设计原电池,然后电解(惰性电极)
为原料设计原电池,然后电解(惰性电极) 制取
制取 ,从而达到治理污染的目的,装置如下:
,从而达到治理污染的目的,装置如下:
①图甲中A电极的电极名称为
②交换膜G为
③图乙中阳极的电极反应式为
(2)可以利用联合法吸收大气污染物,图丙是同时吸收
 和NO的示意图。
和NO的示意图。
①b是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③吸收池中发生反应的氧化剂与还原剂的物质的量之比为
您最近半年使用:0次
名校
解题方法
4 . 下列说法正确的是
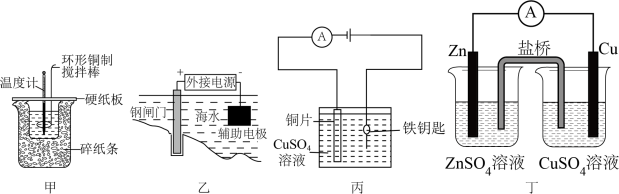

A.用图甲装置测得中和热 偏大 偏大 |
| B.图乙可以保护钢闸门不被腐蚀 |
| C.图丙用于铁上镀铜且硫酸铜溶液浓度不变 |
D.图丁装置盐桥中阴离子向 溶液中迁移 溶液中迁移 |
您最近半年使用:0次
2023-12-14更新
|
413次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题福建省福州格致中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假收官卷02-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)重庆市万州二中2023-2024学年高二下学期开学考试 化学
名校
解题方法
5 . 下列选项描述与对应图像相符的是
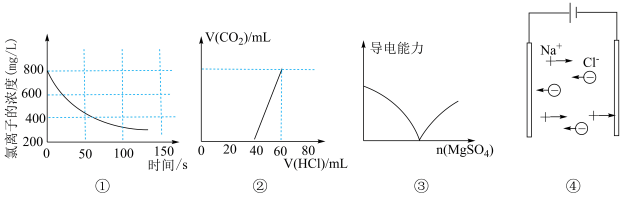

A.图①为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图②为 、 、 混合液中滴加盐酸产生 混合液中滴加盐酸产生 的图像 的图像 |
C.图③为 溶液中滴加 溶液中滴加 溶液的导电性变化图像 溶液的导电性变化图像 |
D.图④为 在水溶液中电离的图示 在水溶液中电离的图示 |
您最近半年使用:0次
解题方法
6 . 某小组探究电解氯化铜的产物,设计如下实验(以石墨为电极):
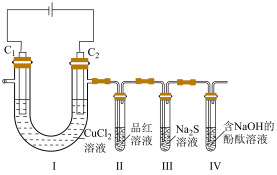
实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是

实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是
| A.根据Ⅲ试管中现象可知,氯的非金属性比硫强 |
B.一段时间后, 极附着一层红色固体物质 极附着一层红色固体物质 |
| C.上述实验中,试管Ⅱ和Ⅳ褪色原理不相同 |
| D.如果用铜极替代石墨也能得到与上述实验完全相同的实验现象 |
您最近半年使用:0次
2023-10-08更新
|
86次组卷
|
2卷引用:河北省秦皇岛市青龙满族自治县2校联考2023-2024学年高一上学期12月月考化学试题
名校
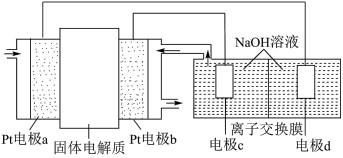
7 . 利用氢氧燃料电池,以镍、铁作电极电解 溶液制备高铁酸钠(
溶液制备高铁酸钠( ,其在浓碱中稳定存在)的装置如图所示。已知固体电解质是掺杂了
,其在浓碱中稳定存在)的装置如图所示。已知固体电解质是掺杂了 的
的 晶体,在高温下能传导
晶体,在高温下能传导 。下列说法正确的是
。下列说法正确的是
 溶液制备高铁酸钠(
溶液制备高铁酸钠( ,其在浓碱中稳定存在)的装置如图所示。已知固体电解质是掺杂了
,其在浓碱中稳定存在)的装置如图所示。已知固体电解质是掺杂了 的
的 晶体,在高温下能传导
晶体,在高温下能传导 。下列说法正确的是
。下列说法正确的是
A.电极 的电极反应为 的电极反应为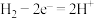 |
B.电极 材料是铁电极,电极反应为 材料是铁电极,电极反应为 |
C.理论上,固体电解质中每迁移 ,可以制得 ,可以制得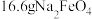 |
D.为提高 的产率,应使用阳离子交换膜 的产率,应使用阳离子交换膜 |
您最近半年使用:0次
2023-08-31更新
|
569次组卷
|
3卷引用:贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题
名校
8 . 锌—空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH-+2H2O=2Zn(OH) 下列说法正确的是
下列说法正确的是
 下列说法正确的是
下列说法正确的是A.放电时,负极反应为:Zn+4OH--2e-=Zn(OH) |
| B.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况) |
| C.充电时,电解质溶液中K+向阳极移动 |
| D.充电时,电解质溶液中c(OH-)逐渐减小 |
您最近半年使用:0次
2023-07-30更新
|
78次组卷
|
3卷引用:黑龙江省大庆铁人中学2022-2023学年高一下学期期末化学试题
名校
解题方法
9 . 将下图所示实验装置的K闭合,回答下列问题:
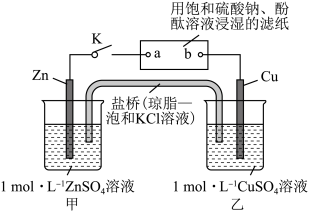
(1)盐桥中的Cl-向_______ 移动,(填“甲池”或“乙池”)滤纸上的 向
向_______ 移动(填“a”或“b”)。
(2)Cu电极上的电极反应式:_______ ,滤纸b点发生_______ 反应(填“氧化”或“还原”)。
(3)a点的电极反应式:_______ ,可观察到滤纸a点现象:_______ 。

(1)盐桥中的Cl-向
 向
向(2)Cu电极上的电极反应式:
(3)a点的电极反应式:
您最近半年使用:0次
2023-07-19更新
|
178次组卷
|
2卷引用:黑龙江省大庆铁人中学2022-2023学年高一下学期期末化学试题
名校
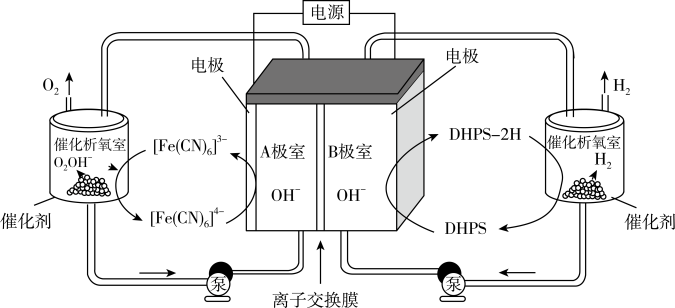
10 . 我国科学家设计了一种高效电解水制氢的系统,实现了在催化剂作用下析氢和析氧反应分离。该系统的工作原理如图所示,其中电极均为惰性电极,电解液中含 。下列关于该装置工作时的说法正确的是
。下列关于该装置工作时的说法正确的是
 。下列关于该装置工作时的说法正确的是
。下列关于该装置工作时的说法正确的是
| A.A电极与外电路的正极相连 |
| B.该装置中离子交换膜为质子交换膜 |
C.催化析氢室的反应为: |
D.理论上,该过程中溶液中 的浓度会不断减小 的浓度会不断减小 |
您最近半年使用:0次



