解题方法
1 . 许多有机化学反应包含电子的转移,使这些反应在电解池中进行时称为电有机合成。制取尼龙-66的原料已二腈 用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
 用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是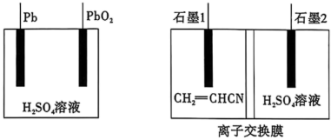
| A.石墨1应与铅酸蓄电池的Pb电极相连 |
| B.离子交换膜应使用阳离子交换膜 |
C.石墨电极1上发生的电极反应为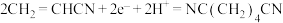 |
D.每生成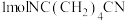 ,石墨2所在极区溶液减重16g ,石墨2所在极区溶液减重16g |
您最近一年使用:0次
名校
2 . CO2的资源化利用不仅可以减少CO2的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:
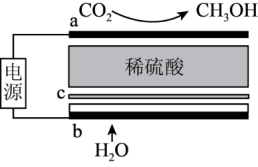
(1)a电极与电源的_______ 极相连,其中c为质子交换膜,写出b电极的电极反应式_______ 。
II. 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
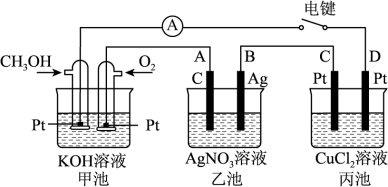
请回答下列问题:
(2)通入CH3OH电极的电极反应式为_______ 。
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出_______ gAg。
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后_______ (填C或D)极首先变红,写出电解时总离子反应式_______ 。
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
则CH4—CO2催化重整反应的ΔH=_______ kJ·mol-1。
I.科学家致力于CO2电催化合成甲醇的研究,其工作原理如图:

(1)a电极与电源的
II.
 燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动、洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入CH3OH电极的电极反应式为
(3)当丙池某个电极增重25.6g时,乙池中收集到了标况下11.2L气体。则乙池中析出
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后
(5)CH4—CO2催化重整对温室气体的减排具有重要意义,其反应为:CH4(g)+CO2(g)⇌2CO(g)+2H2(g)。已知相关物质的燃烧热(25℃、101kPa):
| 物质 | CH4(g) | CO(g) | H2(g) |
| 燃烧热(ΔH/kJ·mol-1) | -890.3 | -283.0 | -285.8 |
您最近一年使用:0次
名校
解题方法
3 .  的资源化利用不仅可以减少
的资源化利用不仅可以减少 的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
Ⅰ.科学家致力于 电催化合成甲醇的研究,其工作原理如图:
电催化合成甲醇的研究,其工作原理如图:
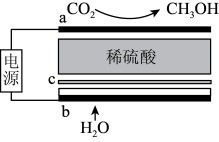
(1)b电极与电源的_______ 极相连,其中c为质子交换膜,写出a电极的电极反应式_______
Ⅱ. 燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
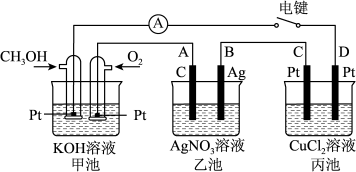
请回答下列问题:
(2)通入 电极的电极反应式为
电极的电极反应式为_______ 。
(3)当丙池某个电极增重38.4g时,乙池中收集到了标况下11.2L气体。则甲池中理论上消耗 的物质的量为
的物质的量为_______ mol,乙池中析出_______ gAg。
(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后_______ (C或D)极首先变红,写出电解时总离子反应式_______
 的资源化利用不仅可以减少
的资源化利用不仅可以减少 的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。
的排放,而且可以提供绿色制备的技术路线,有助于促进“碳中和,碳达峰”。Ⅰ.科学家致力于
 电催化合成甲醇的研究,其工作原理如图:
电催化合成甲醇的研究,其工作原理如图:
(1)b电极与电源的
Ⅱ.
 燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
燃料电池具有低温快速启动,洁净环保等优点,可能成为未来便携式电子产品应用的主流。
请回答下列问题:
(2)通入
 电极的电极反应式为
电极的电极反应式为(3)当丙池某个电极增重38.4g时,乙池中收集到了标况下11.2L气体。则甲池中理论上消耗
 的物质的量为
的物质的量为(4)若丙中电极不变,将其溶液换成KI溶液,溶液中加入无色酚酞溶液,闭合电键后
您最近一年使用:0次
4 . 我国科研团队以聚氨酯为电解液(合成路线如图)实现了稳定高效且可遵循环的K— 电池。总反应为:
电池。总反应为: ,其中生成的
,其中生成的 附着在正极上。下列说法错误的是
附着在正极上。下列说法错误的是
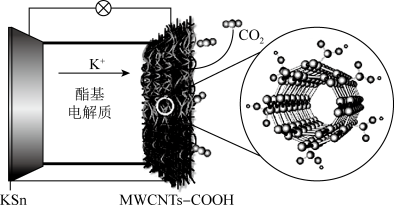
 电池。总反应为:
电池。总反应为: ,其中生成的
,其中生成的 附着在正极上。下列说法错误的是
附着在正极上。下列说法错误的是
| A.放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管 |
B.电池的正极反应式为 |
| C.羧基化碳纳米管中引入的羧基可促进电子的转移 |
| D.充电时,电路中通过1mol电子,多壁碳纳米管减重36g |
您最近一年使用:0次
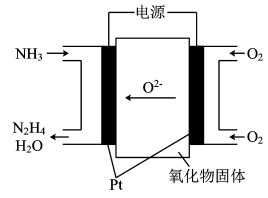
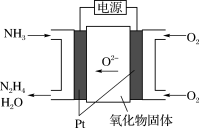
5 . (1)工业上利用N2和H2合成NH3,NH3又可以进一步制备联氨(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为___________ ,有学者探究用电解法制备的效率,装置如图,试写出其阳极电极反应式_________ ;
(2)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)△H=-akJ/mol,已知:CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g)△H=-akJ/mol,已知:CO(g)+H2O(g) CO2(g)+H2(g)△H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:
CO2(g)+H2(g)△H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:_________________ 。
(3)如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。

根据要求回答相关问题:
①甲装置中正极的电极反应式为:________________ 。
②乙装置中石墨电极产生产物如何检验______ ,电解一段时间后,乙池中的溶液呈___ 性。
③图中用丙装置模拟工业中的________ 原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为_____ g。

(2)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g)
 CH3CH2OH(g)+H2O(g)△H=-akJ/mol,已知:CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g)△H=-akJ/mol,已知:CO(g)+H2O(g) CO2(g)+H2(g)△H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:
CO2(g)+H2(g)△H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:(3)如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。

根据要求回答相关问题:
①甲装置中正极的电极反应式为:
②乙装置中石墨电极产生产物如何检验
③图中用丙装置模拟工业中的
您最近一年使用:0次
名校
解题方法
6 . 《自然》杂志报道,科学家们设计出了利用合成气合成液态烃和甲醇,模拟制备合成气的装置如图所示。下列说法不正确的是


| A.交换膜是阳离子交换膜 |
| B.a极是正极,发生还原反应 |
C.由 合成 合成 的电极反应式为 的电极反应式为 |
D.当装置中产生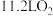 (标准状态)时,理论上迁移的离子为 (标准状态)时,理论上迁移的离子为 |
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)已知: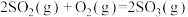
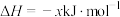
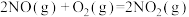
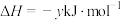
则反应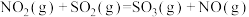 的
的 =
=______  。
。
(2)二十世纪初,工业上以 和
和 ,为原料在一定温度和压强下合成尿素。反应分两步:
,为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和
和 生成
生成 ;
;
ⅱ. 分解生成尿素。
分解生成尿素。
①合成尿素反应的热化学方程式为______ 。
②结合反应过程中能量变化示意图1,下列说法正确的是______ (填序号)。

a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.对总反应速率影响较大的是反应ⅰ
(3)某研究团队合成的低配位Cu在碱性条件下催化 还原生成乙烯的电化学装置如图2所示。
还原生成乙烯的电化学装置如图2所示。
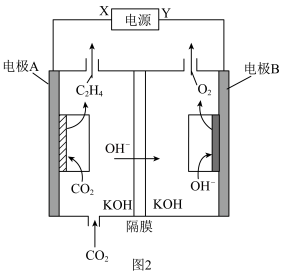
①Y为电源的______ (填“正极”或“负极”)。
②电极A上的电极反应式为______ 。
③理论上电极A上消耗的 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为______ 。
(4)以Al和 为电极,NaOH溶液为电解液组成一种新型电池,该电池保护地下铁管道不被腐蚀,铁管道应连接电池的
为电极,NaOH溶液为电解液组成一种新型电池,该电池保护地下铁管道不被腐蚀,铁管道应连接电池的______ 电极(填“Al”或“ ”),该电化学防护法称为
”),该电化学防护法称为______ 。
(1)已知:
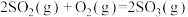
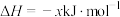
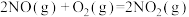
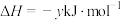
则反应
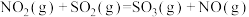 的
的 =
= 。
。(2)二十世纪初,工业上以
 和
和 ,为原料在一定温度和压强下合成尿素。反应分两步:
,为原料在一定温度和压强下合成尿素。反应分两步:ⅰ.
 和
和 生成
生成 ;
;ⅱ.
 分解生成尿素。
分解生成尿素。①合成尿素反应的热化学方程式为
②结合反应过程中能量变化示意图1,下列说法正确的是

a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.对总反应速率影响较大的是反应ⅰ
(3)某研究团队合成的低配位Cu在碱性条件下催化
 还原生成乙烯的电化学装置如图2所示。
还原生成乙烯的电化学装置如图2所示。
①Y为电源的
②电极A上的电极反应式为
③理论上电极A上消耗的
 与电极B上生成的
与电极B上生成的 的物质的量之比为
的物质的量之比为(4)以Al和
 为电极,NaOH溶液为电解液组成一种新型电池,该电池保护地下铁管道不被腐蚀,铁管道应连接电池的
为电极,NaOH溶液为电解液组成一种新型电池,该电池保护地下铁管道不被腐蚀,铁管道应连接电池的 ”),该电化学防护法称为
”),该电化学防护法称为
您最近一年使用:0次
名校
8 . 我国科技工作者设计以CoP和Ni2P纳米片为催化电极材料,电催化合成偶氮化合物的新装置如图所示,下列说法正确的是
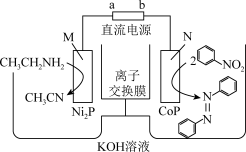

| A.电极a的电势低于b极 |
| B.该离子交换膜是阴离子交换膜 |
| C.M极的电极反应式为CH3CH2NH2+4e- +4OH-=CH3CN+4H2O |
| D.电子由直流电源出发,经电极b, KOH溶液,电极a回到直流电源 |
您最近一年使用:0次
名校
解题方法
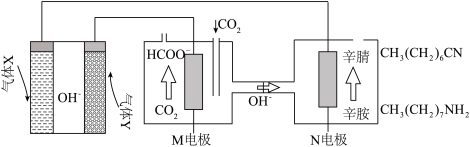
9 . 用氢氧燃料电池为电源,以 与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,装置工作原理如图。下列说法错误的是
与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,装置工作原理如图。下列说法错误的是
 与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,装置工作原理如图。下列说法错误的是
与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,装置工作原理如图。下列说法错误的是
| A.气体X为氧气,气体Y为氢气 |
| B.工作过程中燃料电池内溶液的pH保持不变 |
C.每消耗1 mol  会有4 mol 会有4 mol  由M电极区移向N电极区 由M电极区移向N电极区 |
D.M电极上的电极反应式为 |
您最近一年使用:0次
2023-07-11更新
|
346次组卷
|
6卷引用:安徽省安庆、池州、铜陵三市2022-2023学年高二下学期期末检测化学试题
解题方法
10 . 回答下列问题:
(1)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_______ 。
②已知H2O(l)=H2O(g) ΔH=44kJ·mol-1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是_______ kJ。
③上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是_______ 。
(2)如图所示,某研究性学习小组利用上述氧化还原反应原理设计一个肼(N2H4)-空气燃料电池(如图甲)并探究某些工业原理。
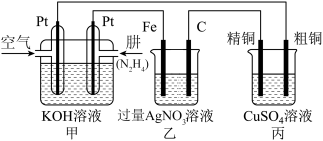
根据要求回答相关问题:
①甲装置中正极的电极反应式为_______ 。
②乙装置中Fe电极的电极反应式为_______ 。电解一段时间后,乙装置中的溶液呈_______ 性。
③图中用丙装置模拟工业中的_______ 原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中消耗肼的质量为_______ g。
(3)工业上利用N2和H2合成NH3,NH3又可以进一步制备肼(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为_______ 。有学者探究用电解法制备,装置如图所示,试写出其阳极的电极反应式:_______ 。
(1)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②已知H2O(l)=H2O(g) ΔH=44kJ·mol-1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是
③上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是
(2)如图所示,某研究性学习小组利用上述氧化还原反应原理设计一个肼(N2H4)-空气燃料电池(如图甲)并探究某些工业原理。

根据要求回答相关问题:
①甲装置中正极的电极反应式为
②乙装置中Fe电极的电极反应式为
③图中用丙装置模拟工业中的
(3)工业上利用N2和H2合成NH3,NH3又可以进一步制备肼(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为

您最近一年使用:0次



