名校
1 . Ⅰ.化学电源在生产生活中有着广泛的应用,请回答下列问题。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
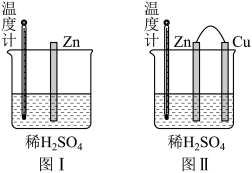
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ 。
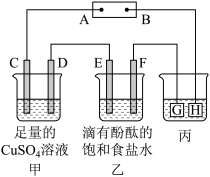
(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:_____ ,C电极反应式:_____ ,乙池中发生的离子反应方程式为:_____ ,丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在_____ 处(填G或H)。为证明铁被保护,可先取少量电解后溶液于试管中,向溶液中加入_____ 溶液观察颜色变化。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能够设计原电池的是______。
A.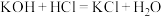 | B. |
C.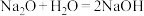 | D. |
(2)为了探究化学反应能量变化,某同学设计了两个实验(如图Ⅰ,Ⅱ)。有关实验现象,说法正确的是:_______。

| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 | B.图Ⅰ和图Ⅱ中温度计示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ中的气泡均产生于锌棒表面 | D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是2mol/L的KOH溶液,电池反应为:
 ,该电池负极的电极反应为:
,该电池负极的电极反应为:(4)以上述氨燃料电池接下图(甲乙丙) A、B两极(C、D、E、F都是惰性电极)。电源接通后,F极附近溶液呈红色,请回答:甲池中电极C名称为:

您最近半年使用:0次
2 . 某化学兴趣小组的同学设计了如图所示原电池装置。下列说法不正确的是


A.溶液中 向Zn电极移动 向Zn电极移动 |
B.Zn片上发生还原反应: |
| C.电池工作一段时间后,铜片质量增大溶液 |
D.该装置能证明金属的活动性: |
您最近半年使用:0次
名校
3 . 下列设计正确且能实现实验目的的是


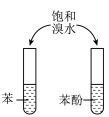
A.图①,验证 可溶于氨水 可溶于氨水 |
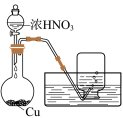
B.图②,验证氯气和甲烷反应生成了 |
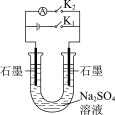
C.图③,闭合 一段时间,再打开 一段时间,再打开 闭合 闭合 可制得简易燃料电池,左侧石墨为电池负极 可制得简易燃料电池,左侧石墨为电池负极 |
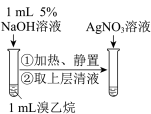
D.图④,分别加热不能证明 分解温度高于 分解温度高于 |
您最近半年使用:0次
解题方法
4 . Ⅰ.化学电源在生产生活中有着广泛的应用。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
(2)为了探究化学反应中的能量变化,某同学用相同的 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________

Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是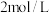 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ ,当反应消耗 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为___________ (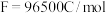 )。
)。
(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。
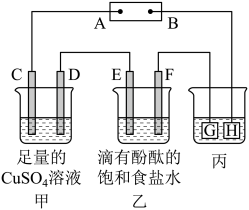
①甲池中C电极为___________ 极,乙池中发生的离子反应方程式为___________ 。
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在___________ 处(填G或H)。为了证明铁能否被保护,可先取少量电解后的溶液于试管中,再向试管中加入___________ (填化学式)溶液,观察是否产生特征蓝色沉淀。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
A.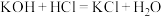 | B. |
C.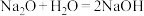 | D. |
(2)为了探究化学反应中的能量变化,某同学用相同的
 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
| A.消耗相同质量的Zn,图Ⅰ中产生的热能大于图Ⅱ |
| B.消耗相同质量的Zn,图Ⅰ中产生的热能等于图Ⅱ |
| C.图Ⅰ和图Ⅱ的锌棒表面均有大量气泡产生 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是
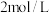 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为: 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为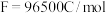 )。
)。(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。

①甲池中C电极为
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在
您最近半年使用:0次
名校
解题方法
5 . 一种简单的原电池装置如图所示。据图回答下列问题。
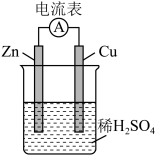
(1)锌是该电池的_______ (填“正”或“负”)极。Zn片上发生的电极反应为___________ 。Cu片上发生的电极反应为_________ 。能证明化学能转化为电能的实验现象为___________ 。
(2)装置中稀硫酸的作用是___________。
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是______ 。
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是___________ (填序号)。
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O

(1)锌是该电池的
(2)装置中稀硫酸的作用是___________。
| A.电极材料 | B.电极反应物 | C.电子导体 | D.离子导体 |
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是
| A | B | C | D |
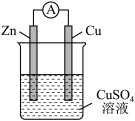 | 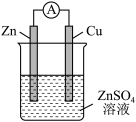 |  | 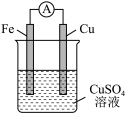 |
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O
您最近半年使用:0次
名校
解题方法
6 . 某实验小组对 分别与
分别与 、
、 的反应进行探究。
的反应进行探究。
【甲同学的实验】
(1)甲同学探究实验Ⅰ的电极产物。
①取少量 溶液电极附近的混合液,加入
溶液电极附近的混合液,加入___________ ,产生白色沉淀,证明产生了 。
。
②该同学又设计实验探究另一电极的产物,所需检验试剂及现象分别是___________ 、___________ 。
(2)实验Ⅰ中负极的电极反应式为___________ 。
【乙同学的实验】
乙同学进一步探究 溶液与
溶液与 溶液能否发生反应,设计、完成实验并记录如下:
溶液能否发生反应,设计、完成实验并记录如下:
(3)查阅资料:溶液中 、
、 、
、 三种微粒会形成红色配合物并存在如下转化:
三种微粒会形成红色配合物并存在如下转化:

从反应速率和化学平衡两个角度解释1~30min的实验现象:___________ 。
(4)解释30min后上层溶液又变为浅红色的可能原因:___________ 。
【实验反思】
(5)分别对比Ⅰ和Ⅱ、Ⅱ和Ⅲ, 能否与
能否与 或
或 发生氧化还原反应和
发生氧化还原反应和___________ 有关(写出两条)。
 分别与
分别与 、
、 的反应进行探究。
的反应进行探究。【甲同学的实验】
| 装置 | 编号 | 试剂X | 实验现象 |
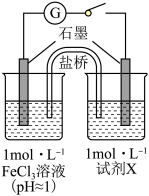 | Ⅰ |  溶液( 溶液(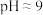 ) ) | 闭合开关后灵敏电流计指针发生偏转 |
| Ⅱ |  溶液( 溶液( ) ) | 闭合开关后灵敏电流计指针未发生偏转 |
①取少量
 溶液电极附近的混合液,加入
溶液电极附近的混合液,加入 。
。②该同学又设计实验探究另一电极的产物,所需检验试剂及现象分别是
(2)实验Ⅰ中负极的电极反应式为
【乙同学的实验】
乙同学进一步探究
 溶液与
溶液与 溶液能否发生反应,设计、完成实验并记录如下:
溶液能否发生反应,设计、完成实验并记录如下:| 装置 | 编号 | 反应时间 | 实验现象 |
 | Ⅲ | 0~1min | 产生红色沉淀,有刺激性气味气体逸出 |
| 1~30min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | ||
| 30min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
 、
、 、
、 三种微粒会形成红色配合物并存在如下转化:
三种微粒会形成红色配合物并存在如下转化:
从反应速率和化学平衡两个角度解释1~30min的实验现象:
(4)解释30min后上层溶液又变为浅红色的可能原因:
【实验反思】
(5)分别对比Ⅰ和Ⅱ、Ⅱ和Ⅲ,
 能否与
能否与 或
或 发生氧化还原反应和
发生氧化还原反应和
您最近半年使用:0次
名校
7 . 下列实验能达到实验目的的是
| A | B |
|
|
| 制作简单的燃料电池 | 证明苯环使羟基活化 |
| C | D |
|
|
制备并收集 | 检验溴乙烷的水解产物 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-23更新
|
112次组卷
|
2卷引用:北京师范大学附属中学2023-2024学年高三上学期期中考试化学试题
8 . 下列电化学装置能达到目的的是


A.图甲:实现原电池反应 ,产生稳定的电流 ,产生稳定的电流 |
B.图乙:制取少量 |
| C.图丙:证明铁发生吸氧腐蚀 |
| D.图丁:在铁表面镀锌 |
您最近半年使用:0次
名校
解题方法
9 . 回答下列问题:
Ⅰ.某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
资料:单质硫可溶于过量硫化钠溶液形成淡黄色的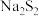 溶液。
溶液。
(1)根据实验可知, 具有
具有___________ 性。
(2)甲同学预测实验Ⅰ中 被氧化成
被氧化成 。
。
①根据实验现象,乙同学认为甲的预测不合理,理由是___________ 。
②乙同学取实验Ⅰ中少量溶液进行实验,检测到有 ,得出
,得出 被氧化成
被氧化成 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是___________ 。
③同学们经讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。
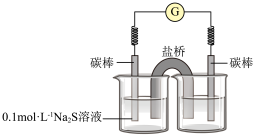
右侧烧杯中的溶液是___________ ;连通后电流计指针偏转,一段时间后,取左侧烧杯中的溶液,用盐酸酸化后,滴加 溶液,观察到有白色沉淀生成,证明
溶液,观察到有白色沉淀生成,证明 氧化成了
氧化成了 。
。
Ⅱ.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的___________ (填“正”或“负”)极,其电极反应式为___________ 。
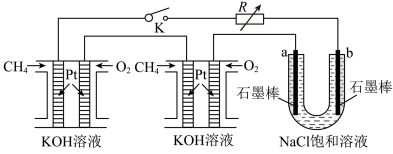
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验:如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为___________ (法拉第常数 ),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为___________ (假设反应后溶液体积不变)。
Ⅰ.某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | Ⅰ | Ⅱ |
| 实验过程 | 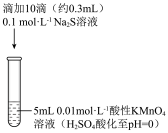 |  |
| 实验 现象 | 紫色变浅(pH>1),生成棕褐色沉淀( ) ) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀( ) ) |
 溶液。
溶液。(1)根据实验可知,
 具有
具有(2)甲同学预测实验Ⅰ中
 被氧化成
被氧化成 。
。①根据实验现象,乙同学认为甲的预测不合理,理由是
②乙同学取实验Ⅰ中少量溶液进行实验,检测到有
 ,得出
,得出 被氧化成
被氧化成 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是③同学们经讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。
右侧烧杯中的溶液是
 溶液,观察到有白色沉淀生成,证明
溶液,观察到有白色沉淀生成,证明 氧化成了
氧化成了 。
。Ⅱ.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验:如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为
 ),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
您最近半年使用:0次
10 . 下列实验装置或操作正确的是


| A.用甲装置制作简单燃料电池 | B.用乙装置制备 并测量其体积 并测量其体积 |
| C.用丙装置检验乙炔具有还原性 | D.用丁装置证明苯环使羟基活化 |
您最近半年使用:0次