名校
解题方法
1 . 依据如图所示三套装置,分别回答下列问题。
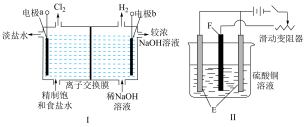
(1)电解饱和食盐水的原理如装置Ⅰ所示。
①电解饱和食盐水的化学方程式是___________ 。
②电极a接电源的___________ (填“正”或“负”)极。
③电极b的反应式是___________ 。
④离子交换膜主要允许___________ (填离子符号)通过。
(2)装置Ⅱ的实验目的是在铁棒上镀铜,铁棒为___________ (填“E”或“F”)。另一电极用于及时补充消耗的镀层物质,结合化学用语说明其原理:___________ 。
(3)装置Ⅲ利用 与Cu发生的反应,设计一个可正常工作的电池,补全该电化学装置示意图
与Cu发生的反应,设计一个可正常工作的电池,补全该电化学装置示意图__________ ,写出电池工作一段时间后的现象。

工作一段时间后的现象是___________ 。

(1)电解饱和食盐水的原理如装置Ⅰ所示。
①电解饱和食盐水的化学方程式是
②电极a接电源的
③电极b的反应式是
④离子交换膜主要允许
(2)装置Ⅱ的实验目的是在铁棒上镀铜,铁棒为
(3)装置Ⅲ利用
 与Cu发生的反应,设计一个可正常工作的电池,补全该电化学装置示意图
与Cu发生的反应,设计一个可正常工作的电池,补全该电化学装置示意图| 供选择的实验用品:KCl溶液,FeCI2溶液,FeCI3溶液,CuSO4溶液,铜棒,锌棒,铁棒,石墨棒,氯化钾盐桥。 |

工作一段时间后的现象是
您最近半年使用:0次
2 . 下列装置和操作能达到实验目的的是
| A | B | C | D |
 |  | 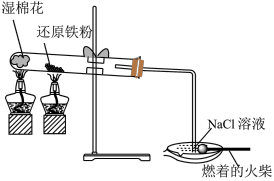 |  |
| 测定醋酸的浓度 | 观察甲烷与氯气反应的现象 | 验证铁与水蒸气反应产生 | 向铁电极区附近溶液中滴入2滴铁氰化钾溶液,验证铁电极受到了保护 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 用如图实验装置进行相应实验,能达到实验目的的是
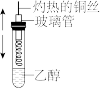 | 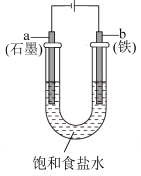 | 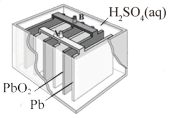 |  |
| 甲 | 乙 | 丙 | 丁 |
| A.装置甲:乙醇可以被氧化为乙醛 |
| B.装置乙:电解饱和食盐水制金属钠 |
| C.装置丙:铅蓄电池负极的质量减小 |
D.装置丁:用 气体和饱和 气体和饱和 溶液能出现喷泉现象 溶液能出现喷泉现象 |
您最近半年使用:0次
名校
解题方法
4 . 以V2O5为原料制备氧钒(Ⅳ)碱式碳酸铵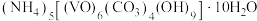 .其过程
.其过程 溶液
溶液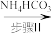 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为___________ ,使用此仪器的优点是_________________________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为_____________________________________ 。
(2)步骤Ⅱ可在如下图装置中进行.
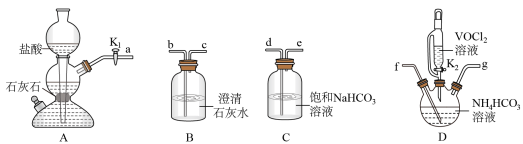
①接口的连接顺序为
___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是__________________________ .当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.
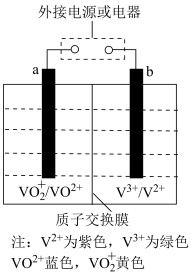
其充电时,阳极的电极方程式为_______________________________________ 。
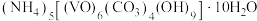 .其过程
.其过程 溶液
溶液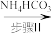 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行.

①接口的连接顺序为

②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取
 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.

其充电时,阳极的电极方程式为
您最近半年使用:0次
名校
5 . 化学是一门以实验为基础的科学探究与创新能力是化学学科核心素养之一,实验探究也是化学学习的重要方法。回答下列问题:
(1)探究浓度、温度对化学平衡的影响。CuCl2溶液中存在下列化学平衡: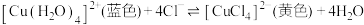
 ,用编号为
,用编号为 的3支试管各取
的3支试管各取 的
的 溶液(蓝绿色)进行下列实验:
溶液(蓝绿色)进行下列实验:
①试管a中进行的操作可以是____ (填标号)。
A.加入蒸馏水稀释 B.滴加浓盐酸 C.滴加AgNO3溶液
②对试管b中溶液加热时,平衡____ (填“正向”“逆向”或“不”)移动。
③对试管c不进行任何操作,其作用是____ 。
(2)利用如图所示装置探究氢氧燃料电池的工作原理。

①电解制备H2、O2:打开K2,闭合K1,连接电池负极的石墨Ⅱ为____ (填“阳极”或“阴极”),阳极的电极反应式为_______ ;_____ (填“石墨I”或“石墨Ⅱ”)附近的溶液变红。
②探究燃料电池的工作原理:在上述实验①结束后,立即打开K1,闭合K2,可以观察到电流表指针偏转,则外电路中电子的流动方向是________ (填“石墨Ⅱ流向石墨Ⅰ”或“石墨Ⅰ流向石墨Ⅱ”);负极的电极反应式是________ 。
(1)探究浓度、温度对化学平衡的影响。CuCl2溶液中存在下列化学平衡:
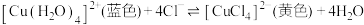
 ,用编号为
,用编号为 的3支试管各取
的3支试管各取 的
的 溶液(蓝绿色)进行下列实验:
溶液(蓝绿色)进行下列实验:| 实验操作(改变的条件) | 实验现象 |
| 试管a:___________ | 溶液变为黄绿色 |
| 试管b:在热水浴中加热 |
A.加入蒸馏水稀释 B.滴加浓盐酸 C.滴加AgNO3溶液
②对试管b中溶液加热时,平衡
③对试管c不进行任何操作,其作用是
(2)利用如图所示装置探究氢氧燃料电池的工作原理。

①电解制备H2、O2:打开K2,闭合K1,连接电池负极的石墨Ⅱ为
②探究燃料电池的工作原理:在上述实验①结束后,立即打开K1,闭合K2,可以观察到电流表指针偏转,则外电路中电子的流动方向是
您最近半年使用:0次
名校
解题方法
6 . 某研究性学习小组用如图所示的装置进行实验,探究原电池、电解池和电解精炼钴的工作原理。一段时间后装置甲的两极均有气体产生,且X极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。请根据实验现象及所查资料,回答下列问题:
查阅资料:高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
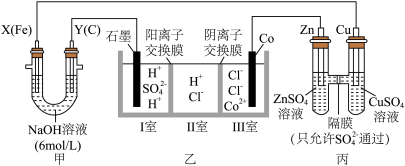
(1)上述装置中,发生还原反应的电极有___________(填字母)。
(2)丙池中的
___________ (填“从左向右”“从右向左”或“不”)移动。
(3)反应过程中,X极处发生的电极反应为 和
和___________ 。
(4)一段时间后,若X极质量减小1.12g,Y电极收集到 气体,则在X极收集到气体为
气体,则在X极收集到气体为___________  (均已折算为标准状况时的气体体积)。
(均已折算为标准状况时的气体体积)。
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中
___________ (填“变大”“变小”或“不变”),该电解池总反应的化学方程式是___________ 。
(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除 外,还可能有
外,还可能有___________ 。
查阅资料:高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(1)上述装置中,发生还原反应的电极有___________(填字母)。
| A.X(Fe) | B.Y(C) | C.Co | D.Zn |
(2)丙池中的

(3)反应过程中,X极处发生的电极反应为
 和
和(4)一段时间后,若X极质量减小1.12g,Y电极收集到
 气体,则在X极收集到气体为
气体,则在X极收集到气体为 (均已折算为标准状况时的气体体积)。
(均已折算为标准状况时的气体体积)。(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中

(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除
 外,还可能有
外,还可能有
您最近半年使用:0次
名校
解题方法
7 . 电压不同,电解饱和食盐水时的阳极产物不同,某学习小组利用如图装置探究在不同电压下电解饱和食盐水的产物(显示的电极均为石墨)。
Ⅰ.电压较低时,利用图1和图2装置制备氯气和“84”消毒液。
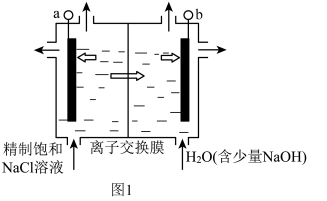
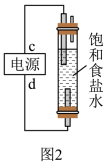
(1)图1中的离子交换膜为___________ (填“阴离子”或“阳离子”)交换膜;图2中,电源的正极接口为___________ (填“c”或“d”)。
Ⅱ.适当加大电压,利用图l装置可制备 。已知
。已知 易溶于水,且不与水反应。
易溶于水,且不与水反应。
(2)产生 的电极反应式为
的电极反应式为___________ 。
(3)当阴极产生标准状况下 气体时,理论上生成
气体时,理论上生成 的物质的量为
的物质的量为___________ 。
Ⅲ.再加大电压,利用图3装置可制备 。
。
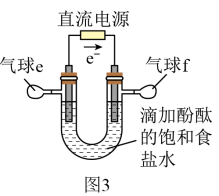
(4)该装置中反应的离子方程式为___________ ;观察到的实验现象为___________ 。
Ⅰ.电压较低时,利用图1和图2装置制备氯气和“84”消毒液。


(1)图1中的离子交换膜为
Ⅱ.适当加大电压,利用图l装置可制备
 。已知
。已知 易溶于水,且不与水反应。
易溶于水,且不与水反应。(2)产生
 的电极反应式为
的电极反应式为(3)当阴极产生标准状况下
 气体时,理论上生成
气体时,理论上生成 的物质的量为
的物质的量为Ⅲ.再加大电压,利用图3装置可制备
 。
。
(4)该装置中反应的离子方程式为
您最近半年使用:0次
2023-03-21更新
|
365次组卷
|
3卷引用:辽宁省名校联盟2022-2023年学高二下学期3月联考化学
辽宁省名校联盟2022-2023年学高二下学期3月联考化学(已下线)上海市华东师范大学第二附属中学2022-2023学年高二下学期期中考试化学试题辽宁省沈阳市等2地辽宁省实验学校等2校2022-2023学年高二下学期3月月考化学试题
名校
解题方法
8 . 某研究性学习小组用下图所示的装置进行实验,探究原电池、电解池和电解精炼钴的工作原理。一段时间后装置甲的两极均有气体产生,且X极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。请根据实验现象及所查资料,回答下列问题:
查阅资料:高铁酸根 在溶液中呈紫红色。
在溶液中呈紫红色。
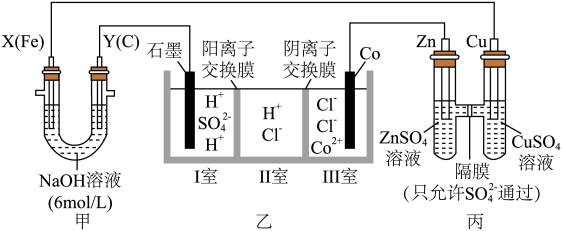
(1)上述装置中,发生氧化反应的电极有_______(填字母)。
(2)丙池中的
_______ (填“从左向右”、“从右向左”或“不”)移动。
(3)反应过程中,X极处发生的电极反应为 和
和_______ 。
(4)一段时间后,若X极质量减小1.12g,Y电极收集到2.24L气体,则在X极收集到气体为_______ mL(均已折算为标准状况时气体体积)。
(5)乙池是电解制备金属钴的装置图,理论上I室中
_______ (填“变大”、“变小”或“不变”),该电解池总反应的化学方程式是_______ 。
(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除 外,还可能有
外,还可能有_______ 。
查阅资料:高铁酸根
 在溶液中呈紫红色。
在溶液中呈紫红色。
(1)上述装置中,发生氧化反应的电极有_______(填字母)。
A.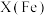 | B. | C. | D. |

(3)反应过程中,X极处发生的电极反应为
 和
和(4)一段时间后,若X极质量减小1.12g,Y电极收集到2.24L气体,则在X极收集到气体为
(5)乙池是电解制备金属钴的装置图,理论上I室中

(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除
 外,还可能有
外,还可能有
您最近半年使用:0次
2023-03-02更新
|
471次组卷
|
3卷引用:辽宁省丹东市2022-2023学年高二上学期期末教学质量监测化学试题
解题方法
9 . Ⅰ.回答下列问题
(1)用0.1000mol/L的NaOH溶液滴定20.00mL醋酸溶液,4次滴定所消耗NaOH溶液的体积如下:
①醋酸溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
②滴定过程中以酚酞做指示剂,下列说法正确的是_______ (填序号)。
a.滴定前,需用醋酸溶液润洗锥形瓶
b.滴定终点时,溶液由粉红色恰好变为无色
c.滴定时,溶液中[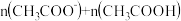 ]始终保持不变
]始终保持不变
③设计实验方案证明醋酸的 大于碳酸的
大于碳酸的 ,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加
,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加_______ 。
(2)25℃时,将pH=13的 溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则
溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则 溶液与HCl溶液的体积比为
溶液与HCl溶液的体积比为_______ 。
(3)25℃时,pH均为a的 和NaOH溶液中,水电离产生的
和NaOH溶液中,水电离产生的 之比为
之比为_______ 。
(4)向饱和 溶液中滴加饱和
溶液中滴加饱和 溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因
溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因_______ 。
(5)某工厂废水中含 的
的 ,为使废水能达标排放,作如下处理:
,为使废水能达标排放,作如下处理: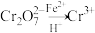 、
、 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的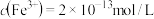 ,则残留的
,则残留的
_______ mol/L。(已知: ,
, )
)
Ⅱ.用甲醇( )燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备
)燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备 (装置乙),示意图如下:
(装置乙),示意图如下:
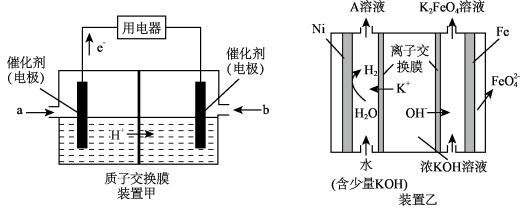
(6)装置甲中,b是_______ (填“甲醇”或“氧气”),负极的电极反应式为_______ 。
(7)装置乙中,Ni电极作_______ 极(填“阴”或“阳”),Fe电极上的电极反应式为_______ 。
(1)用0.1000mol/L的NaOH溶液滴定20.00mL醋酸溶液,4次滴定所消耗NaOH溶液的体积如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 所消耗NaOH溶液的体积/mL | 20.05 | 20.00 | 18.40 | 19.95 |
①醋酸溶液中
 的物质的量浓度为
的物质的量浓度为②滴定过程中以酚酞做指示剂,下列说法正确的是
a.滴定前,需用醋酸溶液润洗锥形瓶
b.滴定终点时,溶液由粉红色恰好变为无色
c.滴定时,溶液中[
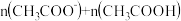 ]始终保持不变
]始终保持不变③设计实验方案证明醋酸的
 大于碳酸的
大于碳酸的 ,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加
,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加(2)25℃时,将pH=13的
 溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则
溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则 溶液与HCl溶液的体积比为
溶液与HCl溶液的体积比为(3)25℃时,pH均为a的
 和NaOH溶液中,水电离产生的
和NaOH溶液中,水电离产生的 之比为
之比为(4)向饱和
 溶液中滴加饱和
溶液中滴加饱和 溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因
溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因(5)某工厂废水中含
 的
的 ,为使废水能达标排放,作如下处理:
,为使废水能达标排放,作如下处理: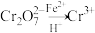 、
、 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的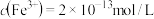 ,则残留的
,则残留的
 ,
, )
)Ⅱ.用甲醇(
 )燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备
)燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备 (装置乙),示意图如下:
(装置乙),示意图如下:
(6)装置甲中,b是
(7)装置乙中,Ni电极作
您最近半年使用:0次
名校
10 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验。回答下列问题:
(1)该小组设计了图1实验装置,模拟工业处理 ,M、N均为惰性材料。
,M、N均为惰性材料。

①从物质变化的角度,该实验装置可用于制备_______ ,从能量变化角度,当看到_______ 现象时,说明该实验装置同时获得了电能。
②M极的电极反应式为_______ 。
(2)该研究性学习小组利用电解法将 转化为
转化为 ,实现了
,实现了 的资源化利用.电解的工作原理如图2所示。
的资源化利用.电解的工作原理如图2所示。
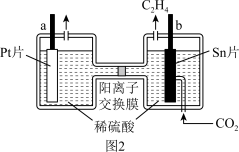
①a极接电源_______ 极,b极电极反应式为_______ 。
②若a极收集到 (标准状况)气体,则理论上消耗
(标准状况)气体,则理论上消耗 的质量为
的质量为_______ g(忽略气体的溶解)。
(1)该小组设计了图1实验装置,模拟工业处理
 ,M、N均为惰性材料。
,M、N均为惰性材料。
①从物质变化的角度,该实验装置可用于制备
②M极的电极反应式为
(2)该研究性学习小组利用电解法将
 转化为
转化为 ,实现了
,实现了 的资源化利用.电解的工作原理如图2所示。
的资源化利用.电解的工作原理如图2所示。
①a极接电源
②若a极收集到
 (标准状况)气体,则理论上消耗
(标准状况)气体,则理论上消耗 的质量为
的质量为
您最近半年使用:0次



