名校
解题方法
1 . 以V2O5为原料制备氧钒(Ⅳ)碱式碳酸铵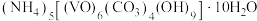 .其过程
.其过程 溶液
溶液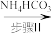 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为___________ ,使用此仪器的优点是_________________________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为_____________________________________ 。
(2)步骤Ⅱ可在如下图装置中进行.
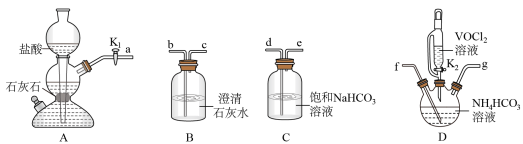
①接口的连接顺序为
___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是__________________________ .当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.
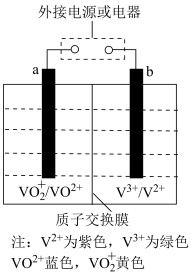
其充电时,阳极的电极方程式为_______________________________________ 。
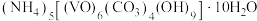 .其过程
.其过程 溶液
溶液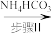 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行.

①接口的连接顺序为

②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取
 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.

其充电时,阳极的电极方程式为
您最近一年使用:0次
名校
2 . 完成下列问题。
(1)用间接电化学法除去NO的过程,如图所示: 在4~7之间,写出阴极的电极反应式:
在4~7之间,写出阴极的电极反应式:___________ 。
②用离子方程式表示吸收池除去NO的原理___________ 。
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能 以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。___________ 。
②分析图3可知,氢氧化钠的质量分数为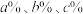 ,由大到小的顺序为
,由大到小的顺序为___________ 。
(1)用间接电化学法除去NO的过程,如图所示:

 在4~7之间,写出阴极的电极反应式:
在4~7之间,写出阴极的电极反应式:②用离子方程式表示吸收池除去NO的原理
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能
 以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。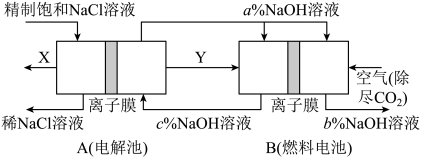
②分析图3可知,氢氧化钠的质量分数为
 ,由大到小的顺序为
,由大到小的顺序为
您最近一年使用:0次
2023-12-19更新
|
116次组卷
|
2卷引用:福建省德化一中、永安一中、漳平一中三校协作2023-2024学年高二上学期12月联考化学试题
名校
解题方法
3 . SO2一空气燃料电池实现了制硫酸、发电、环保三位一体的结合,某实验小组用该燃料电池作电源探究氯碱工业和粗铜精炼的原理,装置示意图如图:
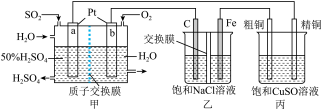
(1)b极的电极反应式为______ ;Fe电极为______ 极,其电极反应式为______ 。
(2)甲装置每消耗32gSO2,溶液中通过质子交换膜的n(H+)为______ mol,如果粗铜中含有锌、银等杂质,丙装置中c(Cu2+)______ (填“增大”“减小”或“不变”)。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(电极未标出)。

装置A发生反应的化学方程式为_____ ;NaOH溶液的质量分数为a%、b%、c%,由大到小的顺序为______ 。

(1)b极的电极反应式为
(2)甲装置每消耗32gSO2,溶液中通过质子交换膜的n(H+)为
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(电极未标出)。

装置A发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
4 . I.某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
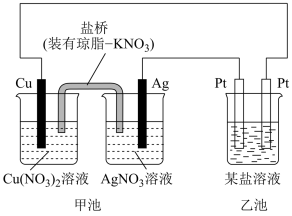
(1)甲池装置为_______ (填“原电池”或“电解池”)。
(2)实验过程中,甲池左侧烧杯 中的浓度
中的浓度_______ (填“增大”、“减小”或“不变”)。
(3)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,则导线中通过_______ mol电子。
(4)其他条件不变,若用U形铜代替“盐桥”,工作一段时间后取出U形铜称量,质量_______ (填“增大”、“减小”或“不变”);若乙池中的某盐溶液为足量的硝酸银溶液,工作一段时间后,若要使乙池中溶液恢复原浓度,可向溶液中加入_______ 。(填化学式)
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。
Ⅱ.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是_______
(7)图中Y是_______ (填化学式),若电解产生11.2L(标准状况)该物质,则至少转移电子_______ mol。
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_______ 。

(1)甲池装置为
(2)实验过程中,甲池左侧烧杯
 中的浓度
中的浓度(3)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,则导线中通过
(4)其他条件不变,若用U形铜代替“盐桥”,工作一段时间后取出U形铜称量,质量
(5)若把乙池改为精炼铜装置(粗铜含Al、Zn、Ag、Pt、Au等杂质),电解质溶液为
 溶液,则下列说法正确的是_______。
溶液,则下列说法正确的是_______。| A.电解过程中,阳极减少的质量与阴极增加的质量相等 |
| B.乙池左侧电极为粗铜,发生氧化反应 |
C. 溶液的浓度保持不变 溶液的浓度保持不变 |
| D.杂质都将以单质的形式沉淀到池底 |
Ⅱ.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图,其中电极未标出,所用离子交换膜只允许阳离子通过。

(6)电解池A中发生的电解化学方程式是
(7)图中Y是
(8)分析图可知:氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
5 .  一空气燃料电池实现了制硫酸、发电、环保三位一体的结合,某实验小组用该燃料电池作电源探究氯碱工业和粗铜精炼的原理,装置示意图如下:
一空气燃料电池实现了制硫酸、发电、环保三位一体的结合,某实验小组用该燃料电池作电源探究氯碱工业和粗铜精炼的原理,装置示意图如下:
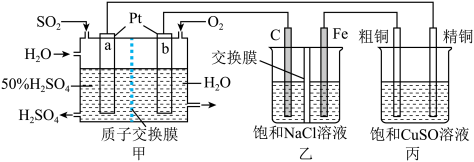
(1)a极的电极反应式为___________ ;Fe电极为___________ 极,其电极反应式为___________ 。
(2)甲装置每消耗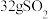 ,溶液中通过质子交换膜的
,溶液中通过质子交换膜的 为
为___________ mol,如果粗铜中含有锌、银等杂质,丙装置中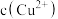
___________ (填“增大”“减小”或“不变”)。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(电极未标出)。
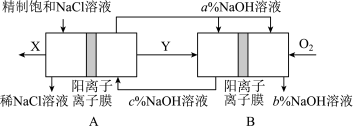
装置A发生反应的化学方程式为___________ ;图中X的化学式为___________ ;NaOH溶液的质量分数为a%、b%、c%,由大到小的顺序为___________ 。
 一空气燃料电池实现了制硫酸、发电、环保三位一体的结合,某实验小组用该燃料电池作电源探究氯碱工业和粗铜精炼的原理,装置示意图如下:
一空气燃料电池实现了制硫酸、发电、环保三位一体的结合,某实验小组用该燃料电池作电源探究氯碱工业和粗铜精炼的原理,装置示意图如下:
(1)a极的电极反应式为
(2)甲装置每消耗
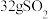 ,溶液中通过质子交换膜的
,溶液中通过质子交换膜的 为
为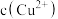
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(电极未标出)。

装置A发生反应的化学方程式为
您最近一年使用:0次
名校
6 . 工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.
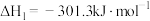 ;
;
 Ⅱ.
Ⅱ.
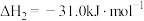 。
。
则CO与 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为___________ 。
(2)某科研小组在 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了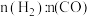 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表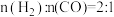 的变化曲线为:
的变化曲线为:___________ (填“曲线a”或“曲线b”)。 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是___________ (填字母)。
b.在恒温恒压的平衡体系中充入氩气, 的产率降低
的产率降低
c.当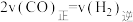 时,反应达到平衡状态
时,反应达到平衡状态
d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲容器平衡后气体的压强为开始时的 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=___________ ,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为___________ 。
(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇( )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为___________ 。
②碳酸二甲酯 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成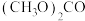 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式:___________ 。
(1)已知:Ⅰ.

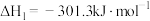 ;
; Ⅱ.
Ⅱ.
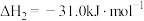 。
。则CO与
 合成气态甲醇的热化学方程式为
合成气态甲醇的热化学方程式为(2)某科研小组在
 作催化剂的条件下,在500℃时,研究了
作催化剂的条件下,在500℃时,研究了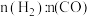 分别为
分别为 、
、 时CO的转化率变化情况(如图1所示),则图中表
时CO的转化率变化情况(如图1所示),则图中表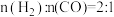 的变化曲线为:
的变化曲线为: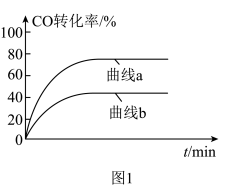
 合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得
合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得 的产率与温度的关系如图2所示。下列说法正确的是
的产率与温度的关系如图2所示。下列说法正确的是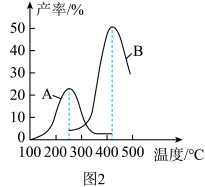
b.在恒温恒压的平衡体系中充入氩气,
 的产率降低
的产率降低c.当
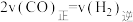 时,反应达到平衡状态
时,反应达到平衡状态d.降低生成物甲醇的浓度,有利于提高甲醇的产率,加快反应速率
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物起始投入量 | 2molCO、 | amolCO、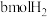 、 、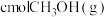 (a、b、c均不为零) (a、b、c均不为零) |
 ,则该温度下,该反应的平衡常数K=
,则该温度下,该反应的平衡常数K=(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(
 )和氧化锆(
)和氧化锆( )晶体,能传导
)晶体,能传导 。则负极的电极反应式为
。则负极的电极反应式为②碳酸二甲酯
 毒性小,是一种绿色化工产品,用CO合成
毒性小,是一种绿色化工产品,用CO合成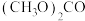 ,其电化学合成原理为
,其电化学合成原理为 ,装置如图3所示,写出阳极的电极反应式:
,装置如图3所示,写出阳极的电极反应式: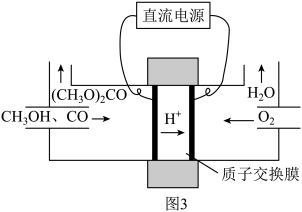
您最近一年使用:0次
名校
7 . 一种清洁、低成本的三步法氯碱工艺工作原理的示意图如图。
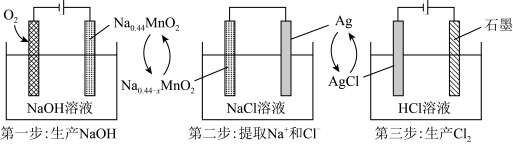
| A.与传统氯碱工艺相比,该方法可避免使用离子交换膜 |
B.第一步中阳极反应为: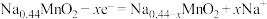 |
| C.第二步中,放电结束后,电解质溶液中NaCl的含量减小 |
| D.理论上,每消耗1molO2,可生产2molNaOH和2molCl2 |
您最近一年使用:0次
2024-04-27更新
|
316次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
8 . 利用库仑测硫仪测定气体中 的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后,
的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解至
还原,测硫仪便立即自动进行电解至 又回到原定值,测定结束后,通过测定电解消耗的电量进行计算
又回到原定值,测定结束后,通过测定电解消耗的电量进行计算 的含量(忽略检测前后溶液体积的变化).下列说法正确的是
的含量(忽略检测前后溶液体积的变化).下列说法正确的是
 的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后,
的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解至
还原,测硫仪便立即自动进行电解至 又回到原定值,测定结束后,通过测定电解消耗的电量进行计算
又回到原定值,测定结束后,通过测定电解消耗的电量进行计算 的含量(忽略检测前后溶液体积的变化).下列说法正确的是
的含量(忽略检测前后溶液体积的变化).下列说法正确的是
| A.X极应该和电源的负极相连 |
B.电解时消耗的电量越多,待测气体中 的含量越低 的含量越低 |
C.当通入 时溶液中 时溶液中 向X极移动 向X极移动 |
D.若有 被处理,则电解质溶液中约增加 被处理,则电解质溶液中约增加 |
您最近一年使用:0次
名校
解题方法
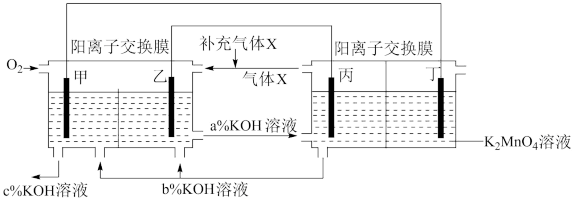
9 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为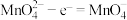 |
C.KOH溶液的质量分数: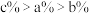 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
670次组卷
|
7卷引用:重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题
重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题
10 . 一种钠硫电池在常温下的工作原理如图所示(以 和
和 的四乙二醇二甲基醚混合溶液为电解液),下列说法正确的是
的四乙二醇二甲基醚混合溶液为电解液),下列说法正确的是

 和
和 的四乙二醇二甲基醚混合溶液为电解液),下列说法正确的是
的四乙二醇二甲基醚混合溶液为电解液),下列说法正确的是
A.电极甲的材料是金属钠,电极乙的材料是 |
B.该电池放电时,电极甲上存在电极反应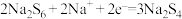 |
C.放电程度越大,电解液中 的含量越少 的含量越少 |
D.可用 的水溶液作为电解液来提高该电池的工作效率 的水溶液作为电解液来提高该电池的工作效率 |
您最近一年使用:0次
2023-07-07更新
|
314次组卷
|
2卷引用:湖南省长沙市长郡中学2022-2023学年高二下学期期末考试化学试题



