名校
解题方法
1 . 有机物电极材料具有来源丰富、可降解等优点,一种负极材料为固态聚酰亚胺-水系二次电池的结构如图所示。下列说法正确的是
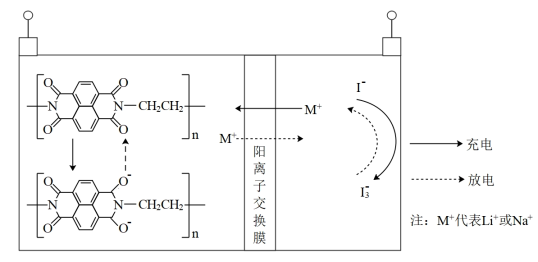

| A.充电时有机电极发生了氧化反应 |
B.将 由 由 换成 换成 ,电池的比能量会下降 ,电池的比能量会下降 |
C.充电时每转移 ,右室离子数目减少 ,右室离子数目减少 |
D.放电时负极电极反应为: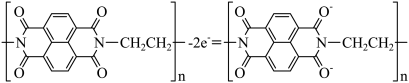 |
您最近一年使用:0次
名校
解题方法
2 . 2019年诺贝尔化学奖授予锂离子电池的发明者, 是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、
是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、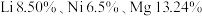 )制备
)制备 ,并用其制备
,并用其制备 。部分工艺流程如图(该流程可能造成水体砷污染):
。部分工艺流程如图(该流程可能造成水体砷污染):
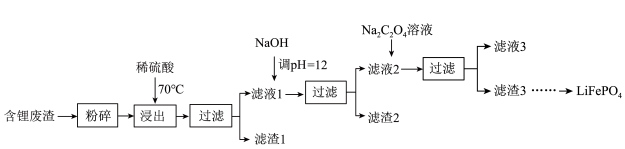
已知:室温下测得滤液1、滤液2中部分离子的浓度如下表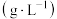 :
:
Ⅰ.制备
(1)处理废渣时粉碎的作用是____________________________________ 。
(2)滤渣2的主要成分(填化学式)_________________ ,滤液3可回收的物质是___________ 。
(3)下列有关说法正确的是__________ 。
A. 中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
C.室温下 的
的 等于
等于 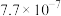
(4)将 和
和 置于高温下反应,生成
置于高温下反应,生成 和一种温室气体,该反应的化学方程式是
和一种温室气体,该反应的化学方程式是__________________ 。
II、如图是一个电化学过程的示意图。请回答下列问题:
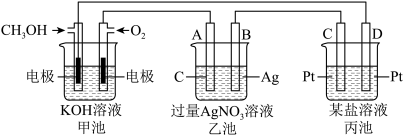
(5)写出通入CH3OH的电极的电极反应式____________ 。
(6)乙池中反应的化学方程式___________ 。
 是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、
是锂离子电池的正极材料。用含锂废渣(主要元素的含量:As 5.40%、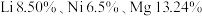 )制备
)制备 ,并用其制备
,并用其制备 。部分工艺流程如图(该流程可能造成水体砷污染):
。部分工艺流程如图(该流程可能造成水体砷污染):
已知:室温下测得滤液1、滤液2中部分离子的浓度如下表
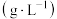 :
: |  |  | |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 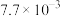 | 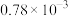 |
Ⅰ.制备

(1)处理废渣时粉碎的作用是
(2)滤渣2的主要成分(填化学式)
(3)下列有关说法正确的是
A.
 中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸
中铁元素的化合价为+2价 B.流程中可以直接循环利用的物质为稀硫酸C.室温下
 的
的 等于
等于 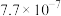
(4)将
 和
和 置于高温下反应,生成
置于高温下反应,生成 和一种温室气体,该反应的化学方程式是
和一种温室气体,该反应的化学方程式是II、如图是一个电化学过程的示意图。请回答下列问题:

(5)写出通入CH3OH的电极的电极反应式
(6)乙池中反应的化学方程式
您最近一年使用:0次
3 . 2020年9月中国明确提出“双碳”目标。因此,研发 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的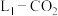 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: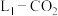 电池中:
电池中:
(1) Li为______ (填“正”或“负”)极,正极的电极反应为____________ 。
(2)研究表明, 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为____________
I.
II._________________
III.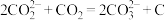
IV.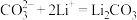
II、利用 电池作为图2装置的中源。
电池作为图2装置的中源。
(3) 片连接
片连接 电池的
电池的_______ (填“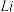 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,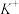 通过阳离子交换膜由
通过阳离子交换膜由_______ (填“左室移向右室”或“右室移向左室”),阴极发生的电极反应为_______ 。
(4)电解一段时间后, 电池中生成
电池中生成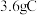 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为_______ L。
 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的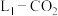 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: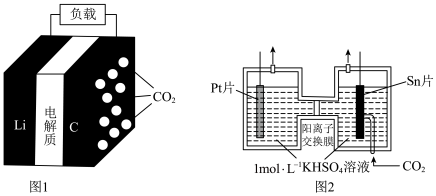
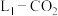 电池中:
电池中:(1) Li为
(2)研究表明,
 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为I.

II._________________
III.
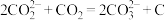
IV.
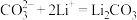
II、利用
 电池作为图2装置的中源。
电池作为图2装置的中源。(3)
 片连接
片连接 电池的
电池的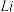 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,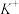 通过阳离子交换膜由
通过阳离子交换膜由(4)电解一段时间后,
 电池中生成
电池中生成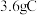 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
I.某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
资料:单质硫可溶于过量硫化钠溶液,Na2S2溶液呈淡黄色。
(1)根据实验可知,Na2S具有_______ 性。
(2)甲同学预测实验I中S2- 被氧化成SO 。
。
①根据实验现象,乙同学认为甲的预测不合理,理由是_______ 。
②乙同学取实验I中少量溶液进行实验,检测到有SO ,得出S2- 被氧化成SO
,得出S2- 被氧化成SO 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是_______ 。
③同学们经讨论后,设计了如下实验,证实该条件下MnO 的确可以将S2- 氧化成SO
的确可以将S2- 氧化成SO 。
。
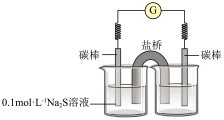
右侧烧杯中的溶液是____ ;连通后电流计指针偏转,一段时间后,____ (填操作和现象)。
II.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:
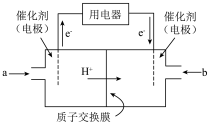
通入a物质的电极是原电池的_______ (填“正”或“负”)极,其电极反应式为_______ 。
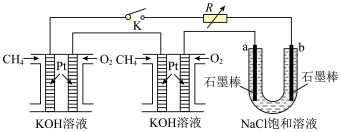
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为_______ (法拉第常数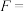
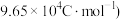 ,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为_______ (假设反应后溶液体积不变)。
I.某小组研究Na2S溶液与KMnO4溶液反应,探究过程如下。
| 实验序号 | I | Ⅱ |
| 实验过程 | 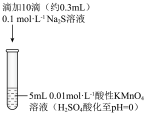 |  |
| 实验现象 | 紫色变浅(pH>1),生成棕褐色沉 淀(MnO2) | 溶液呈淡黄色(pH≈8),生成浅粉色沉淀(MnS) |
资料:单质硫可溶于过量硫化钠溶液,Na2S2溶液呈淡黄色。
(1)根据实验可知,Na2S具有
(2)甲同学预测实验I中S2- 被氧化成SO
 。
。①根据实验现象,乙同学认为甲的预测不合理,理由是
②乙同学取实验I中少量溶液进行实验,检测到有SO
 ,得出S2- 被氧化成SO
,得出S2- 被氧化成SO 的结论,丙同学否定了该结论,理由是
的结论,丙同学否定了该结论,理由是③同学们经讨论后,设计了如下实验,证实该条件下MnO
 的确可以将S2- 氧化成SO
的确可以将S2- 氧化成SO 。
。
右侧烧杯中的溶液是
II.甲烷和甲醇的燃料电池具有广阔的开发和应用前景。
(3)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC的工作原理如图所示:

通入a物质的电极是原电池的
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800mL。闭合K后,若每个电池中甲烷通入量为0.224L(标准状况),且反应完全,则理论上通过电解池的电量为
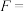
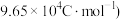 ,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
,若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为
您最近一年使用:0次
名校
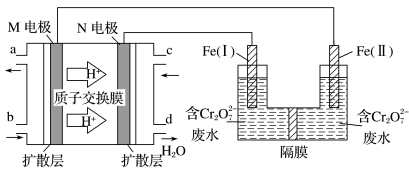
5 . 用甲醇燃料电池作电源,用铁作电极电解含Cr2O 的酸性废水,处理过程发生反应:Cr2O
的酸性废水,处理过程发生反应:Cr2O +6 Fe2++14H+=2Cr3++6Fe3++7H2O,最终可将Cr3+转化成Cr(OH)3沉淀而除去,装置如下图。下列说法正确的是
+6 Fe2++14H+=2Cr3++6Fe3++7H2O,最终可将Cr3+转化成Cr(OH)3沉淀而除去,装置如下图。下列说法正确的是
 的酸性废水,处理过程发生反应:Cr2O
的酸性废水,处理过程发生反应:Cr2O +6 Fe2++14H+=2Cr3++6Fe3++7H2O,最终可将Cr3+转化成Cr(OH)3沉淀而除去,装置如下图。下列说法正确的是
+6 Fe2++14H+=2Cr3++6Fe3++7H2O,最终可将Cr3+转化成Cr(OH)3沉淀而除去,装置如下图。下列说法正确的是
| A.Fe(Ⅱ)为阳极 |
B.M电极的电极反应式为CH3OH+8OH--6e-=CO +6H2O +6H2O |
| C.电解一段时间后,在Fe(Ⅰ)极附近有沉淀析出 |
D.电路中每转移6mol电子,最多有1molCr2O 被还原 被还原 |
您最近一年使用:0次
解题方法
6 . Co是磁性合金的重要材料,也是维生素重要的组成元素。工业上可用如下装置制取单质Co并获得副产品盐酸(A、B均为离子交换膜)。下列说法正确的是
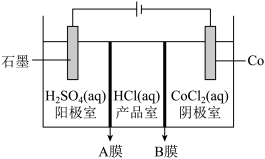

| A.A为阴离子交换膜,B为阳离子交换膜 |
| B.若去掉膜A,石墨电极的电极反应不变 |
C.当电路中转移2mol电子时,阳极产生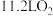 |
D.若产品室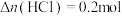 ,阴极溶液质量减少13g ,阴极溶液质量减少13g |
您最近一年使用:0次
7 . 我国科学家研发了一种水系可逆Al-CO2电池,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充电、放电时,复合膜层间的H2O解离成H+和OH—,工作原理如图所示。下列说法正确的是
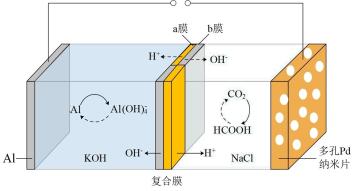

| A.a膜是阴离子交换膜,b膜是阳离子交换膜 |
B.放电时负极的电极反应式为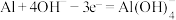 |
| C.放电时多孔Pd纳米片附近pH不变 |
| D.充电时Al与外接直流电源正极相连,将电能转化为化学能 |
您最近一年使用:0次
解题方法
8 . 磷酸铁锂 电池是一种高效、环保的新型电池。电池工作时的总反应为
电池是一种高效、环保的新型电池。电池工作时的总反应为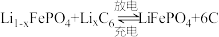 (C为石墨,
(C为石墨,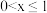 ),则正极上发生反应的物质是
),则正极上发生反应的物质是
 电池是一种高效、环保的新型电池。电池工作时的总反应为
电池是一种高效、环保的新型电池。电池工作时的总反应为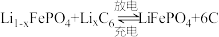 (C为石墨,
(C为石墨,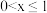 ),则正极上发生反应的物质是
),则正极上发生反应的物质是A. | B. | C. | D.C |
您最近一年使用:0次
解题方法
9 . 随着科学技术的发展,电化学已经渗透到我们生产生活的方方面面,几种生产生活中对电化学的应用的原理模型图如图所示:

回答下列问题:
(1)模型图甲~戊中包含电解池装置的是____________ 。
(2)一种电化学制备 的装置如图甲所示,其中质子传输陶瓷所起的作用是
的装置如图甲所示,其中质子传输陶瓷所起的作用是____________ ;Pd电极b的电极反应式为____________ 。
(3)我国科学家设计了一种能循环利用人体呼出的 并提供
并提供 的装置(如图乙所示),总反应为
的装置(如图乙所示),总反应为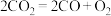 。该装置的能量转化模式(涉及三种形式的能量转化)为
。该装置的能量转化模式(涉及三种形式的能量转化)为____________ ; 移向
移向____________ (填“X”或“Y”)电极,该电极的产物为____________ (填化学式)。
(4)如图丙所示,若a、b电极材料选择粗铜和纯铜。则该装置可应用于工业___________ ;若a、b电极选用惰性电极,电解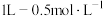 硫酸铜溶液,当a电极产生2.24L(标准状况)气体时,停止电解,要使电解质溶液恢复到电解前的状态,则可加入
硫酸铜溶液,当a电极产生2.24L(标准状况)气体时,停止电解,要使电解质溶液恢复到电解前的状态,则可加入___________ mol___________ (填化学式)。

回答下列问题:
(1)模型图甲~戊中包含电解池装置的是
(2)一种电化学制备
 的装置如图甲所示,其中质子传输陶瓷所起的作用是
的装置如图甲所示,其中质子传输陶瓷所起的作用是(3)我国科学家设计了一种能循环利用人体呼出的
 并提供
并提供 的装置(如图乙所示),总反应为
的装置(如图乙所示),总反应为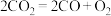 。该装置的能量转化模式(涉及三种形式的能量转化)为
。该装置的能量转化模式(涉及三种形式的能量转化)为 移向
移向(4)如图丙所示,若a、b电极材料选择粗铜和纯铜。则该装置可应用于工业
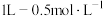 硫酸铜溶液,当a电极产生2.24L(标准状况)气体时,停止电解,要使电解质溶液恢复到电解前的状态,则可加入
硫酸铜溶液,当a电极产生2.24L(标准状况)气体时,停止电解,要使电解质溶液恢复到电解前的状态,则可加入
您最近一年使用:0次
解题方法
10 . 一种无需离子交换膜的氮流电池的工作原理如图所示。下列说法正确的是
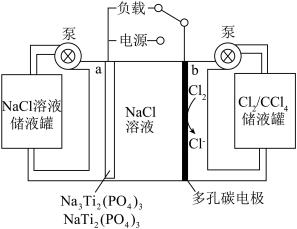

| A.充电时,a极接电源正极 |
| B.充电时,左侧NaCl溶液储液罐中溶液的pH减小 |
| C.放电时,a极的电极反应为Na3Ti2(PO4)3-2e-=NaTi2(PO4)3+2Na+ |
| D.放电时,有1molCl2参与反应,理论上NaCl溶液增重71g |
您最近一年使用:0次



