名校
解题方法
1 . 用铅蓄电池电解 溶液,a、b电极均为石墨。已知铅蓄电池的总反应为
溶液,a、b电极均为石墨。已知铅蓄电池的总反应为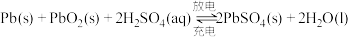 ,通电时a电极质量增加,回答下列问题:
,通电时a电极质量增加,回答下列问题:

(1)①乙中a极是该电池的___________ (填“阳极”或“阴极”)。
②甲中Y电极的电极反应式为___________ 。
(2)乙中装有 溶液,工作一段时间后,停止通电,若甲中放电时共转移
溶液,工作一段时间后,停止通电,若甲中放电时共转移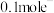 ,通电后乙中发生反应的总反应方程式为
,通电后乙中发生反应的总反应方程式为___________ ,欲使溶液恢复到起始状态,可向溶液中加入___________ (填字母),质量为___________ 。
A.Ag B. C.
C.
(3)①欲用丙装置防止金属铁被腐蚀,则金属铁应为___________ (填“c”或“d”)极。
②欲用丙装置精炼铜,则粗铜应为___________ (填“c”或“d”)极。
 溶液,a、b电极均为石墨。已知铅蓄电池的总反应为
溶液,a、b电极均为石墨。已知铅蓄电池的总反应为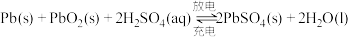 ,通电时a电极质量增加,回答下列问题:
,通电时a电极质量增加,回答下列问题:
(1)①乙中a极是该电池的
②甲中Y电极的电极反应式为
(2)乙中装有
 溶液,工作一段时间后,停止通电,若甲中放电时共转移
溶液,工作一段时间后,停止通电,若甲中放电时共转移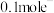 ,通电后乙中发生反应的总反应方程式为
,通电后乙中发生反应的总反应方程式为A.Ag B.
 C.
C.
(3)①欲用丙装置防止金属铁被腐蚀,则金属铁应为
②欲用丙装置精炼铜,则粗铜应为
您最近一年使用:0次
2 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。
(1)已知:
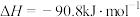 。该反应的熵变
。该反应的熵变
___________ 0(填“>”“<”“=”),该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)。
(2)将 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一,所涉及的反应方程式为:
资源化利用的有效途径之一,所涉及的反应方程式为:
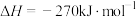 ,几种化学键的键能如表所示:
,几种化学键的键能如表所示:
则a=___________ 。
(3)利用电化学原理,将 还原为
还原为 ,装置如图所示:
,装置如图所示:
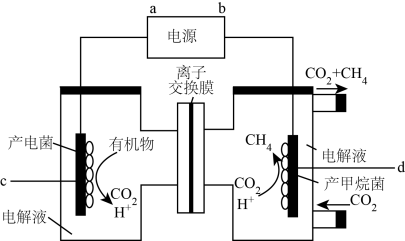
①d电极的电极反应式为___________ 。
②若电源采用 ―
― ―KOH清洁燃料电池,当消耗0.2mol燃料
―KOH清洁燃料电池,当消耗0.2mol燃料 时,离子交换膜中通过
时,离子交换膜中通过___________ mol ,该清洁燃料电池中的a极的电极反应式为
,该清洁燃料电池中的a极的电极反应式为___________ 。
(4)T℃时,向容积为2L的恒容密闭容器中通入3.0mol 和6.5mol
和6.5mol ,发生反应:
,发生反应:
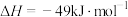 ,5分钟时反应达到平衡,
,5分钟时反应达到平衡, 的转化率为50%,回答下列问题:
的转化率为50%,回答下列问题:
①在0~5min内容器中
___________ 。
②该温度下上述反应的平衡常数
___________ 。
③下列措施能增大反应速率的是___________ (填字母)。
A.升高温度 B.扩大容器体积 C.充入一定量氦气 D.加入催化
(1)已知:

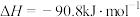 。该反应的熵变
。该反应的熵变
(2)将
 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一,所涉及的反应方程式为:
资源化利用的有效途径之一,所涉及的反应方程式为:
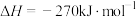 ,几种化学键的键能如表所示:
,几种化学键的键能如表所示:| 化学键 | C―H | H―H | O―H | C=O |
键能/ | 414 | 436 | 464 | a |
(3)利用电化学原理,将
 还原为
还原为 ,装置如图所示:
,装置如图所示:
①d电极的电极反应式为
②若电源采用
 ―
― ―KOH清洁燃料电池,当消耗0.2mol燃料
―KOH清洁燃料电池,当消耗0.2mol燃料 时,离子交换膜中通过
时,离子交换膜中通过 ,该清洁燃料电池中的a极的电极反应式为
,该清洁燃料电池中的a极的电极反应式为(4)T℃时,向容积为2L的恒容密闭容器中通入3.0mol
 和6.5mol
和6.5mol ,发生反应:
,发生反应:
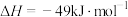 ,5分钟时反应达到平衡,
,5分钟时反应达到平衡, 的转化率为50%,回答下列问题:
的转化率为50%,回答下列问题:①在0~5min内容器中

②该温度下上述反应的平衡常数

③下列措施能增大反应速率的是
A.升高温度 B.扩大容器体积 C.充入一定量氦气 D.加入催化
您最近一年使用:0次
真题
名校
3 . 一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由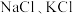 和
和 形成熔点为
形成熔点为 的共熔物),其中氯铝酸根
的共熔物),其中氯铝酸根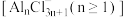 起到结合或释放
起到结合或释放 的作用。电池总反应:
的作用。电池总反应: 。下列说法
。下列说法错误 的是
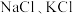 和
和 形成熔点为
形成熔点为 的共熔物),其中氯铝酸根
的共熔物),其中氯铝酸根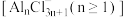 起到结合或释放
起到结合或释放 的作用。电池总反应:
的作用。电池总反应: 。下列说法
。下列说法
A. 含 含 个 个 键 键 |
B. 中同时连接2个 中同时连接2个 原子的 原子的 原子有 原子有 个 个 |
C.充电时,再生 单质至少转移 单质至少转移 电子 电子 |
D.放电时间越长,负极附近熔融盐中n值小的 浓度越高 浓度越高 |
您最近一年使用:0次
2023-11-16更新
|
3333次组卷
|
3卷引用:2023年福建省高考化学试卷
解题方法
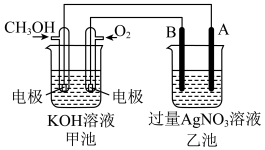
4 . 某电化学原理的示意图如图。填写下列空白: 的电极为
的电极为___________ 极,通入 的电极上发生的电极反应为
的电极上发生的电极反应为___________ ;工作过程中,甲池溶液的碱性会___________ (填“增强”、“减弱”或“不变”,下同)。若将甲池中的 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会___________ 。
(2)若乙池中A为石墨电极,则A作___________ 极,该电极的电极反应式为___________ ;若乙池中A为铁电极,当铁电极的质量增加 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为___________ L。
(3)若将乙池设计为电解精炼铜的装置,则___________ (填“A”或“B”,下同)极为粗铜;若将乙池改为电镀装置,则___________ 极为待镀金属制品。
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为___________  。
。
 的电极为
的电极为 的电极上发生的电极反应为
的电极上发生的电极反应为 溶液换成稀硫酸,工作过程中,甲池溶液的酸性会
溶液换成稀硫酸,工作过程中,甲池溶液的酸性会(2)若乙池中A为石墨电极,则A作
 时,理论上甲池中消耗的氧气在标准状况下的体积为
时,理论上甲池中消耗的氧气在标准状况下的体积为(3)若将乙池设计为电解精炼铜的装置,则
(4)若将乙池中的硝酸银溶液换为硫酸铜溶液,通电一段时间后,向所得溶液中加入
 碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为
碱式碳酸铜后恰好恢复至电解前的状态,则电解过程中转移的电子数目为 。
。
您最近一年使用:0次
2023-11-13更新
|
471次组卷
|
2卷引用:福建省泉州市2023-2024学年高二上学期期中考试化学试题
名校
解题方法
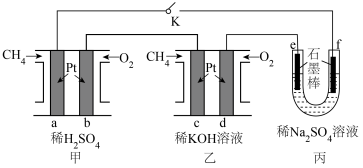
5 . 利用甲烷( )燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
)燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
 )燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
)燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
| A.甲装置为原电池,乙装置、丙装置均为电解池 |
B.b电极的电极反应式为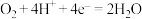 |
C.若甲、乙共通入1 mol  ,向丙加入72 g ,向丙加入72 g  可使丙装置恢复原浓度 可使丙装置恢复原浓度 |
| D.当K闭合时,整个电路中电子的流动方向为a→f,e→d,c→b |
您最近一年使用:0次
2023-10-28更新
|
71次组卷
|
2卷引用:福建省永安市第九中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
6 . 汽车尾气中氮氧化合物、碳氧化合物的处理会污染环境。
(1)①已知:6g碳完全被氧气氧化放出197kJ的热量,则该反应的热化学方程式可表示为:___________ 。
②
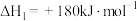

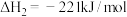
则反应

___________ 。
(2)运用电化学方法可以进行NO的消除和CO含量检测。
①用电化学气敏传感器测定汽车尾气中CO含量,原理如图所示。A电极为___________ 极,电极反应式为___________ 。当O2消耗1.12L(标准状况下),电路中理论上过的电子数目为___________ 。

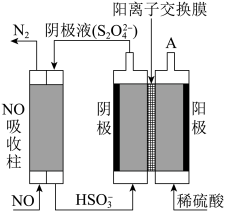
②间接电解法除NO。其原理如图所示,从A中出来的气体是___________ ,电解池阴极的电极反应式___________ 。用离子方程式表示吸收柱中除去NO的原理___________ 。
(1)①已知:6g碳完全被氧气氧化放出197kJ的热量,则该反应的热化学方程式可表示为:
②

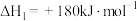

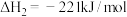
则反应


(2)运用电化学方法可以进行NO的消除和CO含量检测。
①用电化学气敏传感器测定汽车尾气中CO含量,原理如图所示。A电极为

②间接电解法除NO。其原理如图所示,从A中出来的气体是

您最近一年使用:0次
名校
解题方法
7 . 请回答下列问题:
(1)工业上以 和
和 为原料在一定温度和压强下合成尿素。
为原料在一定温度和压强下合成尿素。
反应分两步:i. 和
和 生成
生成 ;ii.
;ii. 分解生成尿素。
分解生成尿素。
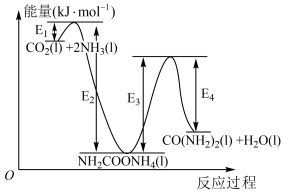
结合反应过程中能量变化示意图,合成尿素总反应的 为
为___________ 。(用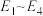 列式表示)
列式表示)
(2)根据表格计算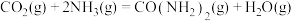

___________ 。
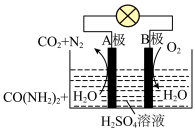
(3)尿素 燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如下图所示,正极反应为
燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如下图所示,正极反应为___________ 。
(4)近年研究发现,电催化 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
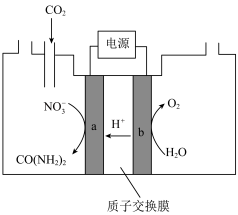
①电极b是电解池的___________ 极。
②尿素分子中,C元素的价态为___________ 。电解过程中生成尿素的电极反应为___________ 。
(5)以石墨为阳极、铁为阴极电解含 废水可用于去除
废水可用于去除 。电解过程中各种含氮微粒的浓度、溶液的pH与时间的关系如图所示。
。电解过程中各种含氮微粒的浓度、溶液的pH与时间的关系如图所示。

①0~1 min时,阴极发生的主要电极反应方程式为___________ 。
②若向废水中加入一定量的NaCl,则电解后的废水中 几乎完全转化为
几乎完全转化为 ,原因是
,原因是___________ 。
(1)工业上以
 和
和 为原料在一定温度和压强下合成尿素。
为原料在一定温度和压强下合成尿素。反应分两步:i.
 和
和 生成
生成 ;ii.
;ii. 分解生成尿素。
分解生成尿素。
结合反应过程中能量变化示意图,合成尿素总反应的
 为
为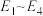 列式表示)
列式表示)(2)根据表格计算
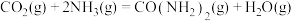

| 化学键 |  |  |  |  |
键能( ) ) | 389 | 728 | 305 | 464 |
(3)尿素
 燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如下图所示,正极反应为
燃料电池可直接去除城市废水中的尿素,既能产生净化水,又能发电。其装置如下图所示,正极反应为
(4)近年研究发现,电催化
 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
①电极b是电解池的
②尿素分子中,C元素的价态为
(5)以石墨为阳极、铁为阴极电解含
 废水可用于去除
废水可用于去除 。电解过程中各种含氮微粒的浓度、溶液的pH与时间的关系如图所示。
。电解过程中各种含氮微粒的浓度、溶液的pH与时间的关系如图所示。
①0~1 min时,阴极发生的主要电极反应方程式为
②若向废水中加入一定量的NaCl,则电解后的废水中
 几乎完全转化为
几乎完全转化为 ,原因是
,原因是
您最近一年使用:0次
名校
8 . 请回答下列问题:
(1)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,电极A的反应为___________ 。将该电池连接两惰性电极,用于电解 的
的 溶液,当原电池中消耗
溶液,当原电池中消耗 的体积在标况下为0.224 L时,电解池中阴极将得到
的体积在标况下为0.224 L时,电解池中阴极将得到___________ g的单质,电解池中 的浓度为
的浓度为___________ (假设溶液体积不变)。为使硝酸银溶液完全复原,可向电解后溶液中加入适量的___________ (填化学式)。

(2)铜锌双液原电池中电极电势Zn___________ Cu(填“高于”、“低于”)。盐桥中琼脂吸附KCl饱和溶液,电池工作时, 将移向
将移向___________ (填“ 溶液”或“
溶液”或“ 溶液”)。
溶液”)。

(3)以 为电池材料设计的一种电化学装置如图。当闭合
为电池材料设计的一种电化学装置如图。当闭合 和
和 、打开
、打开 时,装置处于充电状态;当打开
时,装置处于充电状态;当打开 和
和 、闭合
、闭合 时,装置处于放电状态。放电时,双极膜中间层中的
时,装置处于放电状态。放电时,双极膜中间层中的 解离为
解离为 和
和 并分别向两侧迁移。
并分别向两侧迁移。

①充电时,右侧电解池发生的总反应为___________ 。
②放电时,每消耗 ,理论上有
,理论上有___________  由
由___________ (填“碳锰电极”或“锌电极”或“双极膜”,下同)向___________ 移动。
(1)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,电极A的反应为
 的
的 溶液,当原电池中消耗
溶液,当原电池中消耗 的体积在标况下为0.224 L时,电解池中阴极将得到
的体积在标况下为0.224 L时,电解池中阴极将得到 的浓度为
的浓度为
(2)铜锌双液原电池中电极电势Zn
 将移向
将移向 溶液”或“
溶液”或“ 溶液”)。
溶液”)。
(3)以
 为电池材料设计的一种电化学装置如图。当闭合
为电池材料设计的一种电化学装置如图。当闭合 和
和 、打开
、打开 时,装置处于充电状态;当打开
时,装置处于充电状态;当打开 和
和 、闭合
、闭合 时,装置处于放电状态。放电时,双极膜中间层中的
时,装置处于放电状态。放电时,双极膜中间层中的 解离为
解离为 和
和 并分别向两侧迁移。
并分别向两侧迁移。
①充电时,右侧电解池发生的总反应为
②放电时,每消耗
 ,理论上有
,理论上有 由
由
您最近一年使用:0次
名校
解题方法
9 . 硝化剂可在化学反应中向有机化合物中引入硝基、硝酸酯基 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法不正确 的是
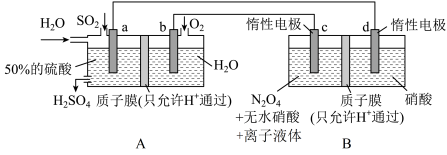
 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法
A.装置 可将电能转化为化学能 可将电能转化为化学能 |
B.装置 中H从a极区迁移到b极区 中H从a极区迁移到b极区 |
C.c电极表面生成 ,电极反应式为: ,电极反应式为: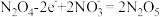 |
D.反应过程中 装置d区 装置d区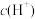 保持不变 保持不变 |
您最近一年使用:0次
2023-10-13更新
|
409次组卷
|
2卷引用:福建省泉州第一中学2023-2024学年高三上学期10月月考化学试题
名校
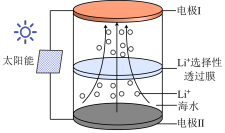
10 . 我国科学家经过研究发明了以下装置从海水中提取锂单质,其工作原理如图所示。该装置运行期间电极Ⅱ上产生 和气体X。下列说法错误的是
和气体X。下列说法错误的是
 和气体X。下列说法错误的是
和气体X。下列说法错误的是
| A.该装置实现了“太阳能→电能→化学能”的转化 |
| B.电极Ⅰ连接太阳能电池的负极 |
| C.工作时,电极Ⅱ附近溶液的pH增大 |
| D.实验室检验气体X可用湿润的淀粉-KI试纸 |
您最近一年使用:0次
2023-08-31更新
|
831次组卷
|
5卷引用:福建省福州市2023-2024学年高三上学期第一次质量检测化学试题
福建省福州市2023-2024学年高三上学期第一次质量检测化学试题福建省莆田第一中学2023-2024学年高二上学期期中考试化学试题福建省福州第二中学2023-2024学年高二上学期10月月考化学试卷题(已下线)考点2 原电池 新型电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)



