解题方法
1 . 某小组探究电解氯化铜的产物,设计如下实验(以石墨为电极):
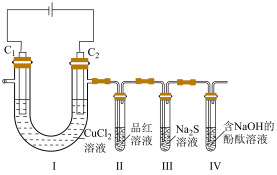
实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是

实验中观察到Ⅱ中品红溶液褪色,Ⅲ中产生浅黄色固体,Ⅳ中溶液褪色。下列叙述错误的是
| A.根据Ⅲ试管中现象可知,氯的非金属性比硫强 |
B.一段时间后, 极附着一层红色固体物质 极附着一层红色固体物质 |
| C.上述实验中,试管Ⅱ和Ⅳ褪色原理不相同 |
| D.如果用铜极替代石墨也能得到与上述实验完全相同的实验现象 |
您最近一年使用:0次
2023-10-08更新
|
87次组卷
|
2卷引用:河北省秦皇岛市青龙满族自治县2校联考2023-2024学年高一上学期12月月考化学试题
2 . 液流电池是电化学储能领域的研究热点,其电解液置于电堆外部,在循环泵的推动下流经电堆,实现化学能与电能的转换。下图是全钒液流电池的结构及工作原理示意图。

下列说法正确的是

下列说法正确的是
| A.充电时M极应与电源的负极相连 |
B.充电时总反应: |
C.放电时每转移 ,有 ,有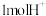 通过交换膜移向N极区 通过交换膜移向N极区 |
D.放电时正极反应式: |
您最近一年使用:0次
名校
解题方法
3 . 化学反应中的能量变化是中学化学中重要组成部分,回答下列相关问题。
(1)二甲醚( )是一种新型燃料,应用前景广阔。
)是一种新型燃料,应用前景广阔。 二甲醚(l)完全燃烧生成
二甲醚(l)完全燃烧生成 和液态水时放出
和液态水时放出 热量。写出二甲醚(l)完全燃烧生成
热量。写出二甲醚(l)完全燃烧生成 和液态水的热化学方程式:
和液态水的热化学方程式:___________ 。
(2)碳(s)在氧气供应不充足时,生成 的同时还有部分生成
的同时还有部分生成 ,因此无法通过实验直接测得反应
,因此无法通过实验直接测得反应 的
的 ,但可以设计实验利用盖斯定律计算出该反应的
,但可以设计实验利用盖斯定律计算出该反应的 ,实验时需要测得的数据有
,实验时需要测得的数据有___________ 。
(3)某同学用铜片、银片、 溶液、
溶液、 溶液、导线和盐桥(装有琼脂—
溶液、导线和盐桥(装有琼脂— 的U形管)设计成一个原电池,装置如图。下列判断中正确的是___________(填标号)。
的U形管)设计成一个原电池,装置如图。下列判断中正确的是___________(填标号)。

(4)甲烷燃料电池用于电解的装置如图所示:
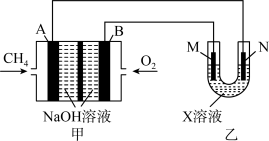
①B电极作___________ (填“正极”或“负极”);A电极上发生的电极反应为___________ 。
②若乙装置用于铁上镀铜,则X的化学式为___________ 。
③若乙装置用于金属铁的防护,应将金属铁置于___________ (填“M”或“N”)极。
(1)二甲醚(
 )是一种新型燃料,应用前景广阔。
)是一种新型燃料,应用前景广阔。 二甲醚(l)完全燃烧生成
二甲醚(l)完全燃烧生成 和液态水时放出
和液态水时放出 热量。写出二甲醚(l)完全燃烧生成
热量。写出二甲醚(l)完全燃烧生成 和液态水的热化学方程式:
和液态水的热化学方程式:(2)碳(s)在氧气供应不充足时,生成
 的同时还有部分生成
的同时还有部分生成 ,因此无法通过实验直接测得反应
,因此无法通过实验直接测得反应 的
的 ,但可以设计实验利用盖斯定律计算出该反应的
,但可以设计实验利用盖斯定律计算出该反应的 ,实验时需要测得的数据有
,实验时需要测得的数据有(3)某同学用铜片、银片、
 溶液、
溶液、 溶液、导线和盐桥(装有琼脂—
溶液、导线和盐桥(装有琼脂— 的U形管)设计成一个原电池,装置如图。下列判断中正确的是___________(填标号)。
的U形管)设计成一个原电池,装置如图。下列判断中正确的是___________(填标号)。
A.实验过程中,左侧烧杯中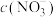 变大 变大 |
| B.若用U形铜代替盐桥,装置中无电流产生 |
| C.若用U形铜代替盐桥,则左池中电能转化成化学能,右池中化学能转化成电能 |
| D.若用U形铜代替盐桥,一段时间之后U形铜的质量减小 |

①B电极作
②若乙装置用于铁上镀铜,则X的化学式为
③若乙装置用于金属铁的防护,应将金属铁置于
您最近一年使用:0次
4 . 利用甲醇燃料电池为电源进行电解的实验装置如下图所示,电极a和b都是石墨电极。该装置工作一段时间后,a电极没有气体放出,那么在这段时间内,下列说法正确的是


| A.a电极作电解池的阳极 |
B.燃料电池工作时,负极反应方程式为 |
C.硫酸铜溶液中 浓度减小,若使 浓度减小,若使 的浓度恢复原状可加入CuCO3 的浓度恢复原状可加入CuCO3 |
| D.同温同压下b电极产生的气体与电池中消耗甲醇的物质的量之比为3:1 |
您最近一年使用:0次
解题方法
5 . 如图是工业制钠电解槽的示意图,下列选项错误的是
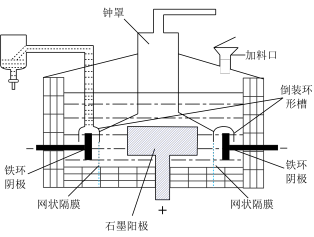

A. 在阴极上析出 在阴极上析出 |
B.网状隔膜用于防止生成的 和Na相互反应 和Na相互反应 |
C.理论上,每转移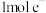 ,生成 ,生成 |
| D.若用串联的铅酸电池组电解氯化钠,则PbO2/Pt极应接石墨极 |
您最近一年使用:0次
名校
解题方法
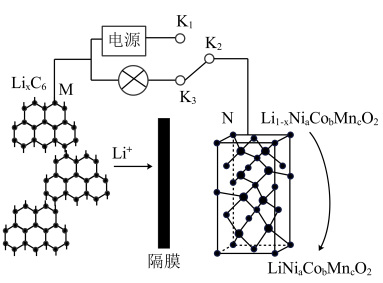
6 . 目前的新能源汽车多采用三元锂电池,某三元锂电池工作原理如图所示,该电池离子导体为有机锂盐溶液。
(1)锂离子电池的电极材料为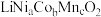 ,当
,当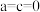 且
且 时该物质中Co元素的化合价为
时该物质中Co元素的化合价为_____________ , 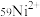 的中子数为31,1mol
的中子数为31,1mol 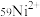 含有电子
含有电子_____________ mol。
(2)连接 、
、 时,N为
时,N为_____________ 极,电极电势高的电极发生_____________ (填“氧化”或“还原”)反应,被氧化的物质为_____________ (填化学式)。
(3)连接 、
、 时,N极的电极反应式为
时,N极的电极反应式为__________________ ,当外电路通过0.1mol电子时,通过隔膜的 质量为
质量为______ g。
(1)锂离子电池的电极材料为
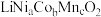 ,当
,当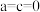 且
且 时该物质中Co元素的化合价为
时该物质中Co元素的化合价为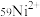 的中子数为31,1mol
的中子数为31,1mol 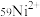 含有电子
含有电子(2)连接
 、
、 时,N为
时,N为(3)连接
 、
、 时,N极的电极反应式为
时,N极的电极反应式为 质量为
质量为
您最近一年使用:0次
2023-05-07更新
|
227次组卷
|
2卷引用:山东省潍坊市2022-2023学年高一下学期期中考试化学试题
名校
7 . 锂离子电池是目前手机、笔记本电脑等现代数码产品中应用最广泛的电池,它主要依靠锂离子在正极和负极之间移动来工作。典型的锰酸锂可充电电池的总反应为:LixC6 + Li1−xMn2O4 C6 + LiMn2O4。其电极分别为层状LiMn2O4和碳材料。下列说法正确的是
C6 + LiMn2O4。其电极分别为层状LiMn2O4和碳材料。下列说法正确的是
 C6 + LiMn2O4。其电极分别为层状LiMn2O4和碳材料。下列说法正确的是
C6 + LiMn2O4。其电极分别为层状LiMn2O4和碳材料。下列说法正确的是| A.放电时层状LiMn2O4电极作正极 |
| B.充电时碳材料应接电源的正极 |
| C.充电时阳极反应为:C6 + xLi+ - xe− = LixC6 |
| D.放电时,Li+嵌入碳材料使该电极增重 |
您最近一年使用:0次
2023-05-03更新
|
381次组卷
|
5卷引用:辽宁省沈阳市第一二〇中学2022-2023学年高一下学期第三次质量监测化学试题
名校
8 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
(1)若用如图1装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为_____ (填化学式),石墨电极的电极反应式为_____ 。将石墨换成铁电极后,电池总反应变为_____ 。
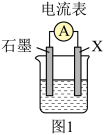
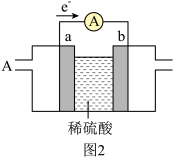
(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图2,a、b均为惰性电极。a为_____ 极,正极的电极反应式为_____ 。当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为_____ 。(保留小数点后1位)。
(3)在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图3所示:

已知H2O在电极附近发生电极反应H2O+2e-=H2+O2-,则CO2发生的电极反应为_____ 。当H2和CO共生成2mol时,生成标准状况下O2的体积为_____ 。
(1)若用如图1装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图2,a、b均为惰性电极。a为

(3)在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图3所示:

已知H2O在电极附近发生电极反应H2O+2e-=H2+O2-,则CO2发生的电极反应为
您最近一年使用:0次
2023-04-29更新
|
236次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
解题方法
9 . 化学电池是新能源和可再生能源的重要组成部分。根据所学知识,回答下列问题:
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
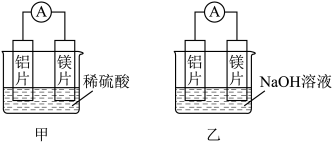
①写出甲中电池总反应的离子方程式:_________ 。
②乙中铝为_________ 极,写出铝电极的电极反应式:_________ 。
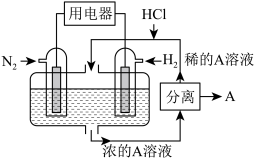
(2)有人设想以 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_________ ,A是_________ (填化学式)。
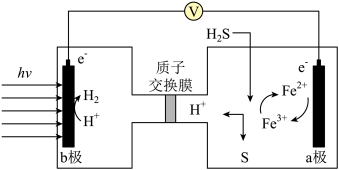
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用_________ (填化学式),该装置的总反应为__________________ ,a极发生的反应为_________ (填“氧化”或“还原”)反应。
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入
 溶液中,实验装置如图所示。
溶液中,实验装置如图所示。
①写出甲中电池总反应的离子方程式:
②乙中铝为
(2)有人设想以
 和
和 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是
(3)我国科学家在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。b极为光能转化为电能的装置,该电极的电极材料可用

您最近一年使用:0次
2023-04-27更新
|
189次组卷
|
2卷引用:河北省邢台市2022-2023学年高一下学期期中考试化学试题
名校
10 . 已知:相同金属在其不同浓度盐溶液中可形成浓差电池。热再生氨电池工作原理如图所示,通入NH3发生反应Cu2++4NH3 [Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
[Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
 [Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
[Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是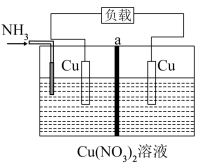
| A.放电、充电过程中,能量主要是在电能与化学能之间转变 |
B.Cu2++4NH3 [Cu(NH3)4]2+正反应为吸热反应 [Cu(NH3)4]2+正反应为吸热反应 |
| C.Cu2+通过中间离子交换膜移向右侧极区 |
| D.放电时,外电路有0.2mol电子通过时,右池溶液质量减少18.8g |
您最近一年使用:0次
2022-06-27更新
|
557次组卷
|
3卷引用:浙江省舟山中学2022-2023学年高一下学期5月月考化学试题



