1 . 下列说法不正确的是
| A.将绿豆大小的钠放入水中,钠在水中的位置、钠的形状都会发生变化 |
| B.可用稀硝酸和KSCN溶液,检验菠菜等食品中的铁元素 |
| C.阿伦尼乌斯的电离模型认为,电解质通电后会电离产生离子 |
D.考古研究中利用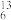 C和 C和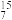 N的测定,分析古代人类的食物结构 N的测定,分析古代人类的食物结构 |
您最近一年使用:0次
解题方法
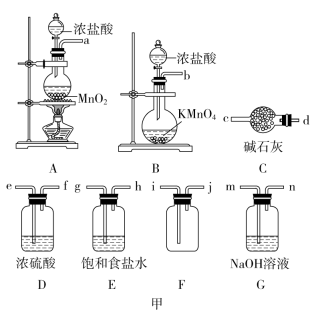
2 . 某同学欲制备干燥洁净的氯气并探究氯气的化学性质:_______ 、装置中盛装浓盐酸的仪器名称是_______ 、装置E的作用是_______ 。
(2)将仪器按顺序连接好后,必须进行的操作是_______ ,书写装置A所发生的离子方程式 _______ 。
(3)已知装置B也可以作为实验室制取了氯气的主要装置,其反应为:___HCl+___KMnO4=___KCl+___MnCl2+___Cl2↑+___H2O。
①配平方程式_______ 。
②若生成标况下6.72L的Cl2则所需要的氧化剂和还原剂的物质的量之比为_______ 。
③若反应消耗15.8gKMnO4,则转移的电子数目为_______ (阿伏加德罗常数用NA表示),生成的氯气在标况下为_______ L。
④该反应中氧化剂、还原剂分别是_______ 、_______ 。
(2)将仪器按顺序连接好后,必须进行的操作是
(3)已知装置B也可以作为实验室制取了氯气的主要装置,其反应为:___HCl+___KMnO4=___KCl+___MnCl2+___Cl2↑+___H2O。
①配平方程式
②若生成标况下6.72L的Cl2则所需要的氧化剂和还原剂的物质的量之比为
③若反应消耗15.8gKMnO4,则转移的电子数目为
④该反应中氧化剂、还原剂分别是
您最近一年使用:0次
解题方法
3 . 回答下列问题
(1)某气体质量mg、摩尔质量为Mg/mol、若阿伏加德罗常数用NA表示,已知:该气体为双原子分子:
①该气体的物质的量为_______ ;
②该气体的分子个数为_______ 、原子个数为 _______ ;
③在标况下该气体所占据的体积为_______ 。
(2)已知在某温度下气体X的分子个数为1.204×1023个,该气体所占据的体积为4L,则该气体在此温度下的Vm为_______ 。
(3)现有一瓶未知浓度的HCl溶液设计实验探究其准确浓度。
①甲同学取了10mlHCl溶液于锥形瓶中,向锥形瓶内滴加了20mL、0.05mol·L-1的NaOH溶液恰好完全反应,则该溶液的浓度为_______ 。
②乙同学取10mLHCl溶液与锥形瓶中,加入足量的铁粉进行反应(假设所有HCl溶液完全反应),收集到的气体在标况下为1.12L,则该溶液浓度为_______ 。
(1)某气体质量mg、摩尔质量为Mg/mol、若阿伏加德罗常数用NA表示,已知:该气体为双原子分子:
①该气体的物质的量为
②该气体的分子个数为
③在标况下该气体所占据的体积为
(2)已知在某温度下气体X的分子个数为1.204×1023个,该气体所占据的体积为4L,则该气体在此温度下的Vm为
(3)现有一瓶未知浓度的HCl溶液设计实验探究其准确浓度。
①甲同学取了10mlHCl溶液于锥形瓶中,向锥形瓶内滴加了20mL、0.05mol·L-1的NaOH溶液恰好完全反应,则该溶液的浓度为
②乙同学取10mLHCl溶液与锥形瓶中,加入足量的铁粉进行反应(假设所有HCl溶液完全反应),收集到的气体在标况下为1.12L,则该溶液浓度为
您最近一年使用:0次
解题方法
4 . 下列说法错误的是
| A.某分散系中分散质微粒直径为2×10-8m,则该分散系可以产生丁达尔效应 |
| B.电解质在水溶液中一定能导电 |
| C.某物质焰色试验呈现黄色,该物质中一定含有钠元素 |
| D.辨别纯碱和小苏打粉末的其中一种方法是加热 |
您最近一年使用:0次
解题方法
5 . 配制一定物质的量浓度的NaCl溶液过程的部分示意图如下:
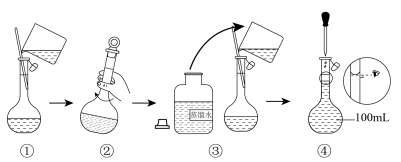
| A.操作①中用玻璃棒引流将NaCl溶液注入100mL容量瓶 |
| B.操作②轻轻摇动容量瓶,使溶液混合均匀 |
| C.操作③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液注入容量瓶 |
| D.操作④若仰视容量瓶上的刻度线,最后配成的溶液中溶质的实际浓度偏大 |
您最近一年使用:0次
解题方法
6 . 下列事实不能用“组成和结构决定性质”来解释的是
| A.常见的一些合金的硬度比其成分金属的大 |
| B.高碳钢、中碳钢和低碳钢的性能有很大差别 |
| C.测试工程师依据组成元素及含量确定不锈钢等级 |
| D.铝和铁是地壳中含量最多的二种金属元素 |
您最近一年使用:0次
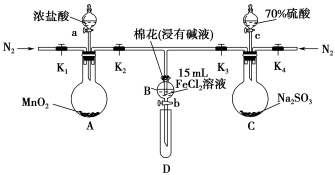
7 . 某化学兴趣小组为验证Cl2、Fe3+、SO2三者氧化性强弱顺序,按照如图所示的装置(夹持装置和A中加热装置已省略)进行探究。
 .打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
.打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
 .打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
.打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
 .打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
.打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
 .打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
.打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
 .另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
.另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
回答下列问题:
(1)实验开始前需进行的操作是___________ 。
(2)步骤 中通入N2的目的是
中通入N2的目的是___________ 。
(3)步骤 中溶液变黄的原因是
中溶液变黄的原因是___________ 。
(4)步骤 ,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由
,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由___________ (请用离子方程式表示)。
(5)步骤 和步骤
和步骤 的检验结果如下:
的检验结果如下:
则Cl2、Fe3+、SO2三者氧化性强弱顺序为 ___________ 。
(6)请设计实验方案检验E试管溶液中的SO :
:___________ 。
 .打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。
.打开止水夹K1、K2、K3、K4,通入N2一段时间,关闭K1、K3、K4,向B中加入15 mL新制FeCl2溶液。 .打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。
.打开活塞a,向容器A中滴加适量浓盐酸,加热A,当B中溶液变黄时,停止加热,关闭K2。 .打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。
.打开活塞b,待约2 mL溶液流入D试管,关闭活塞b,检验D试管溶液中的阳离子。 .打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。
.打开K3和活塞c,向C中滴加70%硫酸,一段时间后关闭K3。 .另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。
.另取试管E,打开活塞b,待约2 mL溶液流入E试管,关闭活塞b,检验E试管溶液中的阴离子。回答下列问题:
(1)实验开始前需进行的操作是
(2)步骤
 中通入N2的目的是
中通入N2的目的是(3)步骤
 中溶液变黄的原因是
中溶液变黄的原因是(4)步骤
 ,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由
,检验D试管溶液中是否含有Fe2+,不能选用酸性KMnO4溶液的理由(5)步骤
 和步骤
和步骤 的检验结果如下:
的检验结果如下:步骤 ,D试管溶液中含有的阳离子 ,D试管溶液中含有的阳离子 | 既有Fe3+,又有Fe2+ |
步骤 ,E试管溶液中含有的阴离子 ,E试管溶液中含有的阴离子 | 有SO |
(6)请设计实验方案检验E试管溶液中的SO
 :
:
您最近一年使用:0次
解题方法
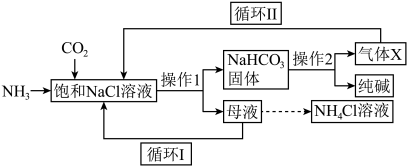
8 . 我国化学家侯德榜先生提出的联合制碱法得到世界各国的认可,主要工业流程可简要表示如图:
(1)“操作1”的名称:___________ 。
(2)“循环 ”的物质为:
”的物质为:___________ 。
(3)“操作2”的化学反应方程式:___________ 。
(4)流程中产生NaHCO3固体的化学方程式:___________ 。
(5)下列说法不正确的是___________。
(1)“操作1”的名称:
(2)“循环
 ”的物质为:
”的物质为:(3)“操作2”的化学反应方程式:
(4)流程中产生NaHCO3固体的化学方程式:
(5)下列说法不正确的是___________。
| A.由“操作1”可知,在相同温度下碳酸氢钠溶解度比NaCl大 |
| B.侯德榜联合制碱法得到的主要产品是烧碱,副产物是NH4Cl |
| C.应该向“饱和NaCl溶液”中先通入足量NH3,再通入足量CO2 |
D.使原料氯化钠的利用率从70%提高到90%以上,主要设计了“循环 ” ” |
您最近一年使用:0次
解题方法
9 . 下列实验操作、现象、结论都正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 把温度计插入滴加了几滴水的碳酸氢钠固体中,温度计读数下降 | 碳酸氢钠溶解放热 |
| B | 用玻璃棒蘸取新制氯水点在pH试纸上,试纸变白 | Cl2分子具有漂白性 |
| C | 向分别装有盐酸和氢氧化钠溶液的两支试管中,各加入一小块铝片,两支试管均产生气泡 | 铝片与酸、碱都能反应 |
| D | 向二氧化硫的水溶液中滴入1~2滴品红溶液,振荡,溶液变为无色 | 二氧化硫有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列有关卤族元素及其化合物的说法不正确的是
| A.F2与H2在暗处能剧烈化合并发生爆炸,生成的HF很稳定 |
| B.次氯酸见光易分解,久置氯水的酸性比新制氯水弱 |
| C.Br2是深红棕色液体,I2是紫黑色固体 |
| D.氯、溴、碘元素最高价氧化物的水化物酸性逐渐减弱 |
您最近一年使用:0次



