1 . 乙酸乙酯是一种用途广泛的精细化工产品,一般通过乙酸和乙醇酯化合生成。
(1)在实验室利用上述方法制得乙酸乙酯含有杂质(不计副反应),简述如何提纯产品_______ 。
(2)若用 标记乙醇,该反应的化学方程式
标记乙醇,该反应的化学方程式_______ 。
(3)一定温度下该反应的平衡常数 。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率
。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率
_______ (计算时不计副反应);若乙酸和乙醇的物质的量之比为 ,相应平衡体系中乙酸乙酯的物质的量分数为x,请绘制x随n变化的示意图
,相应平衡体系中乙酸乙酯的物质的量分数为x,请绘制x随n变化的示意图_______ 。
(4)近年来,用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,具有明显的经济优势,其合成的基本反应为 (
( )。在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是
)。在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是_______ 。
a.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,反应已达到化学平衡
b.当乙烯的百分含量保持不变时,反应已达到化学平衡
c.在反应过程中任意时刻移除部分产品,都可以使平衡正向移动,但该反应的平衡常数不变
d.达到平衡后再通入少量乙烯,再次达到平衡时,乙烯的浓度大于原平衡
(5)在乙烯与乙酸等物质的量投料条件下,某研究小组在不同压强、相同时间点进行了乙酸乙酯的产率随温度变化的测定实验,实验结果如图所示。回答下列问题:
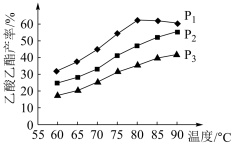
①温度在60~80℃范围内,乙烯与乙酸反应速率由大到小的顺序是_______ [用 、
、 、
、 分别表示在不同压强下的反应速率]。
分别表示在不同压强下的反应速率]。
②在压强为 、温度超过80℃时,乙酸乙酯产率下降的原因可能是
、温度超过80℃时,乙酸乙酯产率下降的原因可能是_______ 。
③为提高乙酸乙酯的合成速率和产率,可以采取的措施_______ (任写两条)。
(1)在实验室利用上述方法制得乙酸乙酯含有杂质(不计副反应),简述如何提纯产品
(2)若用
 标记乙醇,该反应的化学方程式
标记乙醇,该反应的化学方程式(3)一定温度下该反应的平衡常数
 。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率
。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率
 ,相应平衡体系中乙酸乙酯的物质的量分数为x,请绘制x随n变化的示意图
,相应平衡体系中乙酸乙酯的物质的量分数为x,请绘制x随n变化的示意图(4)近年来,用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,具有明显的经济优势,其合成的基本反应为
 (
( )。在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是
)。在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是a.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,反应已达到化学平衡
b.当乙烯的百分含量保持不变时,反应已达到化学平衡
c.在反应过程中任意时刻移除部分产品,都可以使平衡正向移动,但该反应的平衡常数不变
d.达到平衡后再通入少量乙烯,再次达到平衡时,乙烯的浓度大于原平衡
(5)在乙烯与乙酸等物质的量投料条件下,某研究小组在不同压强、相同时间点进行了乙酸乙酯的产率随温度变化的测定实验,实验结果如图所示。回答下列问题:

①温度在60~80℃范围内,乙烯与乙酸反应速率由大到小的顺序是
 、
、 、
、 分别表示在不同压强下的反应速率]。
分别表示在不同压强下的反应速率]。②在压强为
 、温度超过80℃时,乙酸乙酯产率下降的原因可能是
、温度超过80℃时,乙酸乙酯产率下降的原因可能是③为提高乙酸乙酯的合成速率和产率,可以采取的措施
您最近一年使用:0次
2021-04-09更新
|
720次组卷
|
2卷引用:上海市黄埔区2021届高三第二次模拟考试化学试题
名校
2 . 某学生在实验室制取乙酸丁酯(已知乙酸丁酯的沸点124~126℃,乙酸的沸点118℃反应温度115~125℃),其反应装置应选择( )
A.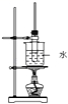 | B.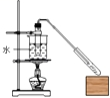 |
C. | D. |
您最近一年使用:0次
2016-12-09更新
|
2153次组卷
|
6卷引用:上海市崇明区2018届高三第一次模拟考试化学试题
上海市崇明区2018届高三第一次模拟考试化学试题上海市青浦区2021届高三等级考二模化学试题2015-2016学年安徽合肥一中高二下期中化学试卷辽宁省实验中学2017-2018学年高一下学期期末考试化学试题(已下线)第31讲 乙醇和乙酸(精练)-2022年高考化学一轮复习讲练测上海市上海华东师范大学附属进华中学2022届高三9月月考化学试题



