名校
1 . 乙酰乙酸乙酯是有机合成的中间体,用乙酸乙酯合成乙酰乙酸乙酯的原理如下:
已知:乙酰乙酸乙酯在95℃开始分解。
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性( )。
)。
④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水 充分振荡静置后过滤。
充分振荡静置后过滤。
⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择___________ (填标号)。
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是___________ 。
(3)分离回收溶剂A采用的方法是___________ (填标号)。
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式___________ ,乙酸乙酯中乙醇含量过少或过多均不利于乙酰乙酸乙酯的生成,原因是___________ 。
(5)步骤④中加入饱和氯化钠溶液的目的是___________ 。
(6)下列仪器在步骤⑤中无需使用的是___________ (填名称);采用减压蒸馏获得乙酰乙酸乙酯的原因___________ 。
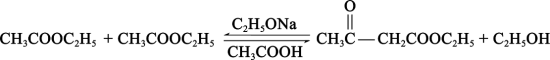
| 名称 | 熔点/℃ | 沸点/℃ | 密度/ | 溶解度 | ||
 | 乙醇 | 乙醚 | ||||
| 苯 | 5.5 | 80.1 | 0.88 | 不溶 | 互溶 | 互溶 |
| 二甲苯 | -25.18 | 144.4 | 0.8802 | 不溶 | 互溶 | 互溶 |
| 乙酸乙酯 | -83.6 | 77.1 | 0.9003 | 难溶 | 互溶 | 互溶 |
| 金属钠 | 97.82 | 881.4 | 0.968 | 反应 | 反应 | 不溶 |
| 乙酰乙酸乙酯 | <-80 | 180.4 | 1.0282 | 微溶 | 互溶 | 互溶 |
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属
 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。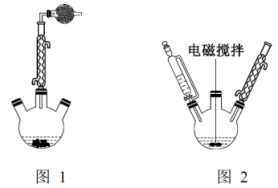
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性(
 )。
)。④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水
 充分振荡静置后过滤。
充分振荡静置后过滤。⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是
(3)分离回收溶剂A采用的方法是
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式
(5)步骤④中加入饱和氯化钠溶液的目的是
(6)下列仪器在步骤⑤中无需使用的是

您最近一年使用:0次



