名校
解题方法
1 . 下列有关各实验说法不正确的是
| A.配制60mL0.1mol/L硫酸铜溶液,需称取胆矾晶体2.5g |
| B.制取乙酸乙酯的实验中,饱和Na2CO3溶液可以换成饱和NaHCO3溶液 |
| C.测定硫酸铜晶体中结晶水的含量实验中,加热后坩埚和药品总质量应至少连续两次称量质量差小于0.1g |
| D.用质量分数98%的浓H2SO4配制0.5mol/LH2SO4溶液,量取浓硫酸时俯视读数,将导致实验结果偏高 |
您最近一年使用:0次
名校
2 . 有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为 ;C的相对分子质量为46,能与Na反应,但不能与
;C的相对分子质量为46,能与Na反应,但不能与 溶液反应;D的空间填充模型为
溶液反应;D的空间填充模型为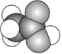 ,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:
,向该物质的水溶液中滴加紫色石蕊溶液,溶液变红色。请回答下列问题:
(2)B的结构简式是
(3)C和D在浓硫酸、加热的条件下可发生反应,装置如图。
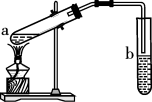
②b试管中盛放的溶液是
③导管末端不伸入b试管溶液中是为了
(4)已知B可以发生如下转化过程:
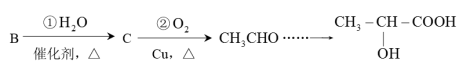
ii.②中发生反应的化学方程式为
iii.含有相同官能团的有机物具有相似的化学性质,下列关于 的说法正确的是
的说法正确的是
b.该物质可以发生酯化反应
c.
 该物质与足量金属钠反应,可生成
该物质与足量金属钠反应,可生成 氢气
氢气d.该物质不能使酸性高锰酸钾溶液褪色
您最近一年使用:0次
名校
解题方法
3 . 水杨酸异戊酯(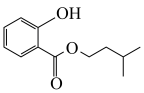 ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
①取27.6g(0.20mol)水杨酸、43.2mL(0.40mol)异戊醇、8mL环己烯和2mL浓硫酸依次加到圆底烧瓶中。
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。
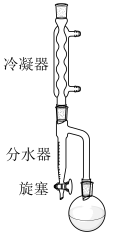
③待反应液冷却后依次用水、 溶液、饱和NaCl溶液洗涤至中性后分出有机层。
溶液、饱和NaCl溶液洗涤至中性后分出有机层。
④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和_______ ,加入环己烯的目的是_______ 。
(2)写出制备水杨酸异戊酯的化学方程式:_______ 。
(3)步骤②中回流到圆底烧瓶中的物质主要有_______ ,表明反应中不再有水生成的现象是_______ 。
(4)洗涤反应液时需要使用的仪器是_______ 。
(5)采用减压蒸馏有机层滤液的原因是_______ 。
(6)本次实验的产率为_______ %。
(7)红外光谱图中可获得产物信息包括_______ 。
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
 ,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:
,摩尔质量为208g/mol)是一种具有较高应用价值的化工产品,在香精、医药等领域有广泛的应用。制备水杨酸异戊酯实验步骤如下:①取27.6g(0.20mol)水杨酸、43.2mL(0.40mol)异戊醇、8mL环己烯和2mL浓硫酸依次加到圆底烧瓶中。
②按照下图搭建反应装置,在145~155℃油浴下加热回流至不再有水生成。

③待反应液冷却后依次用水、
 溶液、饱和NaCl溶液洗涤至中性后分出有机层。
溶液、饱和NaCl溶液洗涤至中性后分出有机层。④干燥、减压蒸馏有机层,收集到31.2g产物。
⑤用红外光谱仪和核磁共振仪对产物进行表征。
已知:①环己烯(沸点83℃)可与水形成沸点为70℃的共沸物。
②沸点:水杨酸211℃、异戊醇131℃、环己烯83℃、水杨酸异戊酯282℃。
回答以下问题:
(1)反应中浓硫酸的作用是吸水剂和
(2)写出制备水杨酸异戊酯的化学方程式:
(3)步骤②中回流到圆底烧瓶中的物质主要有
(4)洗涤反应液时需要使用的仪器是
(5)采用减压蒸馏有机层滤液的原因是
(6)本次实验的产率为
(7)红外光谱图中可获得产物信息包括
a.产物中碳氧双键键长 b.产物相对分子质量
c.产物中含有酯基结构 d.产物中氧元素质量分数
您最近一年使用:0次
名校
4 . 乙酰乙酸乙酯是有机合成的中间体,用乙酸乙酯合成乙酰乙酸乙酯的原理如下:
已知:乙酰乙酸乙酯在95℃开始分解。
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性( )。
)。
④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水 充分振荡静置后过滤。
充分振荡静置后过滤。
⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择___________ (填标号)。
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是___________ 。
(3)分离回收溶剂A采用的方法是___________ (填标号)。
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式___________ ,乙酸乙酯中乙醇含量过少或过多均不利于乙酰乙酸乙酯的生成,原因是___________ 。
(5)步骤④中加入饱和氯化钠溶液的目的是___________ 。
(6)下列仪器在步骤⑤中无需使用的是___________ (填名称);采用减压蒸馏获得乙酰乙酸乙酯的原因___________ 。
| 名称 | 熔点/℃ | 沸点/℃ | 密度/ | 溶解度 | ||
 | 乙醇 | 乙醚 | ||||
| 苯 | 5.5 | 80.1 | 0.88 | 不溶 | 互溶 | 互溶 |
| 二甲苯 | -25.18 | 144.4 | 0.8802 | 不溶 | 互溶 | 互溶 |
| 乙酸乙酯 | -83.6 | 77.1 | 0.9003 | 难溶 | 互溶 | 互溶 |
| 金属钠 | 97.82 | 881.4 | 0.968 | 反应 | 反应 | 不溶 |
| 乙酰乙酸乙酯 | <-80 | 180.4 | 1.0282 | 微溶 | 互溶 | 互溶 |
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属
 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。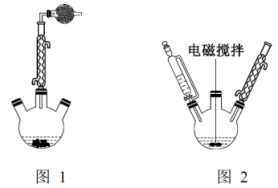
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性(
 )。
)。④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水
 充分振荡静置后过滤。
充分振荡静置后过滤。⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是
(3)分离回收溶剂A采用的方法是
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式
(5)步骤④中加入饱和氯化钠溶液的目的是
(6)下列仪器在步骤⑤中无需使用的是

您最近一年使用:0次
5 . 下列说法不正确的是
| A.乙酸乙酯的制备实验中不能将导管伸入饱和碳酸钠溶液中 |
| B.可以用紫外可见分光光度法测定废水中苯酚的含量 |
| C.发现有人氨气或溴蒸汽中毒时应立即转移至室外,必要时进行人工呼吸 |
D.应选择 进行亚铁盐和 进行亚铁盐和 溶液反应的实验 溶液反应的实验 |
您最近一年使用:0次
6 . 下列实验操作可达到预期目的的是
| 选项 | 目的 | 操作 |
| A | 利用密度差异分离混合物 | 对乙酸乙酯和乙醇混合液用分液漏斗进行分液 |
| B | 配制0.10mol/LNa2CO3溶液 | 称取5.3gNa2CO3•10H2O固体于烧杯中,加入少量蒸馏水溶解,冷却后,转移至500mL容量瓶中定容 |
| C | 测定硫酸铜晶体中结晶水含量 | 加热后的坩埚直接放置在石棉网上冷却,称重 |
| D | 配制FeSO4溶液 | 先将FeSO4固体溶在稀硫酸中,然后稀释,并加入少量铁粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-23更新
|
1210次组卷
|
5卷引用:山东省潍坊青州市2022届5月学业水平等级考试化学试题
山东省潍坊青州市2022届5月学业水平等级考试化学试题四川省成都市2022届高三第二次诊断性检测理综化学试题(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)化学-2022年高考押题预测卷01(山东卷)(已下线)第一部分 二轮专题突破 专题17 典型实验装置及化学实验基本操作
名校
7 . 某化学兴趣小组在实验室中用苯甲醛制备苯甲醇和苯甲酸。有关物质的性质如表所示:
已知:2HCHO+KOH=CH3OH+HCOOK
回答下列问题:
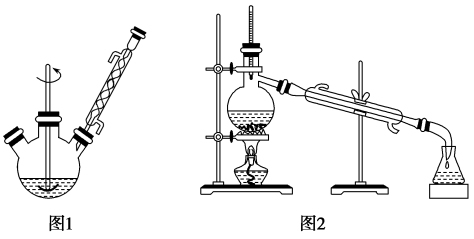
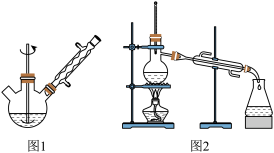
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有_______ (写结构简式)杂质。
②写出三颈烧瓶内发生反应的化学方程式_______ 。
(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是_______ ,而用碳酸钠溶液洗涤可除去醚层中极少量的苯甲酸。
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140 ℃时改用空气冷凝管,收集198 ℃~206 ℃的馏分。
①锥形瓶上加塞子的目的是_______ ;无水硫酸镁的作用是_______ 。
②蒸馏除去乙醚的过程中宜采用的加热方式为_______ ;收集的198 ℃~206 ℃的馏分为_______ (写名称)。
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为_______ 。
(5)图1和图2装置中都用了冷凝管,下列说法正确的是_______ (填选项序号)。
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
| 苯甲醛 | 微溶于水,易溶于有机溶剂;易被空气氧化;与饱和NaHSO3溶液反应产生沉淀 |
| 苯甲醇 | 沸点为205.3 ℃;微溶于水,易溶于醇、醚等 |
| 苯甲酸 | 熔点为121.7 ℃,沸点为249 ℃;微溶于水 |
| 乙醚 | 沸点为34.8 ℃;难溶于水;易燃烧,当空气中含量为1.83%~48.0%时易发生爆炸 |
回答下列问题:
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有
②写出三颈烧瓶内发生反应的化学方程式

(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140 ℃时改用空气冷凝管,收集198 ℃~206 ℃的馏分。
①锥形瓶上加塞子的目的是
②蒸馏除去乙醚的过程中宜采用的加热方式为
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为
(5)图1和图2装置中都用了冷凝管,下列说法正确的是
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
您最近一年使用:0次
2021-09-15更新
|
553次组卷
|
3卷引用:广东省揭阳普宁市普师高级中学2021-2022学年高三上学期第一次阶段考试化学试题
广东省揭阳普宁市普师高级中学2021-2022学年高三上学期第一次阶段考试化学试题河南省许昌市高级中学2022-2023学年高三上半年第一次模拟考试化学试题(已下线)05 以分离提纯为主线的有机制备类综合实验 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
名校
解题方法
8 . 某化学兴趣小组在实验室中用苯甲醛制备苯甲醇和苯甲酸。有关物质的性质如表所示:
已知:2HCHO+KOH CH3OH+HCOOK
CH3OH+HCOOK
回答下列问题:
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛5.10mL,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有___ (写结构简式)杂质。
②写出三颈烧瓶内发生反应的化学方程式___ 。
(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是___ ,而用碳酸钠溶液洗涤可除去醚层中极少量的苯甲酸。
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140℃时改用空气冷凝管,收集198℃~206℃的馏分。
①锥形瓶上加塞子的目的是___ ;无水硫酸镁的作用是___ 。
②蒸馏除去乙醚的过程中宜采用的加热方式为___ ;收集的198℃~206℃的馏分为___ (写名称)。
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为___ ,最终得到2.1g苯甲酸,其产率为__ %(保留三位有效数字)。
(5)图1和图2装置中都用了冷凝管,下列说法正确的是___ (填选项序号)。
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
| 苯甲醛 | 密度为1.04g/ml;微溶于水,易溶于有机溶剂;易被空气氧化;与饱和NaHSO3溶液反应产生沉淀 |
| 苯甲醇 | 沸点为205.3℃;微溶于水,易溶于醇、醚等 |
| 苯甲酸 | 熔点为121.7℃,沸点为249℃;微溶于水 |
| 乙醚 | 沸点为34.8℃;难溶于水,易燃烧,当空气中含量为1.83%~48.0%时易发生爆炸 |
 CH3OH+HCOOK
CH3OH+HCOOK回答下列问题:
(1)向图1所示装置(夹持及加热装置已略去)中加入少量NaOH和水,搅拌溶解,稍冷,加入新蒸过的苯甲醛5.10mL,开启搅拌器,加热回流。
①长久放置的苯甲醛中易含有
②写出三颈烧瓶内发生反应的化学方程式

(2)停止加热,从球形冷凝管上口缓缓加入冷水,摇动,冷却后将液体倒入分液漏斗,用乙醚萃取三次,水层保留待用。合并三次萃取液,依次用饱和NaHSO3溶液、Na2CO3溶液、水洗涤。用饱和亚硫酸氢钠溶液洗涤的目的是
(3)将洗涤后的醚层倒入干燥的锥形瓶内,加入无水MgSO4后再加上瓶塞,静置一段时间后,将锥形瓶中溶液转入图2所示蒸馏装置中,缓缓加热,蒸馏除去乙醚。当温度升到140℃时改用空气冷凝管,收集198℃~206℃的馏分。
①锥形瓶上加塞子的目的是
②蒸馏除去乙醚的过程中宜采用的加热方式为
(4)将萃取后的水层慢慢地加入到盛有盐酸的烧杯中,同时用玻璃棒搅拌,析出白色固体。冷却、过滤,得到粗苯甲酸产品,然后提纯得到较纯净的产品。将苯甲酸粗产品提纯所用的实验方法为
(5)图1和图2装置中都用了冷凝管,下列说法正确的是
a.两种冷凝管冷凝效果相同,本实验中可以互换使用
b.直形冷凝管一般在用蒸馏法分离物质时使用
c.两种冷凝管的冷凝水进出方向都为“高(处)进低(处)出”
d.球形冷凝管能冷凝回流反应物而减少其蒸发流失,使反应更彻底
您最近一年使用:0次
9 . 实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr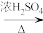 C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
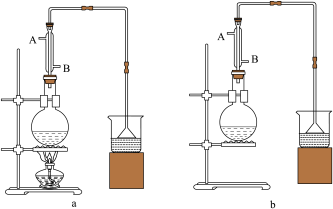
(1)该实验应选择图中的a装置还是b装置?_____________ 。
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是( )
A. A进B出B. B进A出C.从A进或B进均可
(4)可能发生的副反应为:_____________ 、__________ 、______________ (至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_____________________________ 。
C2H5—OH+HBr
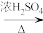 C2H5Br+H2O
C2H5Br+H2O已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?

(2)反应装置中的烧瓶应选择下列哪种规格最合适
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是
A. A进B出B. B进A出C.从A进或B进均可
(4)可能发生的副反应为:
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是
您最近一年使用:0次
2016-12-09更新
|
653次组卷
|
22卷引用:2015-2016学年宁夏银川二中高二下3月月考化学试卷
2015-2016学年宁夏银川二中高二下3月月考化学试卷云南省鲁甸县一中2019-2020学年高二10月月考化学试题云南省昭通鲁甸县二中2019-2020学年高二10月月考化学试题云南省河口县第一中学2019-2020学年高二上学期12月月考化学试题河北省张家口市第一中学2020-2021学年高二下学期 4月月考(普实班)化学试题云南省玉溪市通海县三中2019-2020学年高二上学期期中考试化学试题云南省玉溪市澄江一中2019-2020学年高二上学期期中考试化学试题云南省玉溪市华宁县第二中学2019-2020学年高二上学期期末考试化学试题云南省迪庆州香格里拉中学2019-2020学年高二上学期期末考试化学试题云南省富宁县三中2019-2020学年高二上学期期末考试化学试题云南省绿春县高级中学2019-2020学年高二上学期期末考试化学试题云南省普洱市墨江县民族学校2019—2020学年高二上学期期末考试化学试题云南省镇雄县民族中学2019-2020学年高二上学期期末考试化学试题云南省昭通市彝良县第一中学2019—2020学年高二上学期期末考试化学试题贵州省贞丰县第二中学2019-2020学年高二上学期期末考试化学试题云南省勐腊县第二中学2019-2020学年高二上学期期末考试化学试题广西罗城县第二高级中学2019-2020学年高二上学期期末考试化学试题广西贺州市富川县民族中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区河池市环江县第三中学2019-2020学年高二上学期期末考试化学试题云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题广东省深圳市龙华中学2021-2022学年高三下学期(二月第一次)半周测化学试题广东省佛山市萌茵实验学校2020-2021学年高二下学期期中考试化学试题



