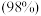名校
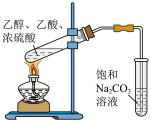
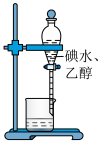
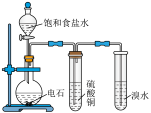
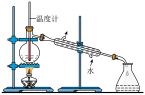
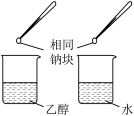
1 . 利用下列装置(夹持装置略)或操作进行实验,能达到实验目的的是
| A | B |
|
|
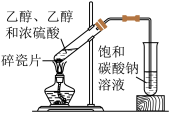
| 制备乙酸乙酯 | 分离碘水和乙醇 |
|
|
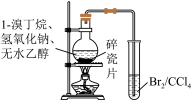
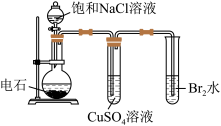
| 检验产物乙炔 | 分离甲苯和乙醇 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 下列实验操作不正确的是
| A.制备乙酸乙酯时,为防止暴沸,应加入沸石 |
| B.不慎将苯酚溶液沾到皮肤上,应立即用稀NaOH溶液清洗 |
| C.饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率 |
D.向 溶液中逐滴加入稀氨水,至沉淀恰好溶解,制得银氨溶液 溶液中逐滴加入稀氨水,至沉淀恰好溶解,制得银氨溶液 |
您最近半年使用:0次
名校
解题方法
3 . 某化学兴趣小组设计实验利用苯甲酸(沸点249℃)和异丙醇(沸点82℃)制备苯甲酸异丙酯(沸点218℃),实验装置如图:
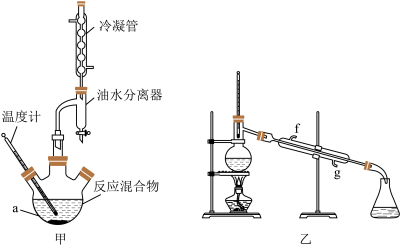
| A.在仪器a中加入三种试剂的先后顺序是:浓硫酸、异丙醇、苯甲酸 |
| B.实验采用水浴加热,若温度过高会使产率减小 |
| C.加入的苯甲酸和异丙醇中,需过量的是苯甲酸 |
| D.步骤③操作时应收集218℃的馏分,如果温度计水银球偏下,则收集的精制产品中可能混有的杂质为苯甲酸 |
您最近半年使用:0次
名校
解题方法
4 . 下列实验方案中,不能达到相应实验目的的是
方案 |
|
|
目的 | A.比较乙醇中羟基氢原子和水分子中氢原子的活泼性 | B.验证1-溴丁烷在NaOH乙醇溶液中发生消去反应 |
方案 |
|
|
目的 | C.检验电石与水反应生成乙炔 | D.实验室制备乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 下列实验方案不合理的是
| A.用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸等 |
| B.分离苯和溴苯的混合物,可用蒸馏法 |
| C.分离苯和CCl4的混合液,可以加蒸馏水然后分液 |
| D.可用水来鉴别苯、乙醇、四氯化碳 |
您最近半年使用:0次
名校
解题方法
6 . 丙炔酸甲酯(CH≡C-COOCH3)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为CH≡C-COOH+CH3OH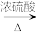 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。
实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
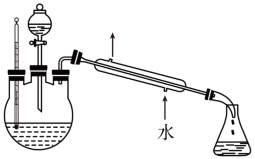
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。___________ 。
(2)步骤2中,如图所示的装置中仪器A的名称是___________ ;蒸馏烧瓶中加入碎瓷片的目的是___________ 。
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是___________ ;分离出有机相的操作名称为___________ 。
(4)步骤4中,蒸馏时不能用水浴加热的原因是___________ 。
(5)实验中丙炔酸甲酯的产率为___________ 。
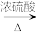 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。
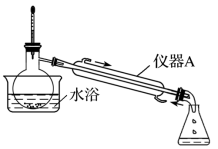
(2)步骤2中,如图所示的装置中仪器A的名称是
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是
(4)步骤4中,蒸馏时不能用水浴加热的原因是
(5)实验中丙炔酸甲酯的产率为
您最近半年使用:0次
名校
7 . 乙酸乙酯是一种重要的化工原料。查阅资料得到下列数据:
请回答:
(1)实验室常用下图装置来制备乙酸乙酯。______ ;浓硫酸对反应有催化作用,但加入的浓硫酸不能太多也不能太少,原因是______ 。
②防止加热时液体暴沸,需要在试管加入碎瓷片,如果加热一段时间后发现忘记了加碎瓷片,应该采取的正确操作是______ 。
A. 立即补加 B. 冷却后补加 C. 不需补加 D. 重新配料
(2)产品纯化。分液法从试管B中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,首先向乙酸乙酯中加入无水氯化钙,除去__________ (填名称);然后再加入无水硫酸钠除去水,最后进行__________ (填操作名称)得到较纯净的乙酸乙酯。
(3)该实验中用 乙酸与
乙酸与 乙醇反应,如果实际得到的乙酸乙酯的质量是
乙醇反应,如果实际得到的乙酸乙酯的质量是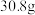 ,则该实验中乙酸乙酯的产率是
,则该实验中乙酸乙酯的产率是________ 。(产率指的是某种生成物的实际产量与理论产量的比值)
(4)另一化学小组设计下图所示的装置制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)。此装置和上图装置相比的优点是________ (写出一条即可)。
物质 | 沸点 | 密度 | 相对分子质量 | 水溶性 |
乙醇 | 78.0 | 0.8 | 46 | 互溶 |
乙酸 | 118.0 | 1.1 | 60 | 可溶 |
乙酸乙酯 | 77.5 | 0.9 | 88 | 微溶 |
乙醚 |
| 0.7 | 74 | 微溶 |
浓硫酸 | 338.0 | 1.8 | 98 | 易溶 |
无水氯化钙 | 可与乙醇形成难溶于水的 | |||
(1)实验室常用下图装置来制备乙酸乙酯。
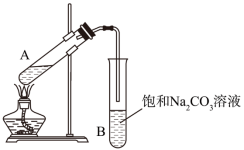
②防止加热时液体暴沸,需要在试管加入碎瓷片,如果加热一段时间后发现忘记了加碎瓷片,应该采取的正确操作是
A. 立即补加 B. 冷却后补加 C. 不需补加 D. 重新配料
(2)产品纯化。分液法从试管B中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,首先向乙酸乙酯中加入无水氯化钙,除去
(3)该实验中用
 乙酸与
乙酸与 乙醇反应,如果实际得到的乙酸乙酯的质量是
乙醇反应,如果实际得到的乙酸乙酯的质量是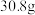 ,则该实验中乙酸乙酯的产率是
,则该实验中乙酸乙酯的产率是(4)另一化学小组设计下图所示的装置制取乙酸乙酯(铁架台、铁夹、加热装置均已略去)。此装置和上图装置相比的优点是
您最近半年使用:0次
解题方法
8 . 下列说法正确的是
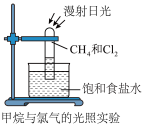
①甲烷与氯气反应得到的液态混合物中含有二氯甲烷、三氯甲烷和四氯化碳
②李比希元素定量分析只能进行碳、氢、氧等有机化合物的元素定量分析
③食用白糖的主要成分是蔗糖
④乙烯、氯乙烯、聚己烯均可使酸性高锰酸钾溶液褪色
⑤纤维素、合成纤维、光导纤维都是有机高分子化合物
⑥可利用饱和碳酸钠溶液除去乙酸乙酯中含有的少量乙酸
①甲烷与氯气反应得到的液态混合物中含有二氯甲烷、三氯甲烷和四氯化碳
②李比希元素定量分析只能进行碳、氢、氧等有机化合物的元素定量分析
③食用白糖的主要成分是蔗糖
④乙烯、氯乙烯、聚己烯均可使酸性高锰酸钾溶液褪色
⑤纤维素、合成纤维、光导纤维都是有机高分子化合物
⑥可利用饱和碳酸钠溶液除去乙酸乙酯中含有的少量乙酸
| A.②④⑤ | B.①③④ | C.①⑤⑥ | D.①③⑥ |
您最近半年使用:0次
名校
9 . 下列实验操作、现象或解释均符合客观事实的是
| 选项 | 装置 | 操作、现象或解释 |
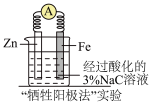
| A |
| 一段时间后用胶头滴管取铁电极区域的溶液少量于试管中,滴加2滴铁氰化钾溶液,可观察到特征蓝色沉淀 |
| B |
| 有机产物使试管内产生少量白雾且内壁有油状液滴出现 |
| C |
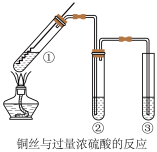
| 观察到试管①底部有白色固体生成,向其中缓慢加入适量蒸馏水,溶液变蓝,证明加热条件下铜与浓硫酸反应生成了硫酸铜 |
| D |
| 实验结束后取下右侧试管,沿内壁缓缓加入1mL紫色石蕊溶液,发现石蕊分为三层,由下而上分别是蓝、紫、红(整个过程不振荡试管) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 乙酰乙酸乙酯是有机合成的中间体,用乙酸乙酯合成乙酰乙酸乙酯的原理如下:
已知:乙酰乙酸乙酯在95℃开始分解。
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性( )。
)。
④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水 充分振荡静置后过滤。
充分振荡静置后过滤。
⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择___________ (填标号)。
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是___________ 。
(3)分离回收溶剂A采用的方法是___________ (填标号)。
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式___________ ,乙酸乙酯中乙醇含量过少或过多均不利于乙酰乙酸乙酯的生成,原因是___________ 。
(5)步骤④中加入饱和氯化钠溶液的目的是___________ 。
(6)下列仪器在步骤⑤中无需使用的是___________ (填名称);采用减压蒸馏获得乙酰乙酸乙酯的原因___________ 。
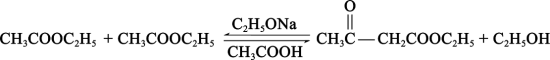
| 名称 | 熔点/℃ | 沸点/℃ | 密度/ | 溶解度 | ||
 | 乙醇 | 乙醚 | ||||
| 苯 | 5.5 | 80.1 | 0.88 | 不溶 | 互溶 | 互溶 |
| 二甲苯 | -25.18 | 144.4 | 0.8802 | 不溶 | 互溶 | 互溶 |
| 乙酸乙酯 | -83.6 | 77.1 | 0.9003 | 难溶 | 互溶 | 互溶 |
| 金属钠 | 97.82 | 881.4 | 0.968 | 反应 | 反应 | 不溶 |
| 乙酰乙酸乙酯 | <-80 | 180.4 | 1.0282 | 微溶 | 互溶 | 互溶 |
现用市售乙酸乙酯(含2%乙醇)合成乙酰乙酸乙酯的步骤如下:
①制备钠珠:将1.0g金属
 迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。
迅速切成薄片,放入50mL的三颈烧瓶中,并加入10mL经过干燥的溶剂A,加热回流至熔融,装置如图1,拆去回流装置,用橡皮塞塞住瓶口,用力振摇即得细粒状钠珠。稍冷分离回收溶剂A。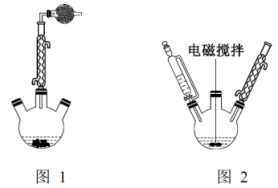
③酸化:向橘红色溶液中加入50%醋酸使其呈弱酸性(
 )。
)。④分液:将反应液转入分液漏斗,加入等体积的饱和氯化钠溶液,振摇,静置,分液。将有机层倒入锥形瓶中,并加适量的无水
 充分振荡静置后过滤。
充分振荡静置后过滤。⑤蒸馏:将步骤④所得有机混合液水浴加热蒸馏出未反应的乙酸乙酯,停止蒸馏,冷却。再将蒸馏得到的剩余物进行减压蒸馏,收集馏分。
回答下列问题:
(1)步骤①中溶剂A最好选择
a.乙醇 b.水 c.二甲苯 d.苯
(2)制备钠珠采用步骤①中操作方法的原因是
(3)分离回收溶剂A采用的方法是
a.蒸馏 b.分液 c.蒸发 d.倾倒法
(4)乙醇钠是制备乙酰乙酸乙酯的催化剂,写出生成乙醇钠的化学方程式
(5)步骤④中加入饱和氯化钠溶液的目的是
(6)下列仪器在步骤⑤中无需使用的是

您最近半年使用:0次