名校
解题方法
1 . 乙酸乙酯是一种重要的有机溶剂,在工业上有广泛用途。某兴趣小组同学欲制备乙酸乙酯并对所得产物进行探究。
Ⅰ.乙酸乙酯的制备(实验装置如下图所示)
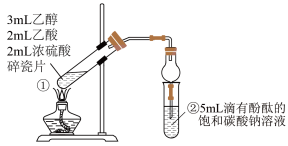
(1)试管①中反应的化学方程式为___________ ,饱和碳酸钠溶液的作用为___________ 。
Ⅱ.产物的探究
反应结束后在试管②中看到分层现象,上层为无色透明的油状液体。取下试管②进行振荡,下层溶液红色褪去。
甲同学认为下层溶液褪色是蒸出的乙酸中和了碳酸钠,乙同学通过查阅资料对甲同学推测产生质疑。
资料:酚酞是一种白色晶状粉末,不溶于水,可溶于乙醇。酚酞试剂是酚酞的乙醇溶液。
(2)乙同学的推测是:___________ 。
两位同学针对各自的推测又进行了如下实验。
实验1:
甲同学用pH计测得饱和碳酸钠溶液(浓度约为2mol/L)的pH为12.23;
按照上述方法进行乙酸乙酯的制取实验,实验结束后,取振荡后的试管②中下层无色液体,分成三份,分别完成以下实验:
(3)b中现象为___________ ,实验1的结论___________ 。
实验2:
(4)e中的实验现象为___________ 。
甲乙两位同学通过对乙酸乙酯收集装置中产生的现象进一步实验和分析,最终确认了酚酞褪色原因。
Ⅲ.拓展延伸
在以上实验过程中,丙同学还有新的发现,他查阅到以下资料:
资料:室温下,当酚酞试剂滴入pH>13的无色溶液时,溶液先变红,静置后褪色。
(5)据此资料,丙同学想到了一种区分1mol/L碳酸钠溶液和1mol/L氢氧化钠溶液的方法,这种方法是___________ 。
Ⅰ.乙酸乙酯的制备(实验装置如下图所示)

(1)试管①中反应的化学方程式为
Ⅱ.产物的探究
反应结束后在试管②中看到分层现象,上层为无色透明的油状液体。取下试管②进行振荡,下层溶液红色褪去。
甲同学认为下层溶液褪色是蒸出的乙酸中和了碳酸钠,乙同学通过查阅资料对甲同学推测产生质疑。
资料:酚酞是一种白色晶状粉末,不溶于水,可溶于乙醇。酚酞试剂是酚酞的乙醇溶液。
(2)乙同学的推测是:
两位同学针对各自的推测又进行了如下实验。
实验1:
甲同学用pH计测得饱和碳酸钠溶液(浓度约为2mol/L)的pH为12.23;
按照上述方法进行乙酸乙酯的制取实验,实验结束后,取振荡后的试管②中下层无色液体,分成三份,分别完成以下实验:
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| a | 滴加几滴酚酞试剂 | 溶液变红 | ___________ |
| b | 滴入乙酸溶液 | ___________ | |
| c | 用pH计测溶液pH | pH为12.21 |
实验2:
| 序号 | 操作 | 现象 |
| d | 试管②中分离出的上层液体,加入饱和碳酸钠溶液,振荡 | 溶液变成浅红色,静置分层后红色消失 |
| e | 取5mL饱和碳酸钠溶液,滴入几滴酚酞试剂,再加入与试管②中上层液体体积相等的纯净的乙酸乙酯,振荡 |
甲乙两位同学通过对乙酸乙酯收集装置中产生的现象进一步实验和分析,最终确认了酚酞褪色原因。
Ⅲ.拓展延伸
在以上实验过程中,丙同学还有新的发现,他查阅到以下资料:
资料:室温下,当酚酞试剂滴入pH>13的无色溶液时,溶液先变红,静置后褪色。
(5)据此资料,丙同学想到了一种区分1mol/L碳酸钠溶液和1mol/L氢氧化钠溶液的方法,这种方法是
您最近一年使用:0次
2023-05-27更新
|
105次组卷
|
2卷引用:江西省宜春市上高中学2022-2023学年高一下学期7月期末考试化学试题
名校
2 . 下列实验不能达到实验目的的是

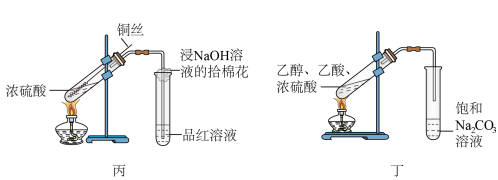


| A.装置甲实验室制氨气 | B.装置乙实验室制氯气 |
| C.装置丙检验浓硫酸与Cu反应产生SO2 | D.装置丁实验室制乙酸乙酯 |
您最近一年使用:0次
2023-03-30更新
|
526次组卷
|
3卷引用:江西省南昌市铁路第一中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
3 . 用图1所示的装置制备乙酸乙酯,并用图2所示的步骤分离乙酸乙酯、乙醇和乙酸。下列说法错误的是


| A.反应试剂的加入顺序为浓硫酸→乙酸→乙醇 |
| B.乙试管内液体不可以用氢氧化钠溶液代替 |
| C.操作1、操作2是分液,操作3是蒸馏 |
| D.A是乙酸乙酯,E是乙醇,试剂a可以是硫酸 |
您最近一年使用:0次
2022-07-14更新
|
475次组卷
|
3卷引用:江西省全南中学2022-2023学年高一下学期教学质量验收化学试题
江西省全南中学2022-2023学年高一下学期教学质量验收化学试题山东省德州市2021-2022学年高一下学期期末考试化学试题(已下线)专题09 乙醇 乙酸 基本营养物质(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
名校
解题方法
4 . 用乙酸和乙醇反应制备乙酸乙酯的装置如图,下列说法正确的是


| A.试管a中药品添加顺序依次为:浓硫酸、乙醇、乙酸 |
| B.导管伸入试管b中液面以下,防止产物挥发造成损失 |
| C.试管b中溶液红色变浅,是因Na2CO3与乙醇发生反应 |
| D.浓硫酸作反应的催化剂,同时可吸水提高酯的产率 |
您最近一年使用:0次
2022-06-01更新
|
225次组卷
|
2卷引用:江西省抚州市东乡区实验中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
5 . 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取乙酸乙酯的主要步骤如下:
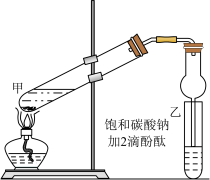
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3—5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:_______ ;与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用_______ 。
(2)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是_______ ;分离时,乙酸乙酯应该从仪器_______ (填:“下口放”或“上口倒”)出。
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_______ mL和_______ mol·L−1。
②分析实验_______ (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(4)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产品产率为_______ (产率%=(实际产量/理论产量)×100%)。

①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3—5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:
(2)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
| 实验编号 | 试管I中试剂 | 试管II中试剂 | 有机层的厚度 厚度/cm |
| A | 2mL乙醇、1mL乙酸、3mL18mol·L−1浓硫酸 | 饱和Na2CO3溶液 | 30 |
| B | 2mL乙醇、1mL乙酸、3mLH2O | 0.1 | |
| C | 2mL乙醇、1mL乙酸、3mL2mol·L−1H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验
(4)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产品产率为
您最近一年使用:0次
名校
解题方法
6 . 利用乙酸乙酯可以制备乙酰乙酸乙酯,有关乙酸乙酯与乙酰乙酸乙酯的制备原理,纯化流程如下。
一、乙酰乙酸乙酯的制备原理
Ⅰ.乙酸乙酯的制备CH3COOH+CH3CH2OH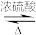 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
Ⅱ. 乙酰乙酸乙酯的制备2CH3COOC2H5 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH
二、乙酸乙酯的制备及纯化实验装置(加热及夹持装置省略)如图:

三、乙酸乙酯纯化的流程

四、乙酰乙酸乙酯的制备和纯化流程

回答下列问题:
(1)仪器乙的名称是___________ ;仪器甲为刺形分馏柱,其作用是___________ 。
(2)乙酸乙酯纯化的过程中,向粗产品中加入饱和碳酸钠溶液的目的是___________ ,“分离”操作所需要的主要玻璃仪器是___________ 。
(3)在圆底烧瓶中放入5g金属钠和25mL二中苯,装上冷凝管加热使钠熔化。拆去冷凝管,用塞子塞紧圆底烧瓶,趁热用力摇动,得到细粒状的钠珠,然后将圆底烧瓶中的二甲苯迅速向圆底烧瓶中加入55mL(约0. 57mol)乙酸乙酯(含少量乙醇),装上带有一根长玻璃导管的单孔胶塞,并在导管上端接一个干燥管,缓缓加热,保持瓶中混合液呈微沸状态。导管上端接一干燥管的目的是___________ 。经过一系列操作,收集到约13g(约0. 1mol)乙酰乙酸乙酯,其产率是___________ %(结果保留三位有效数字)。
一、乙酰乙酸乙酯的制备原理
Ⅰ.乙酸乙酯的制备CH3COOH+CH3CH2OH
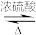 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2OⅡ. 乙酰乙酸乙酯的制备2CH3COOC2H5
 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH二、乙酸乙酯的制备及纯化实验装置(加热及夹持装置省略)如图:

三、乙酸乙酯纯化的流程

四、乙酰乙酸乙酯的制备和纯化流程

回答下列问题:
(1)仪器乙的名称是
(2)乙酸乙酯纯化的过程中,向粗产品中加入饱和碳酸钠溶液的目的是
(3)在圆底烧瓶中放入5g金属钠和25mL二中苯,装上冷凝管加热使钠熔化。拆去冷凝管,用塞子塞紧圆底烧瓶,趁热用力摇动,得到细粒状的钠珠,然后将圆底烧瓶中的二甲苯迅速向圆底烧瓶中加入55mL(约0. 57mol)乙酸乙酯(含少量乙醇),装上带有一根长玻璃导管的单孔胶塞,并在导管上端接一个干燥管,缓缓加热,保持瓶中混合液呈微沸状态。导管上端接一干燥管的目的是
您最近一年使用:0次
名校
7 . 乙酸乙酯是重要的有机合成中间体,广泛应用于化工业。实验室利用如图所示装置制备乙酸乙酯。__ 。与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是__ 。
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始时先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束时充分振荡试管Ⅱ,静置后再测有机层的厚度,实验记录如下:
实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是__ mL和__ mol•L-1。
②分析实验__ (填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
(3)若现有乙酸90g,乙醇138g,发生酯化反应得到88g乙酸乙酯,试计算该反应的产率为__ (保留一位小数)。
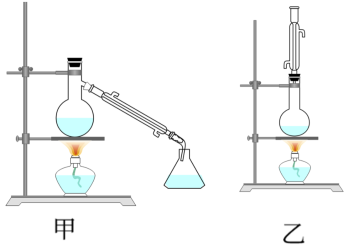
(4)为充分利用反应物,甲、乙两位同学分别设计了如图所示的甲、乙两个装置制备乙酸乙酯(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为最合理的是__ (填“甲”或“乙”)。
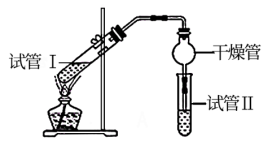
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始时先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束时充分振荡试管Ⅱ,静置后再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的厚度/cm |
| A | 2mL乙醇、1mL乙酸、3mL18mol•L-1浓硫酸 | 饱和碳酸钠溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、3mL2mol•L-1硫酸 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验
(3)若现有乙酸90g,乙醇138g,发生酯化反应得到88g乙酸乙酯,试计算该反应的产率为
(4)为充分利用反应物,甲、乙两位同学分别设计了如图所示的甲、乙两个装置制备乙酸乙酯(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为最合理的是
您最近一年使用:0次
2021-02-16更新
|
640次组卷
|
4卷引用:江西省抚州市金溪县第一中学2021-2022学年高一下学期第二次月考化学试题
名校
解题方法
8 . 下列选用的仪器和药品不能达到实验目的的是
A.粗盐提纯时不溶物的分离 | B.验证氨气极易溶于水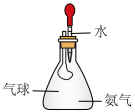 |
C.制备乙酸乙酯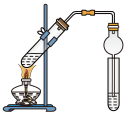 | D.除去乙烷中混有的乙烯 |
您最近一年使用:0次
2020-07-27更新
|
212次组卷
|
4卷引用:江西省宜春市万载中学2021-2022学年高一上学期第二次月考化学试题



