解题方法
1 . 不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀。
(1)基态碳原子的电子排布图为___ 。
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为___ 。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是___ ,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为____ 。
③氨是___ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___ ,氨的沸点高于PH3,原因是___ 。
(3)镍元素基态原子的价电子排布式为___ ,3d能级上的未成对电子数为___ 。
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是___ 。
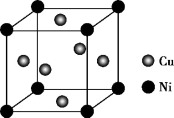
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=___ nm。
(1)基态碳原子的电子排布图为
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
③氨是
(3)镍元素基态原子的价电子排布式为
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=

您最近一年使用:0次
2020-02-12更新
|
793次组卷
|
3卷引用:河南省洛阳市2019-2020学年高二上学期期末考试化学试题
11-12高三·河南许昌·阶段练习
2 . 前四周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子得到一个电子后3p轨道全充满;D最高价氧化物中D的质量分数为40%,且核内质子数等于中子数;F为红色单质,有F+和F2+两种离子。回答下列问题:
(1)元素电负性:D___________ E (填>、<或=)
(2)A、C单质熔点A___________ C(填>、<或=)
(3)AE4中A原子杂化轨道方式为:___________ 杂化;其固态晶体类型为___________
(4)F的核外电子排布式为___________ ;向F的硫酸盐中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体,该晶体中F与NH3之间的化学键为___________
(5)氢化物的沸点:B比D高的原因___________ ;
(6)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。

该晶体中阳离子和阴离子个数比为___________ ,晶体中每个Xn-被___________ 个等距离的C+离子包围。
(1)元素电负性:D
(2)A、C单质熔点A
(3)AE4中A原子杂化轨道方式为:
(4)F的核外电子排布式为
(5)氢化物的沸点:B比D高的原因
(6)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX晶体的最小结构单元如图所示。

该晶体中阳离子和阴离子个数比为
您最近一年使用:0次



