10-11高一·山西忻州·阶段练习
解题方法
1 . 已知X、Y、Z、W为四种短周期元素,其原子序数依次增大,且由这些元素所组成的单质在常温下均呈气态。X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,甲、乙可化合生成离子化合物丙。试回答下列问题:
(1)W元素在周期表中的位置是_________ ;甲的空间构型为___________ 。
(2)丙的水溶液呈酸性,用离子方程式表示其原因____________________________ 。
(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式_________________ ;X、Y组成的液态化合物Y2X416克与足量丁反应生成Y2和液态水,放出Q kJ的热量,请写出该反应的热化学方程式___________
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为____________________ 。
(1)W元素在周期表中的位置是
(2)丙的水溶液呈酸性,用离子方程式表示其原因
(3)X、Z可组成四原子化合物丁,丁是一种二元弱酸,写出丁在水中的电离方程式
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为
您最近一年使用:0次
2011·山西太原·三模
解题方法
2 . 已知A~N分别代表一种物质,它们之间的转化关系如图所示(部分反应的反应条件和生成物已略去)。A、B、C分别是由短周期元素组成的单质,A是金属,D是无色液体。F是一种离子化含物,其阴阳离子的个数比为1:3,且能与水反应得到两种碱。反应①是实验室检验某离子的方法,反应②是工业、生产N的重要反应。请回答下列问题:
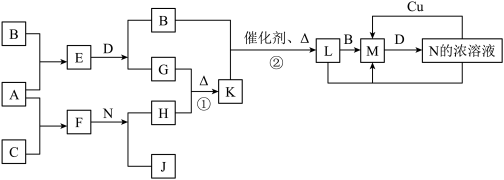
(1)B元素在元素周期表中的位置是__________ ,F的电子式是_____________ 。
(2)写出反应①的离子方程式:___________ ;
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是__________ (请用上图所示关系中反应的化学方程式回答)。
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法。亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO·bCr2O3等,统称为亚铬酸铜。其中:CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的化学方程式:______________________ 。
(5)已知一定温度(>100℃)下,反应②的平衡常数为1。将0.8molK和1.1molB放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4mol/L,此时反应v正_____ v逆(填“>”、“<”或“=”)。当反应到达平衡后,保持温度不变,再加入一定物质的量的B,重新达到平衡,则L的平衡浓度__________ (填“增大”、“不变”或“减小”),B的转化率_________ 。(填“升高”、“不变”或“降低”),L的体积分数___________ (填“增大”、“不变”、“减小”或“无法确定”)。

(1)B元素在元素周期表中的位置是
(2)写出反应①的离子方程式:
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法。亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO·bCr2O3等,统称为亚铬酸铜。其中:CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的化学方程式:
(5)已知一定温度(>100℃)下,反应②的平衡常数为1。将0.8molK和1.1molB放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4mol/L,此时反应v正
您最近一年使用:0次
10-11高三上·福建·阶段练习
解题方法
3 . 短周期元素X、Y、Z在元素周期表中的位置如右图所示,它们的质子数之和为21。

(1)氢元素与Z形成原子个数比为1∶1的化合物,其电子式为_____________ 。该化合物分子中存在__________ (填“共价键”或“离子键”)。
(2)Y最高价氧化物的水化物与Y的氢化物恰好完全反应时,生成物的水溶液呈酸性,其原因是____________________ ;(用离子方程式表示)该溶液中各种离子浓度由大到小顺序为_______________ 。
(3)①恒温下,在容积为2L的刚性容器中充入2mol H2与2mol Y的单质,5分钟后反应达到平衡时,此时Y的单质为1.8mol,则产物的反应速率为_______________ ,平衡时容器内压强与反应前压强比为__________________ ;
②若该反应在恒温恒压条件下进行(其它条件相同),反应达到平衡时,H2的转化率比上述条件下H2的转化率_______ (填“大”、“小”或“相同”)。
(4)常温下,由X的最简单气态氢化物3.2g在氧气中完全燃烧后恢复至常温,放出a kJ 的热量,试写出该反应的热化学方程式:__________________ 。

(1)氢元素与Z形成原子个数比为1∶1的化合物,其电子式为
(2)Y最高价氧化物的水化物与Y的氢化物恰好完全反应时,生成物的水溶液呈酸性,其原因是
(3)①恒温下,在容积为2L的刚性容器中充入2mol H2与2mol Y的单质,5分钟后反应达到平衡时,此时Y的单质为1.8mol,则产物的反应速率为
②若该反应在恒温恒压条件下进行(其它条件相同),反应达到平衡时,H2的转化率比上述条件下H2的转化率
(4)常温下,由X的最简单气态氢化物3.2g在氧气中完全燃烧后恢复至常温,放出a kJ 的热量,试写出该反应的热化学方程式:
您最近一年使用:0次
9-10高一下·北京朝阳·期末
解题方法
4 . 下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
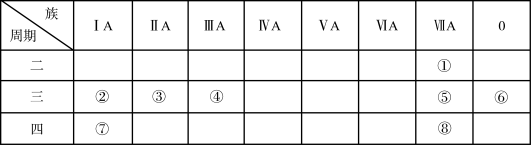
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为___________ 。
(2)地壳中含量最多的金属元素是___________ 。
(3)用电子式表示①与③形成化合物的过程:__________________ 。
(4)这些元素的氧化物对应的水化物中,酸性最强的是________ ,碱性最强的是__________ ,显两性的是___________ ,该两性物质与②的最高价氧化物对应水化物的溶液反应的离子方程式为: _______________________ 。
(5)①②③④四种元素的简单离子核外电子排布相同,都有__________ 个电子,它们的离子半径由大到小的顺序是__________________ (用“>”表示)。
(6)①⑤⑧三种元素的单质沸点由高到低的顺序是_________________ (用“>”表示)。

(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)地壳中含量最多的金属元素是
(3)用电子式表示①与③形成化合物的过程:
(4)这些元素的氧化物对应的水化物中,酸性最强的是
(5)①②③④四种元素的简单离子核外电子排布相同,都有
(6)①⑤⑧三种元素的单质沸点由高到低的顺序是
您最近一年使用:0次
2010·辽宁大连·二模
解题方法
5 . 下列框图中涉及的物质是中学化学常见的。其相互转化关系如图所示。已知:单质A在单质G中能燃烧,其产物溶于水得L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题:
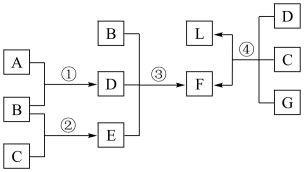
(1)写出B、L的名称:B_________ 、L_________ ;写出F在工业上的任何两点用途_______________________________________ 。
(2)写出③的化学方程式_____________________________ 。
(3)说出形成单质C的元素在元素周期表的位置,第____________ 周期,第_____ 族。
(4)将E通入到某种棕黄色的溶液中也有L、F生成。其反应的离子方程式为_______________________________________ 。
(5)写出④反应的化学方程式____________________ 。

(1)写出B、L的名称:B
(2)写出③的化学方程式
(3)说出形成单质C的元素在元素周期表的位置,第
(4)将E通入到某种棕黄色的溶液中也有L、F生成。其反应的离子方程式为
(5)写出④反应的化学方程式
您最近一年使用:0次
名校
6 . 下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:

(1)a的一种核素核内有一个质子、一个中子,该核素的符号为________ 。
(2)b、c、d、f四种元素的原子半径由大到小的顺序为________ (用元素符号表示)。
(3)c、d、e、h四种元素最高价氧化物对应的水化物的酸性由弱到强的顺序为(用化学式表示)_______________________________ 。
(4)从b、f形成的化合物与d、f形成的化合物的混合物中分离提纯d、f形成的化合物,可加入上述________ (用元素符号表示)两种元素形成的化合物的水溶液后再过滤洗涤。

(1)a的一种核素核内有一个质子、一个中子,该核素的符号为
(2)b、c、d、f四种元素的原子半径由大到小的顺序为
(3)c、d、e、h四种元素最高价氧化物对应的水化物的酸性由弱到强的顺序为(用化学式表示)
(4)从b、f形成的化合物与d、f形成的化合物的混合物中分离提纯d、f形成的化合物,可加入上述
您最近一年使用:0次
2015-05-12更新
|
621次组卷
|
3卷引用:2014-2015河南省南阳方城一中高一下学期学期第一次月考化学试卷
2014-2015河南省南阳方城一中高一下学期学期第一次月考化学试卷陕西省榆林市绥德县绥德中学2019-2020高一下学期第一次阶段性测试化学试题(已下线)4.2.1 元素性质的周期性变化规律练习(1)——《高中新教材同步备课》(人教版 必修第一册)
7 . 下表为元素周期表的一部分。
(1)表中元素________ 的非金属性最强;元素________ 的金属性最强;元素________ 的单质在室温下呈液态;(写元素符号)。
(2)表中半径最大的元素是_______ ;(写元素符号)
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是_______ ;(写化学式,下同)
(4)表中元素⑥、⑦氢化物的稳定性顺序为________ >________ ;
(5)表中元素最高价氧化物对应水化物酸性最强的酸是_________________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ⑤ | |||||
| 三 | ③ | ⑥ | |||||
| 四 | ④ | ⑦ | |||||
(1)表中元素
(2)表中半径最大的元素是
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是
(4)表中元素⑥、⑦氢化物的稳定性顺序为
(5)表中元素最高价氧化物对应水化物酸性最强的酸是
您最近一年使用:0次
11-12高三上·浙江宁波·期中
8 . 下表为部分短周期元素化合价及相应氢化物沸点的数据:
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙。
请回答:
(1)表中属于第三周期元素的是_________________________ (用表中元素编号填写)。
(2)写出H的最高价氧化物的电子式:__________________________ ;
比较A、D、G三种简单阴离子的半径大小:r( ) >r( ) >r( ) (均用实际的元素符号表示)。
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________________ 。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是:______________________ 。
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙。
请回答:
(1)表中属于第三周期元素的是
(2)写出H的最高价氧化物的电子式:
比较A、D、G三种简单阴离子的半径大小:r
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是:
您最近一年使用:0次
9 . 从下列事实所得出的相应结论正确的是
实验事实 | 结论 | |
| A | A元素的原子半径比B元素的原子半径大 | 元素A位于B的下一周期 |
| B | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
| C | 常温下,铜能与浓硝酸反应而铝遇浓硝酸钝化 | 还原性:Cu>Al |
| D | 常温下白磷可自燃而氮气需在放电时才与氧气反应 | 非金属性:P>N |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



