名校
1 . 钨(W)常用于制造白炽灯、碘钨灯等。工业上以黑钨矿(主要成分是 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。
请回答下列问题:
(1)基态 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是__________ ;Mn位于元素周期表__________ 区。
(2)“粉碎”的目的是__________ ;从“浸取”得到的浸渣中分离出 的操作方法是
的操作方法是__________ 、过滤、洗涤、干燥。
(3)根据“转化”,判断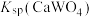
__________ 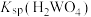 (填“>”或“<”)。
(填“>”或“<”)。
(4)“灼烧”中盛装固体的仪器是__________ (填名称);发生反应的化学方程式为______________________________ 。
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm, 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为__________  (列出计算式即可)。
(列出计算式即可)。
 、
、 ,含少量
,含少量 、
、 )为原料冶炼钨的流程如图所示。
)为原料冶炼钨的流程如图所示。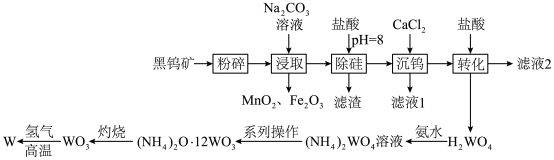
请回答下列问题:
(1)基态
 核外电子占据能量最高的能级符号是
核外电子占据能量最高的能级符号是(2)“粉碎”的目的是
 的操作方法是
的操作方法是(3)根据“转化”,判断
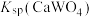
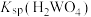 (填“>”或“<”)。
(填“>”或“<”)。(4)“灼烧”中盛装固体的仪器是
(5)碳化钨是一种耐磨、耐高温、高硬度材料。碳化钨晶胞如图所示。已知:晶胞底边长为apm,高为bpm,
 为阿伏加德罗常数的值。碳化钨晶体密度为
为阿伏加德罗常数的值。碳化钨晶体密度为 (列出计算式即可)。
(列出计算式即可)。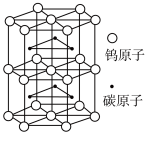
您最近半年使用:0次
昨日更新
|
42次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
解题方法
2 . 一种超导材料(仅由 、
、 、F三种元素组成)的长方体晶胞结构如图所示(已知
、F三种元素组成)的长方体晶胞结构如图所示(已知 ),下列说法错误的是
),下列说法错误的是
 、
、 、F三种元素组成)的长方体晶胞结构如图所示(已知
、F三种元素组成)的长方体晶胞结构如图所示(已知 ),下列说法错误的是
),下列说法错误的是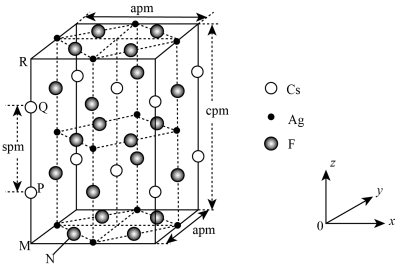
A.基态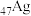 位于元素周期表的 位于元素周期表的 区 区 |
B.若N点原子分数坐标为 ,则P点原子分数坐标为 ,则P点原子分数坐标为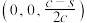 |
C.M、N之间的距离为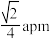 |
D.该晶体最简化学式为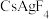 |
您最近半年使用:0次
2024-05-02更新
|
326次组卷
|
3卷引用:2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题
2024届湖南省岳阳市高三下学期第二次教学质量监测(二模)化学试题广西钦州市第四中学2023-2024学年高二下学期3月考试化学试卷(已下线)提升练01 晶体结构及相关计算-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
3 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:___________ 区。
②2017年5月9日我国发布了113号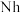 、115号
、115号 、117号
、117号 、118号
、118号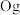 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D_______ E(填“>” “<”或“=”)。
②气态氢化物的沸点:B_____ F (填“>”“<”或“=”),理由是___________ 。B的另一种氢化物可以作为火箭推进剂的燃料之一,其电子式为___________ 。
(1)认识元素周期表的结构:
②2017年5月9日我国发布了113号
 、115号
、115号 、117号
、117号 、118号
、118号 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中 “
的信息,其中 “ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近半年使用:0次
2024-04-26更新
|
39次组卷
|
2卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
名校
解题方法
4 . I.氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式___________ 。
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为___________ 。
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是___________ ,其中 H2S在该反应中___________ (填序号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是___________ (填“还原性”或“氧化性”)。
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:___________ 。
(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式___________ 。
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是___________ 。
(8)比较④与⑨的简单气态氢化物的稳定性___________ >___________ (填化学式)。
(9)由下列元素形成的化合物中含有离子键的是___________。
(10)写出⑤在空气中燃烧产物的电子式:___________ 。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是
(8)比较④与⑨的简单气态氢化物的稳定性
(9)由下列元素形成的化合物中含有离子键的是___________。
| A.①③ | B.②③ | C.①④ | D.⑥⑨ |
您最近半年使用:0次
名校
解题方法
5 . 实验室中可用 或
或 来检验
来检验 ,下列说法正确的是
,下列说法正确的是
 或
或 来检验
来检验 ,下列说法正确的是
,下列说法正确的是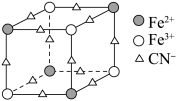
A.铁元素位于周期表第四周期第ⅧB族,属于 区 区 |
B. 与 与 溶液混合,得到的配合物 溶液混合,得到的配合物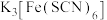 中,提供空轨道的是 中,提供空轨道的是 ,配位原子是 ,配位原子是 ,配位数是6 ,配位数是6 |
C. 中含有离子键、极性共价键和非极性共价键 中含有离子键、极性共价键和非极性共价键 |
D. 与 与 反应可得到一种蓝色沉淀,该沉淀物质晶胞的 反应可得到一种蓝色沉淀,该沉淀物质晶胞的 结构如图所示( 结构如图所示( 未画出),则一个晶胞中的 未画出),则一个晶胞中的 个数为4 个数为4 |
您最近半年使用:0次
名校
解题方法
6 . 反应 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
A. 位于元素周期表 位于元素周期表 区 区 |
B.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
C.该反应的平衡常数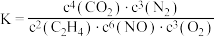 |
D.其他条件不变时,增大 , ,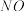 的平衡转化率下降 的平衡转化率下降 |
您最近半年使用:0次
名校
解题方法
7 . 近期科研人员研究发现,四苯基膦阳离子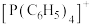 (结构如下)可与卤化镉(Cd)阴离子簇(卤素为Cl或Br)通过自组装形成多种杂化晶体材料,具有优异的发光特性。
(结构如下)可与卤化镉(Cd)阴离子簇(卤素为Cl或Br)通过自组装形成多种杂化晶体材料,具有优异的发光特性。_____ ,基态P原子电子占据的最高能级符号为_____ 。
(2)氯化四苯基膦可通过 和
和 反应得到。
反应得到。 是
是_____ (填“极性”或“非极性”)分子, 分子空间构型为
分子空间构型为_____ 。
(3)氯化四苯基膦( )在水中和有机溶剂中都有一定溶解性,其原因是
)在水中和有机溶剂中都有一定溶解性,其原因是_____ 。这一性质可使其用作不相溶的有机溶液和水溶液之间反应的催化剂。
(4)基态 原子的价电子排布式为
原子的价电子排布式为 ,
, 在元素周期表中的位置是
在元素周期表中的位置是_____ 。
(5)在上述晶体材料中,氯化镉阴离子以单体 或
或 形式存在,
形式存在,
_____ 。
(6)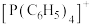 与
与 形成的杂化晶体材料中,存在的化学键有
形成的杂化晶体材料中,存在的化学键有_____ 。
(7)碘化镉晶胞示意图如下图所示。碘原子和镉原子分层排布,“一层镉、一层碘、一层碘”地相间。_____ 。
②镉原子的配位数是_____ 。
③碘化镉晶体很容易解离成片状,原因是_____ 。
(8)氧化镉晶体如下所示。已知晶胞边长为anm,阿伏加德罗常数为 ,该晶体密度为
,该晶体密度为_____  。(列计算式表达)
。(列计算式表达)
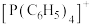 (结构如下)可与卤化镉(Cd)阴离子簇(卤素为Cl或Br)通过自组装形成多种杂化晶体材料,具有优异的发光特性。
(结构如下)可与卤化镉(Cd)阴离子簇(卤素为Cl或Br)通过自组装形成多种杂化晶体材料,具有优异的发光特性。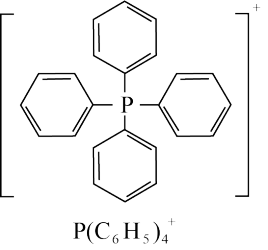
(2)氯化四苯基膦可通过
 和
和 反应得到。
反应得到。 是
是 分子空间构型为
分子空间构型为(3)氯化四苯基膦(
 )在水中和有机溶剂中都有一定溶解性,其原因是
)在水中和有机溶剂中都有一定溶解性,其原因是(4)基态
 原子的价电子排布式为
原子的价电子排布式为 ,
, 在元素周期表中的位置是
在元素周期表中的位置是(5)在上述晶体材料中,氯化镉阴离子以单体
 或
或 形式存在,
形式存在,
(6)
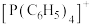 与
与 形成的杂化晶体材料中,存在的化学键有
形成的杂化晶体材料中,存在的化学键有(7)碘化镉晶胞示意图如下图所示。碘原子和镉原子分层排布,“一层镉、一层碘、一层碘”地相间。
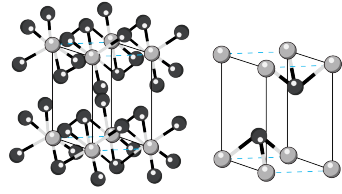
②镉原子的配位数是
③碘化镉晶体很容易解离成片状,原因是
(8)氧化镉晶体如下所示。已知晶胞边长为anm,阿伏加德罗常数为
 ,该晶体密度为
,该晶体密度为 。(列计算式表达)
。(列计算式表达)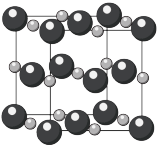
您最近半年使用:0次
解题方法
8 . 尿素还原法合成溴化锂,设备简单、产品质量好、无有毒气体排放、生产成本低。下图是制备无水溴化锂的工艺路线:
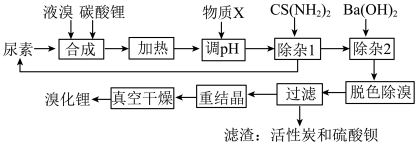
回答下列问题:
(1)Br位于周期表第________ 周期________ 族。
(2)常用焰色试验鉴别碳酸锂,火焰呈现________ 色。
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因________ 。
(4)合成溴化锂的主要化学方程式________ 。
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为________ 。
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是________ 。
(7)重结晶的操作为________ 。

温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
碳酸锂溶解度(g) | 1.51 | 1.43 | 1.33 | 1.26 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)Br位于周期表第
(2)常用焰色试验鉴别碳酸锂,火焰呈现
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因
(4)合成溴化锂的主要化学方程式
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是
(7)重结晶的操作为
您最近半年使用:0次
2024-04-02更新
|
294次组卷
|
2卷引用:2024届湖北省十一校高三下学期第二次联考化学试卷
9 . 固体化合物X由四种元素组成,某学习小组开展如下探究实验。下列说法错误的是
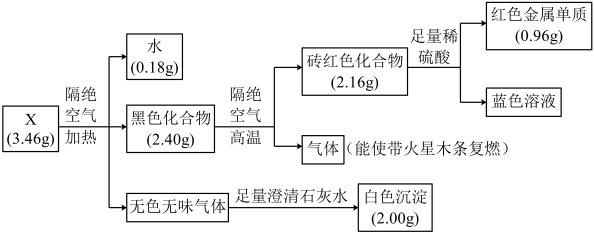
| A.固体化合物X中的金属元素位于周期表第四周期第ⅠB族 |
| B.固体化合物X为Cu2(OH)2CO3 |
| C.黑色化合物隔绝空气分解的过程中,生成1 mol砖红色化合物,转移2 mol电子 |
| D.蓝色溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可制得胆矾晶体 |
您最近半年使用:0次
名校
解题方法
10 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确 的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.乙的简单氢化物的沸点一定高于戊的简单氢化物的沸点 |
| C.甲的简单氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近半年使用:0次



