解题方法
1 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
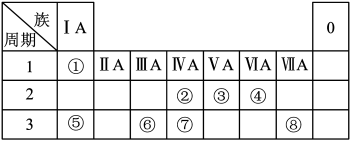
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的分子式为___________ ;⑦的最高价氧化物对应水化物的分子式为___________ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:___________ 、___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)半径大小比较:③___________ ④;金属性强弱比较:⑤___________ ⑥(填“>”、“<”或“=”)。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 | B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(5)半径大小比较:③
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
名校
解题方法
2 . 已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设X的原子序数为a,则下列说法不正确的是
| Y | ||
| X | ||
| Z |
| A.Y的原子序数可能为a-17 | B.Y与Z的原子序数之和可能为2a |
| C.Z的原子序数可能为a+31 | D.X、Y、Z可能均为短周期元素 |
您最近一年使用:0次
2023-06-18更新
|
963次组卷
|
8卷引用:陕西省渭南市华州区咸林中学2022-2023学年高一下学期期中考试化学试题
解题方法
3 . 现有四种短周期元素的有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为( )
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期序数 | 工业上用电解法冶炼该金属 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 单质是重要的半导体材料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质 | 丁的一种单质与KI溶液反应生成丁的另一种单质 |
| A.甲、乙、丙、丁 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.乙、甲、丁、丙 |
您最近一年使用:0次
2020-10-07更新
|
1538次组卷
|
4卷引用:陕西省西安市蓝田县乡镇学校联考2023-2024学年高一上学期1月期末化学试题
陕西省西安市蓝田县乡镇学校联考2023-2024学年高一上学期1月期末化学试题高一必修第一册(苏教2019版)专题5 高考挑战区四川省泸州合江县利城高级中学校2021-2022学年高一下学期第三次月考化学试题(已下线)第四章《物质结构 元素周期律》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)
4 . A、B、C是短周期ⅠA和ⅡA族元素的碳酸正盐,它们的质量分别为mA、mB、mC,与足量盐酸完全反应,消耗盐酸的物质的量分别为nA(HCl)、nB(HCl)、nC(HCl)。
已知:。mA=mB+mC,nA(HCl)=nB(HCl)+nC(HCl)。请填空:
(1)写出短周期ⅠA和ⅡA族元素形成的所有碳酸盐的名称:___ 。
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式___ 。
(3)A的正确选择有___ 种,其化学式为:___ 。
已知:。mA=mB+mC,nA(HCl)=nB(HCl)+nC(HCl)。请填空:
(1)写出短周期ⅠA和ⅡA族元素形成的所有碳酸盐的名称:
(2)若以MA、MB和MC分别表示A、B、C的相对分子质量,试写出MA、MB和MC三者的相互关系式
(3)A的正确选择有
您最近一年使用:0次
5 . 碳及其化合物在生产、生活中有广泛的用途。
I.金刚砂SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为____________ ,R的电子式为______________ ;
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为_____________ ,除去粗产品中少量钠的试剂为______________ ;
(3)碳还原制取SiC,其粗产品中杂质为Si和SiO2。先将20.0g SiC粗产品加入到过量NaOH溶液中充分反应,收集到0.1 mol氢气,过滤SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为____________________ ,硅酸盐的物质的量浓度为____________ 。
II.工业上向氨化的CaSO4悬浊液中通入适量CO2,可制取(NH4)2SO4,其流程如图所示。已知CaSO4的KSP=9.1×10-4,CaCO3的KSP=2.8×10-4。请回答:
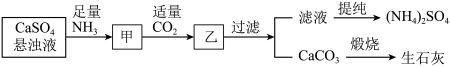
(1)向甲中通入过量CO2__________ (填“有”或“不”)利于CaCO3和(NH4)2SO4的生成,原因是_________________ 。
(2)直接蒸干滤液得到的(NH4)2SO4主要含有的杂质是____________ (填含量最多的一种)。
(3)锅炉水垢中含有的CaSO4,可先用Na2CO3溶液浸泡,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为___________________________ ;
②请分析CaSO4转化为CaCO3的原理:___________________________ 。
I.金刚砂SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为
(3)碳还原制取SiC,其粗产品中杂质为Si和SiO2。先将20.0g SiC粗产品加入到过量NaOH溶液中充分反应,收集到0.1 mol氢气,过滤SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为
II.工业上向氨化的CaSO4悬浊液中通入适量CO2,可制取(NH4)2SO4,其流程如图所示。已知CaSO4的KSP=9.1×10-4,CaCO3的KSP=2.8×10-4。请回答:

(1)向甲中通入过量CO2
(2)直接蒸干滤液得到的(NH4)2SO4主要含有的杂质是
(3)锅炉水垢中含有的CaSO4,可先用Na2CO3溶液浸泡,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为
②请分析CaSO4转化为CaCO3的原理:
您最近一年使用:0次
名校
6 . 一种新兴宝玉石主要成分的化学式为X2Y10Z12W30,X、Y、Z、W均为短周期主族元素且Y、W、X、Z的原子序数依次增大,X与Y位于同一主族,Y与W位于同一周期。X、Y、Z的最外层电子数之和与W的最外层电子数相等,W是地壳中含量最多的元素。下列说法错误的是
| A.原子半径:X>Y>W |
| B.最高价氧化物对应水化物的碱性:X>Y |
| C.Z、W组成的化合物能与强碱反应 |
| D.X的单质在氧气中燃烧所得的产物中阴、阳离子个数比为1:1 |
您最近一年使用:0次
2019-05-31更新
|
1226次组卷
|
5卷引用:陕西省韩城市司马迁中学2020届高三第四次模拟考试理综化学试题
陕西省韩城市司马迁中学2020届高三第四次模拟考试理综化学试题【市级联考】福建省福州市2019届高三第三次质量检测理科综合化学试题(已下线)专题06 物质结构 元素周期律——2019年高考真题和模拟题化学分项汇编吉林省吉化第一高级中学校2020-2021学年高二下学期3月月考化学试题吉林省延边第二中学2020-2021学年高二下学期第一次考试月考化学试题
7 . W、X、Y、Z为原子序数依次增大的短周期元素,已知W的一种氧化物常温下为液体,是与人类关系最密切的物质;X的一种核素可用于测定文物的年代;Y位于第三周期与Z相邻;在常温下,Z的单质是黄绿色气体。下列判断错误的是
| A.W与X形成的最简单化合物在与足量的Z单质反应时只生成一种产物 |
| B.最高价氧化物的水化物的酸性:Z>Y>X |
| C.Y的一种氧化物可能与O2反应生成Y的另一种氧化物 |
| D.W可以与某些元素形成二元离子化合物 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.碱金属随原子序数的增大,其熔沸点逐渐降低 |
B.卤素单质随原子序数的增大 ,其氧化性逐渐增强 ,其氧化性逐渐增强 |
| C.在周期表中,族序数都等于该族元素的最外层电子数 |
| D.非金属性最强的元素,其最高价氧化物对应水化物的酸性最强 |
您最近一年使用:0次
9 . 短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是
| W | X | |||
| Y | Z |
| A.氢化物沸点:W < Z | B.氧化物对应水化物的酸性:Y > W |
| C.化合物熔点:Y2X3 < YZ3 | D.简单离子的半径:Y < X |
您最近一年使用:0次
2017-08-08更新
|
10680次组卷
|
52卷引用:陕西省西安市铁一中2017-2018学年高一下学期期中考试化学试题
陕西省西安市铁一中2017-2018学年高一下学期期中考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)四川省双流中学2017-2018学年高二上学期开学考试化学试题四川省新津中学2018届高三上学期入学考试化学试题黑龙江省哈尔滨市第十八中学2018届高三第一次月考化学试题广西柳州市城中区第二中学2016-2017学年高一下学期期末考试化学试题河南省林州市第一中学2018届高三10月调研化学试题2017-2018学年人教版高中化学必修2单元测试题 第1章 物质结构 元素周期律(已下线)狂刷05 元素周期表和元素周期律的应用—《小题狂刷》2017-2018学年高一化学人教必修2(已下线)《考前20天终极攻略》-5月19日 物质结构 元素周期律(已下线)解密07 物质结构和元素周期律(教师版)——备战2018年高考化学之高频考点解密【全国百强校】四川省雅安中学2018-2019学年高一上学期开学考试化学试题【全国百强校】四川省雅安市雅安中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)【全国百强校】江西省南昌市第十中学2019届高三上学期期末考试理科综合化学试题(已下线)考点07 元素周期律和元素周期表——备战2019年浙江新高考化学考点吉林省长春市德惠市实验中学2018-2019学年高一下学期期初检测化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第二次月考化学试题步步为赢 高一化学暑假作业:作业十九 综合评估百所名校联考-物质结构 元素周期律四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训黑龙江省鸡西市鸡东县第二中学2019-2020学年高一下学期线上考试化学试题湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题四川省武胜烈面中学校2019-2020学年高二下学期期中考试化学试题黑龙江省大庆市第四中学2019-2020学年高二下学期第一次月考化学试题安徽省安庆市第一中学2019-2020学年高一下学期月考化学试题(已下线)5.1.1 元素周期律练习(1)——《高中新教材同步备课》(苏教版 必修第一册)黑龙江省哈尔滨师范大学附属中学2020-2021学年高二上学期开学考试化学试题苏教版(2020)高一必修第一册专题5 总结检测人教版(2019)高一必修第一册 第四章素养检测安徽省霍邱县第二中学2019-2020学年高一下学期段考化学试题(已下线)福建省泉州市泉港区第一中学2018-2019学年高二年级下学期期中考化学试题安徽省阜阳市第十一中学2019-2020学年高一下学期期中考试化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)专题5 第一单元综合拔高练-高中化学苏教2019版必修第一册云南省保山第九中学2021届高三上学期开学考试化学试题(已下线)小题13 元素周期表、律(根据元素周期表片段推断) ——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)【浙江新东方】双师208高一下(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)四川省汉源县第二中学2019-2020学年高二下学期第二次月考化学试题宁夏银川市第六中学2021-2022学年高三上学期第一次月考(9月)化学试题河南省南阳市第一中学校2021-2022学年高一下学期第三次月考化学试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)第四章 物质结构 元素周期律 本章复习提升(已下线)4.2元素周期律-同步学习必备知识四川省广元市八二一中学2021-2022学年高一下学期期中考试化学试题新疆维吾尔自治区喀什市喀什第二中学2022-2023学年高三上学期网上11月月考化学试题(已下线)题型76 通过元素周期表考查元素周期律四川省仁寿第一中学校南校区2022—2023学年高二下学期3月月考化学试题
10 . Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,Q元素的原子最外层电子数是其内层电子数的2倍,W、Z原子最外层电子数相同,Z的核电荷数是W的2倍,元素Y的合金是日常生活中使用最广泛的金属材料之一、下列说法正确的是
| A.简单离子半径的大小顺序:rX>rY>rZ>rW |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.Z元素氢化物的沸点高于W元素氢化物的沸点 |
| D.X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
您最近一年使用:0次



