名校
解题方法
1 . 反应 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
A. 位于元素周期表 位于元素周期表 区 区 |
B.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
C.该反应的平衡常数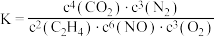 |
D.其他条件不变时,增大 , ,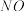 的平衡转化率下降 的平衡转化率下降 |
您最近一年使用:0次
名校
2 . 三氧化二锑,又称锑白,在工业上作阻燃剂、填充剂等,用途广泛。一种利用辉锑矿粉(含 及少量
及少量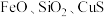 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
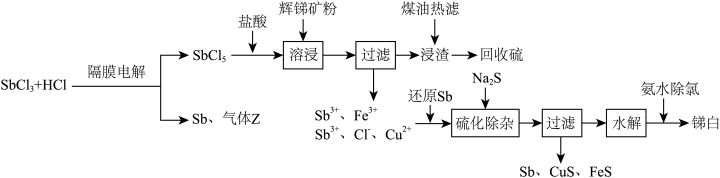
已知:①常温下,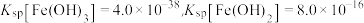 ,
, 。
。
②锑的常见价态为+3、+5价,其中 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。
(1)锑元素的原子序数为51,位于元素周期表第___________ 周期第___________ 族。
(2)溶浸时发生的主要反应的离子方程式为___________ 。
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是___________ 。
(4) 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:___________ ,锑白洗涤后便可干燥保存,检验洗净的试剂为___________ 。
(5)隔膜电解时,气体Z的分子式为___________ ;为平衡两极电荷,应使用___________ 交换膜(填“阴离子”“阳离子”或“质子”),理由是___________ 。
 及少量
及少量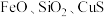 )制取锑白的工艺流程如图:
)制取锑白的工艺流程如图:
已知:①常温下,
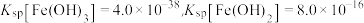 ,
, 。
。②锑的常见价态为+3、+5价,其中
 具有强氧化性,在溶液中能发生较剧烈的水解生成
具有强氧化性,在溶液中能发生较剧烈的水解生成 。
。(1)锑元素的原子序数为51,位于元素周期表第
(2)溶浸时发生的主要反应的离子方程式为
(3)加入还原Sb还原高价金属离子,能够提高产物锑白的纯度,原因是
(4)
 水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:
水解会生成多种物质,较为稳定的是SbOCl,写出SbOCl在稀氨水中最终生成锑白的化学方程式:(5)隔膜电解时,气体Z的分子式为
您最近一年使用:0次
2023-02-03更新
|
419次组卷
|
2卷引用:江苏省扬州中学2022-2023学年高三下学期开学摸底考试化学试题
名校
解题方法
3 . 短周期元素W、X、Y、Z、Q,原子序数依次增大,W原子没有中子,X元素为地壳中含量最多的元素,Y、Z、Q同周期,且Y、Z、Q最外层电子数之和为14,Y与W同主族,下列结论不正确的是
| A.原子半径大小顺序为Y>Z>Q>X>W |
| B.W、X、Y形成的化合物中只有共价键 |
| C.X、Y可以形成的原子个数比1:1或1:2的化合物 |
| D.最高价氧化物对应的水化物酸性Z﹤Q |
您最近一年使用:0次
2023-01-12更新
|
1045次组卷
|
4卷引用:江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题
江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题(已下线)专题09 原子结构 元素周期律和周期表-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用) 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题山东省青岛第十九中学2022-2023学年高一4月月考化学试题
4 . 据Nature Energy报道,最近科研人员研制出一种低浓度锂盐水系电解质溶液,充放电过程中锂离子具有较高的扩散速率,使得锂离子电池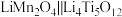 表现出优异的稳定性和放电容量。
表现出优异的稳定性和放电容量。
(1)对电极材料组成元素的分析。
①O原子核外电子有___________ 种运动状态。
②Mn元素位于元素周期表的___________ 区。
③基态Ti原子的核外电子排布式为___________ 。
(2)将 和
和 按
按 的物质的量比配料,经研磨后升温至600~750℃可制得电极材料
的物质的量比配料,经研磨后升温至600~750℃可制得电极材料 。
。
①该反应的化学方程式为___________ 。
② 中锰元素的平均价态为+3.5。不同温度下,合成的
中锰元素的平均价态为+3.5。不同温度下,合成的 中
中 、
、 和
和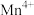 的含量与温度的关系见下表。
的含量与温度的关系见下表。
在上述温度范围内,锰元素平均价态的变化趋势为___________ 。
(3)以某种Ti的氧化物为原料,可制备正极材料尖晶石型钛酸锂( )。
)。
①Ti的氧化物晶胞结构如图所示,其化学式为___________ 。
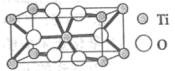
②电池放电过程中,钛酸锂(难溶于水)由尖晶石型转变为岩盐型(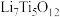 ),则正极的电极反应式为
),则正极的电极反应式为___________ 。
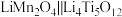 表现出优异的稳定性和放电容量。
表现出优异的稳定性和放电容量。(1)对电极材料组成元素的分析。
①O原子核外电子有
②Mn元素位于元素周期表的
③基态Ti原子的核外电子排布式为
(2)将
 和
和 按
按 的物质的量比配料,经研磨后升温至600~750℃可制得电极材料
的物质的量比配料,经研磨后升温至600~750℃可制得电极材料 。
。①该反应的化学方程式为
②
 中锰元素的平均价态为+3.5。不同温度下,合成的
中锰元素的平均价态为+3.5。不同温度下,合成的 中
中 、
、 和
和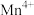 的含量与温度的关系见下表。
的含量与温度的关系见下表。| T/℃ | 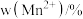 | 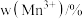 | 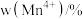 |
| 700 | 5.56 | 44.58 | 49.86 |
| 750 | 2.56 | 44.87 | 52.57 |
| 800 | 5.50 | 44.17 | 50.33 |
| 850 | 6.22 | 44.40 | 49.38 |
(3)以某种Ti的氧化物为原料,可制备正极材料尖晶石型钛酸锂(
 )。
)。①Ti的氧化物晶胞结构如图所示,其化学式为

②电池放电过程中,钛酸锂(难溶于水)由尖晶石型转变为岩盐型(
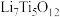 ),则正极的电极反应式为
),则正极的电极反应式为
您最近一年使用:0次
2022-06-29更新
|
228次组卷
|
2卷引用:江苏省常州市教育学会2021-2022学年高二下学期期末学业水平监测化学试题
解题方法
5 . 下表中的实线表示元素周期表的部分边界。①~⑤分别表示元素周期表中对应位置的元素。

(1)元素③④⑤的氢化物的稳定性由强到弱的顺序是____________________ (用氢化物的化学式表示)。
(2)元素③一般在化合物中显________ 价,但在与______ 形成化合物时,所显示的价态正好相反。
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式:____________________________________ 。
(4)X、Y、Z代表原子序数依次增大的三种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,请在上表中用元素符号标出不是①~⑤元素的相应位置。___________
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,表中除A、B、C、D外每个位置只表示一种元素。则该表中的A位置包含________ (填数字)种元素。C位置中的元素是否全部是金属元素________ (填“是”或“否”)。


(1)元素③④⑤的氢化物的稳定性由强到弱的顺序是
(2)元素③一般在化合物中显
(3)M、N两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式:
(4)X、Y、Z代表原子序数依次增大的三种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17;X、Y、Z三种元素有的是上表中编号①~⑤的元素,有的不是,请在上表中用元素符号标出不是①~⑤元素的相应位置。
(5)某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,表中除A、B、C、D外每个位置只表示一种元素。则该表中的A位置包含

您最近一年使用:0次
名校
6 . 短周期主族元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍。下列说法正确的是
| Y | Z | ||
| X | W |
| A.X的最高价氧化物是碱性氧化物 |
| B.Z、W均可与Mg形成离子化合物. |
| C.原子半径的大小顺序:r(Z)>r(Y)>r(X) |
| D.Y、Z、W的氧化物排放到空气中均会导致酸雨 |
您最近一年使用:0次
2017-05-03更新
|
385次组卷
|
3卷引用:江苏省宿迁市名校2016-2017学年高一下学期期中考试化学试题
7 . X、Y、Z、R是短周期主族元素,X原子最外层电子数为电子总数的2/3,Y原子最外层电子数是内层电子数的3倍, Z元素的单质常温下能与水反应产生氢气,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是
| A.原子半径的大小顺序:X>Y>Z>R |
| B.最高价氧化物的水化物的酸性:R>X |
| C.氢化物的稳定性:X>Y |
| D.Y与Z形成的两种化合物中的化学键和晶体类型均相同 |
您最近一年使用:0次
8 . 下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次



