23-24高三上·安徽·阶段练习
名校
解题方法
1 . 硅在自然界大部分以二氧化硅及硅酸盐的形式存在,它们的基本结构单位是硅氧四面体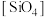 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
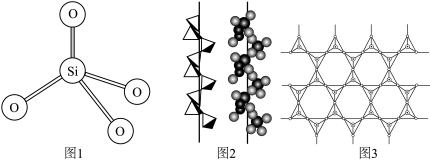
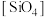 (图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
(图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种硅酸根阴离子结构(图3)。下列说法不正确的是
A.基态 原子的原子核外的电子有8种空间运动状态 原子的原子核外的电子有8种空间运动状态 |
| B.二氧化硅中硅原子的配位数是4 |
C.图2中Si原子的杂化轨道类型是 |
D.图3硅酸根阴离子结构中硅和氧的原子个数比为 |
您最近一年使用:0次
2023-12-01更新
|
324次组卷
|
3卷引用:T9-物质结构与性质
名校
解题方法
2 . 已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设X的原子序数为a,则下列说法不正确的是
| Y | ||
| X | ||
| Z |
| A.Y的原子序数可能为a-17 | B.Y与Z的原子序数之和可能为2a |
| C.Z的原子序数可能为a+31 | D.X、Y、Z可能均为短周期元素 |
您最近一年使用:0次
2023-06-18更新
|
962次组卷
|
8卷引用:2018-2019学年河南省洛阳市下学期第一次月考高一化学试题
3 . 按照要求回答下列问题。
(1)有下列物质: 、
、 、
、 、
、 、
、 、
、 、
、 。
。
①上述物质中既含共价键又含离子键的__________ ;属于共价化合物的是__________ ;
② 溶于水时破坏
溶于水时破坏__________ (填“共价键”或“离子键”,下同), 熔化时破坏
熔化时破坏__________ 。
(2)砷在元素周期表中的位置__________ 。原子序数为115的 中子数为
中子数为__________ 。
(3)向 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为__________ 。可证明非金属性:
__________ S(填“>”或“<”)。
(4)短周期元素Y的一种含氧酸化学式为 ,其结构式可表示为
,其结构式可表示为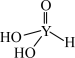 。该酸为
。该酸为__________ 元酸。写出该酸与过量 溶液反应的化学方程式:
溶液反应的化学方程式:__________ 。(用对应元素符号作答。已知信息:氢氧原子结合成的一种原子团“ ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
(1)有下列物质:
 、
、 、
、 、
、 、
、 、
、 、
、 。
。①上述物质中既含共价键又含离子键的
②
 溶于水时破坏
溶于水时破坏 熔化时破坏
熔化时破坏(2)砷在元素周期表中的位置
 中子数为
中子数为(3)向
 溶液中通入氯气出现黄色浑浊,反应的离子方程式为
溶液中通入氯气出现黄色浑浊,反应的离子方程式为
(4)短周期元素Y的一种含氧酸化学式为
 ,其结构式可表示为
,其结构式可表示为 。该酸为
。该酸为 溶液反应的化学方程式:
溶液反应的化学方程式: ”叫羟基,含氧酸中只有羟基氢才可电离出
”叫羟基,含氧酸中只有羟基氢才可电离出 )
)
您最近一年使用:0次
2023-03-24更新
|
649次组卷
|
3卷引用:河南省南阳市六校2022-2023学年高一下学期第一次联考化学试题
名校
解题方法
4 . 下列说法错误的是
| A.周期表中第5周期有18种元素 |
| B.①乙炔、②水、③甲醛、④氨四种分子中,键角由大到小的顺序是①>③>④>② |
| C.第4周期最外层有一个单电子的元素共有3种 |
D.两元素的基态原子的价电子排布式分别为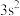 、 、 ,则一定为同一族元素 ,则一定为同一族元素 |
您最近一年使用:0次
2022-08-22更新
|
648次组卷
|
3卷引用:河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题
5 . 如图为元素周期表的一部分。请回答下列问题。
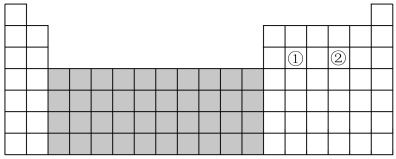
(1)图中阴影部分所示区域的元素称为____ 元素,下列元素属于该区域的是____ (填字母)。
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如表:
写出D元素在元素周期表中的位置____ 。
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为____ ;由F的化合物生成A的单质的化学方程式为____ 。
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25g•L-1,该气体的摩尔质量为____ 。
(5)下列说法不正确 的是____ 。
(6)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式____ 。

(1)图中阴影部分所示区域的元素称为
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如表:
| 元素 | A | B | C | D | E | F |
| 化合价 | -2 | +5、-3 | +4、-4 | +6、-2 | +2 | +1 |
| 原子半径/nm | 0.074 | 0.075 | 0.077 | 0.102 | 0.160 | 0.186 |
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25g•L-1,该气体的摩尔质量为
(5)下列说法
| A.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族 |
| B.第5周期第ⅤA族元素的原子序数为65 |
| C.②形成的最简单氢化物比①形成的最简单氢化物的稳定性高 |
| D.周期表中当某元素的周期序数大于其族序数时,该元素可能属于金属或非金属 |
您最近一年使用:0次
名校
6 . X、Y、Z是周期表中位置相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为16,核内质子数之和为30,则X、Y、Z分别是( )
| A.O、N、P | B.S、P、N | C.N、O、S | D.Cl、S、O |
您最近一年使用:0次
2020-09-23更新
|
1988次组卷
|
5卷引用:河南省平顶山一中新区学校2020-2021学年高一上学期教学质量评估(二)化学试题
河南省平顶山一中新区学校2020-2021学年高一上学期教学质量评估(二)化学试题鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律第2节 元素周期律和元素周期表(已下线)4.1.2 元素周期表(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)云南省曲靖市会泽县实验高级中学校2022-2023学年高一下学期月考(四)化学试题天津市第五十四中学2023-2024学年高一上学期第二次月考(12月考)化学试题
7 . 下列说法正确的是
| A.氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少 |
| B.最外层电子数为ns2的元素都在元素周期表第2列 |
C.处于最低能量的原子叫做基态原子,1s22s22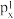 →1s22s22 →1s22s22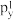 过程中形成的是发射光谱 过程中形成的是发射光谱 |
| D.已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素位于周期表中的第四周期第VIII族位置,属于ds区 |
您最近一年使用:0次
2019-07-15更新
|
2326次组卷
|
7卷引用:河南省焦作市第一中学2022-2023学年高二下学期3月份教学质量检测 化学试题
解题方法
8 . 在元素周期表中,非金属元素集中于右上角的位置,它们虽然种类少,但其用途却不容小觑。
(1)元素周期表的非金属元素中,属于主族元素的共有________ 种。
(2)红磷是巨型共价分子、无定型结构。能证明红磷是非晶体的最可靠方法是________ 。
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X 射线衍射
(3)成语“信口雕黄”中的雌黄分子式为As2S3,分子结构如右图。
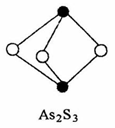
其分子中S原子的杂化方式为________ 。雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应的化学方程式______ 。
(4)已知pKa=-lgKa。
①有机酸的酸性强弱受邻近碳上取代原子的影响,如酸性: BrCH2COOH >CH3COOH。据此推测,pKa:ClCH2COOH______ FCH2COOH(填“>”、“<”、“=”)。
②硼酸(H3BO3)是一元酸,它在水中表现出来的弱酸性,并不是自身电离出H+所致,而是H3BO3与水电离出的OH-结合生成一个酸根离子,请写出该酸根离子的结构简式:________ (若存在配位键,请用箭头标出)。
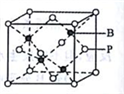
(5)磷化硼的晶胞模型如右图所示,晶胞参数为a pm,已知B、P的原子半径分别表示为rBpm、rP pm。该晶胞中磷原子的配位数为________ ,晶体中原子的空间利用率为______ 。
(1)元素周期表的非金属元素中,属于主族元素的共有
(2)红磷是巨型共价分子、无定型结构。能证明红磷是非晶体的最可靠方法是
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X 射线衍射
(3)成语“信口雕黄”中的雌黄分子式为As2S3,分子结构如右图。

其分子中S原子的杂化方式为
(4)已知pKa=-lgKa。
①有机酸的酸性强弱受邻近碳上取代原子的影响,如酸性: BrCH2COOH >CH3COOH。据此推测,pKa:ClCH2COOH
②硼酸(H3BO3)是一元酸,它在水中表现出来的弱酸性,并不是自身电离出H+所致,而是H3BO3与水电离出的OH-结合生成一个酸根离子,请写出该酸根离子的结构简式:
(5)磷化硼的晶胞模型如右图所示,晶胞参数为a pm,已知B、P的原子半径分别表示为rBpm、rP pm。该晶胞中磷原子的配位数为

您最近一年使用:0次
名校
9 . 具有以下结构的原子一定属于p区元素的是( )
①最外层有3个电子的原子 ②最外层电子排布式为ns2的原子 ③最外层有3个未成对电子的原子 ④最外层电子形成全满结构的原子
①最外层有3个电子的原子 ②最外层电子排布式为ns2的原子 ③最外层有3个未成对电子的原子 ④最外层电子形成全满结构的原子
| A.②③ | B.①③ |
| C.②④ | D.①④ |
您最近一年使用:0次
2018-05-02更新
|
782次组卷
|
7卷引用:河南省新乡市河南师范大学附属中学2021-2022学年高二下学期3月月考化学试题
名校
解题方法
10 . 核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q,其中在同周期中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示
(1)五种元素形成的单质,其中固态时属于原子晶体的是________ (填化学式);常用作强氧化剂的是________ 、________ (填化学式)。
(2)这五种元素中,原子半径最大的是________ (填化学式);由Z、W、Q形成的简单离子半径由大到小的顺序是________ (用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序是________ (用化学式表示)。
(3)Y和Z形成的一种化合物中含有离子键和共价键,请用电子书表示该化合物中化学键的形成过程___________________________________ 。
(4)Z与Q反应生成的化合物属于________ 化合物;电解该化合物的饱和溶液,阳极的电极反应式为________ ;电解一段时间后,将阳极产物和阴极溶液混合,反应的化学方程式是______________ 。
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧放出140 kJ的热,写出该化合物燃烧热的热化学方程式:_______________________________ 。

(1)五种元素形成的单质,其中固态时属于原子晶体的是
(2)这五种元素中,原子半径最大的是
(3)Y和Z形成的一种化合物中含有离子键和共价键,请用电子书表示该化合物中化学键的形成过程
(4)Z与Q反应生成的化合物属于
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧放出140 kJ的热,写出该化合物燃烧热的热化学方程式:
您最近一年使用:0次



