在元素周期表中,非金属元素集中于右上角的位置,它们虽然种类少,但其用途却不容小觑。
(1)元素周期表的非金属元素中,属于主族元素的共有________ 种。
(2)红磷是巨型共价分子、无定型结构。能证明红磷是非晶体的最可靠方法是________ 。
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X 射线衍射
(3)成语“信口雕黄”中的雌黄分子式为As2S3,分子结构如右图。
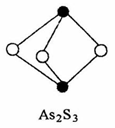
其分子中S原子的杂化方式为________ 。雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应的化学方程式______ 。
(4)已知pKa=-lgKa。
①有机酸的酸性强弱受邻近碳上取代原子的影响,如酸性: BrCH2COOH >CH3COOH。据此推测,pKa:ClCH2COOH______ FCH2COOH(填“>”、“<”、“=”)。
②硼酸(H3BO3)是一元酸,它在水中表现出来的弱酸性,并不是自身电离出H+所致,而是H3BO3与水电离出的OH-结合生成一个酸根离子,请写出该酸根离子的结构简式:________ (若存在配位键,请用箭头标出)。
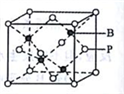
(5)磷化硼的晶胞模型如右图所示,晶胞参数为a pm,已知B、P的原子半径分别表示为rBpm、rP pm。该晶胞中磷原子的配位数为________ ,晶体中原子的空间利用率为______ 。
(1)元素周期表的非金属元素中,属于主族元素的共有
(2)红磷是巨型共价分子、无定型结构。能证明红磷是非晶体的最可靠方法是
A.质谱 B.原子发射光谱 C.核磁共振谱 D.X 射线衍射
(3)成语“信口雕黄”中的雌黄分子式为As2S3,分子结构如右图。

其分子中S原子的杂化方式为
(4)已知pKa=-lgKa。
①有机酸的酸性强弱受邻近碳上取代原子的影响,如酸性: BrCH2COOH >CH3COOH。据此推测,pKa:ClCH2COOH
②硼酸(H3BO3)是一元酸,它在水中表现出来的弱酸性,并不是自身电离出H+所致,而是H3BO3与水电离出的OH-结合生成一个酸根离子,请写出该酸根离子的结构简式:
(5)磷化硼的晶胞模型如右图所示,晶胞参数为a pm,已知B、P的原子半径分别表示为rBpm、rP pm。该晶胞中磷原子的配位数为

更新时间:2018-06-20 19:48:41
|
相似题推荐
【推荐1】据Nature Energy报道,最近科研人员研制出一种低浓度锂盐水系电解质溶液,充放电过程中锂离子具有较高的扩散速率,使得锂离子电池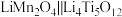 表现出优异的稳定性和放电容量。
表现出优异的稳定性和放电容量。
(1)对电极材料组成元素的分析。
①O原子核外电子有___________ 种运动状态。
②Mn元素位于元素周期表的___________ 区。
③基态Ti原子的核外电子排布式为___________ 。
(2)将 和
和 按
按 的物质的量比配料,经研磨后升温至600~750℃可制得电极材料
的物质的量比配料,经研磨后升温至600~750℃可制得电极材料 。
。
①该反应的化学方程式为___________ 。
② 中锰元素的平均价态为+3.5。不同温度下,合成的
中锰元素的平均价态为+3.5。不同温度下,合成的 中
中 、
、 和
和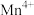 的含量与温度的关系见下表。
的含量与温度的关系见下表。
在上述温度范围内,锰元素平均价态的变化趋势为___________ 。
(3)以某种Ti的氧化物为原料,可制备正极材料尖晶石型钛酸锂( )。
)。
①Ti的氧化物晶胞结构如图所示,其化学式为___________ 。
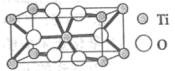
②电池放电过程中,钛酸锂(难溶于水)由尖晶石型转变为岩盐型(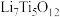 ),则正极的电极反应式为
),则正极的电极反应式为___________ 。
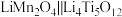 表现出优异的稳定性和放电容量。
表现出优异的稳定性和放电容量。(1)对电极材料组成元素的分析。
①O原子核外电子有
②Mn元素位于元素周期表的
③基态Ti原子的核外电子排布式为
(2)将
 和
和 按
按 的物质的量比配料,经研磨后升温至600~750℃可制得电极材料
的物质的量比配料,经研磨后升温至600~750℃可制得电极材料 。
。①该反应的化学方程式为
②
 中锰元素的平均价态为+3.5。不同温度下,合成的
中锰元素的平均价态为+3.5。不同温度下,合成的 中
中 、
、 和
和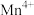 的含量与温度的关系见下表。
的含量与温度的关系见下表。| T/℃ | 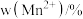 | 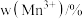 | 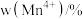 |
| 700 | 5.56 | 44.58 | 49.86 |
| 750 | 2.56 | 44.87 | 52.57 |
| 800 | 5.50 | 44.17 | 50.33 |
| 850 | 6.22 | 44.40 | 49.38 |
(3)以某种Ti的氧化物为原料,可制备正极材料尖晶石型钛酸锂(
 )。
)。①Ti的氧化物晶胞结构如图所示,其化学式为

②电池放电过程中,钛酸锂(难溶于水)由尖晶石型转变为岩盐型(
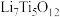 ),则正极的电极反应式为
),则正极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界存在多种A的化合物,B原子核外电子由6种不同的运动状态,B与C可形成正四面体形分子,D的M能层没有空轨道且只有2个未成对电子。请回答下列问题:
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为________ 。
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有________ 个六元环;图2位在元素周期表中与B相邻的元素位置关系,B、G形成的晶胞结构如图3所示(其中“●”为B元素原子,“〇”为G元素原子),图中“●”点构成的堆积方式与图4中_____ (填序号)所表示的堆积方式相同;图3的结构中,设晶胞边长为a cm,B原子直径为bcm,G原子直径为c cm,则该晶胞的空间利用率为_______ (用含a、b、c的式子表示)。

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式_____ (用化学式表示)。
(4)元素C的含氧酸中,酸性最强的是_________ (写化学式),该酸根离子的立体构型为________ 。
(5)基态D原子的核外电子排布式为[Ar]_______ ;D形成的配合物D(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______ ;由D一铝合金为原料可制得一种历史悠久、应用广泛的催化剂,其催化的i实例为: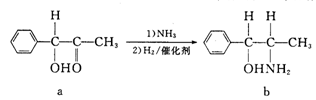 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有__________ (填元素符号)。
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式
(4)元素C的含氧酸中,酸性最强的是
(5)基态D原子的核外电子排布式为[Ar]
 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体。
(1)铁、钴、镍均位于元素周期表______ 区, 基态Co的价电子排布式为______ 。
(2)Fe、Co、Ni化学性质相似的原因是______ 。
(3)配位离子[Co(NO3)4]2-中,N的杂化方式为______ ,该配离子中各元素的第一电离能的大小顺序为______ ,1mol该配离子中含键数目为______ 。
(4)Ni(CO)4的结构与相关性质见表,其空间构型为______ ,晶体类型为______ 晶体。
(5)Sm(钐)、Ni、O形成的稀土镍基氧化物具有金属→绝缘体相转变特性,其晶胞结构中Sm和O如图所示,Ni位于O形成正八面体空隙中,则该稀土镍基氧化物的化学式为______ ,设晶胞边长为a pm,该稀土氧化物的摩尔质量为M g/mol,NA为阿伏加德罗常数的值,则该氧化物的密度为______ g/cm3(用含a、M、NA的式子表示)。
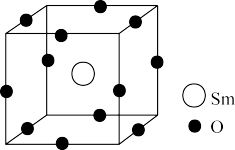
(1)铁、钴、镍均位于元素周期表
(2)Fe、Co、Ni化学性质相似的原因是
(3)配位离子[Co(NO3)4]2-中,N的杂化方式为
(4)Ni(CO)4的结构与相关性质见表,其空间构型为
| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 | -19.3℃ | 43℃ |  |

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】Cu及其化合物在医药、催化、材料等领域有广泛应用。回答下列问题:
(1)通过如图1所示反应可以实现铜离子的富集,进行回收。
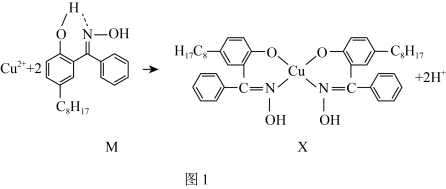
①与Cu元素同周期,基态原子有2个未成对电子的金属元素有____ 种。下列状态的铜中,电离最外层一个电子所需能量最高的是______ (填序号)。
a.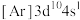 b.
b.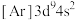 c.
c. d.
d.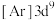 e.
e.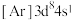
②化合物X中的中心铜离子的配位数是_____ ,图1反应中断裂和生成的化学键有____ (填序号)。
a.离子键 b.p—p 键 c.极性键 d.氢键 e.配位键
键 c.极性键 d.氢键 e.配位键
③M所含元素的第一电离能由大到小顺序是_____ (用元素符号表示)。
(2)4−甲基咪唑(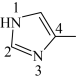 )也可与
)也可与 形成配合物,4−甲基咪唑分子中1号N原子的孤电子对因参与形成大
形成配合物,4−甲基咪唑分子中1号N原子的孤电子对因参与形成大 键,电子云密度降低。1号N原子杂化方式为
键,电子云密度降低。1号N原子杂化方式为______ ,_____ (填“1”或“3”)号N原子更容易与 形成配位键。
形成配位键。
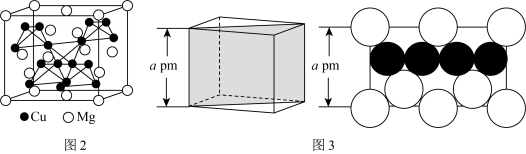
(3)图2是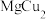 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图3是沿立方格子对角面取得的截面。Mg原子的半径为
的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图3是沿立方格子对角面取得的截面。Mg原子的半径为____ pm,该晶胞中原子的空间利用率为______ 。
(1)通过如图1所示反应可以实现铜离子的富集,进行回收。

①与Cu元素同周期,基态原子有2个未成对电子的金属元素有
a.
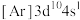 b.
b.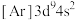 c.
c. d.
d.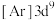 e.
e.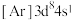
②化合物X中的中心铜离子的配位数是
a.离子键 b.p—p
 键 c.极性键 d.氢键 e.配位键
键 c.极性键 d.氢键 e.配位键③M所含元素的第一电离能由大到小顺序是
(2)4−甲基咪唑(
 )也可与
)也可与 形成配合物,4−甲基咪唑分子中1号N原子的孤电子对因参与形成大
形成配合物,4−甲基咪唑分子中1号N原子的孤电子对因参与形成大 键,电子云密度降低。1号N原子杂化方式为
键,电子云密度降低。1号N原子杂化方式为 形成配位键。
形成配位键。(3)图2是
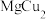 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图3是沿立方格子对角面取得的截面。Mg原子的半径为
的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图3是沿立方格子对角面取得的截面。Mg原子的半径为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
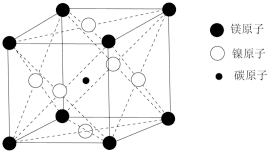
【推荐3】最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。
(1)该新型超导晶体的一个晶胞如图所示,则该晶体的化学式是__________ 。镍在元素周期表中的位置是______ ,Ni2+的价电子有_________ 种不同运动状态。
(2)500-600℃时,BeCl2以双聚分子存在的BeCl2的结构式为________________________ 。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于______ 晶体,配体是______ 该配合物中存在的作用力类型有___________ (填标号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
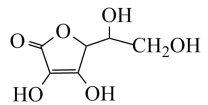
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_______ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(5)副族元素Zn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中为( 为Se,
为Se, 为Zn),Zn的配位数为
为Zn),Zn的配位数为______ ,该晶体的密度为 g/cm3,则Zn—Se键的键长为
g/cm3,则Zn—Se键的键长为______ nm。
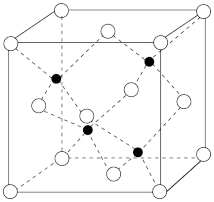
(1)该新型超导晶体的一个晶胞如图所示,则该晶体的化学式是

(2)500-600℃时,BeCl2以双聚分子存在的BeCl2的结构式为
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

(5)副族元素Zn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中为(
 为Se,
为Se, 为Zn),Zn的配位数为
为Zn),Zn的配位数为 g/cm3,则Zn—Se键的键长为
g/cm3,则Zn—Se键的键长为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】铂(Pt)可以和很多化合物形成配合物。生产生活中有重要的用途。
(1)铂和氨水可以形成配合物用于提取铂。氨水中各元素的第一电离能从大到小的顺序为_______ 。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体,科学研究表明,反式分子和顺式分子同样具有抗癌活性。
①Cl-的核外电子排布式为_______ 。
②吡啶分子是大体积平面配体。其结构简式为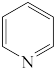 ,吡啶分子中氮原子的轨道杂化方式是
,吡啶分子中氮原子的轨道杂化方式是_______ ,分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数。n代表参与形成大π键的电子数。则吡啶中的大π键应表示为
表示,其中m代表参与形成大π键的原子数。n代表参与形成大π键的电子数。则吡啶中的大π键应表示为_______ ;1 mol吡啶中含有σ键的数目为_______ 。
③二氯二吡啶合铂分子中存在的微粒间作用力有_______ (填字母)。
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键 f.极性键
④二氯二吡啶合铂分子中,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3。简述理由:_______ 。
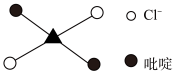
⑤反式二氯二吡啶合铂分子结构如图所示,该分子是_______ 分子(填“极性”或“非极性”)。
(1)铂和氨水可以形成配合物用于提取铂。氨水中各元素的第一电离能从大到小的顺序为
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体,科学研究表明,反式分子和顺式分子同样具有抗癌活性。
①Cl-的核外电子排布式为
②吡啶分子是大体积平面配体。其结构简式为
 ,吡啶分子中氮原子的轨道杂化方式是
,吡啶分子中氮原子的轨道杂化方式是 表示,其中m代表参与形成大π键的原子数。n代表参与形成大π键的电子数。则吡啶中的大π键应表示为
表示,其中m代表参与形成大π键的原子数。n代表参与形成大π键的电子数。则吡啶中的大π键应表示为③二氯二吡啶合铂分子中存在的微粒间作用力有
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键 f.极性键
④二氯二吡啶合铂分子中,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3。简述理由:
⑤反式二氯二吡啶合铂分子结构如图所示,该分子是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】金属镍及其化合物在合成材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态Ni原子的核外电子排布图为___________
(2)NiO、FeO晶体类型及晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为___________ ;又知Ni2+、Fe2+的离子半径分别为69pm、78pm,则NiO熔点___________ FeO(填“>”“<”或“=”)。
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中C原子的杂化类型为___________ ;元素H、C、N、O、Ni电负性由大到小的顺序为___________ 。___________ ;晶体密度为___________ g·cm-3(列出含a、b、NA的计算表达式,NA表示阿伏加德罗常数的值)。
(1)基态Ni原子的核外电子排布图为
(2)NiO、FeO晶体类型及晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中C原子的杂化类型为
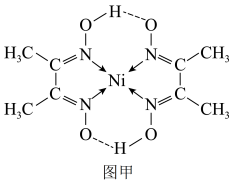
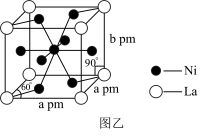
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】已知A、B、C、D、E五种元素是元素周期表中前四周期元素,且原子序数依次增大,其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子。 D、E 为同周期元素且分别位于s区和d区。五种元素所有的s能级电子均为全充满。E的d能级电子数比A、B、C最高能层的P能级电子数之和少一个。回答下列问题:
(1)五种元素中,电负性最大的是___________________ (填元素符号)。
(2)E常有+2、+3两种价态,写出E2+的最外层电子排布式________________________ 。
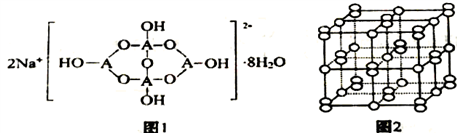
(3)自然界中,含A的钠盐是一种天然矿藏,其化学式写作Na2A4O7·10H2O,实际上它的结构单元是由两个H3AO3和两个[A(OH)4]-缩合而成的双六元环,应该写成Na2A4O5(OH)4·8H2O,其结构如图1。①A原子的杂化轨道类型为_______________________________ 。
②该阴离子由极性键和配位键构成,请在图1中用“→”标出其中的配位键____________ 。
③已知H3AO3为一元弱酸,根据上述信息,用离子方程式解释分析H3AO3为一元酸的原因(用元素符号表示)____________________________________ 。
(4)①写出ECl3与苯酚(C6H5OH)反应生成[E(OC6H5)6]3-的化学方程式:________________________ 。
②请从分子结构的角度解释苯酚室温下在水中的溶解度小,当温度高于65℃时,能与水混溶:_______________________________________________________ 。
(5)由元素B、D组成的某离子化合物的晶胞结构如图2,写出该物质的电子式_____________________ ,若晶胞的长、宽、高分别为520pm、520pm和690pm,该晶体密度为______________ g/cm3(保留到小数点后两位)。
(1)五种元素中,电负性最大的是
(2)E常有+2、+3两种价态,写出E2+的最外层电子排布式
(3)自然界中,含A的钠盐是一种天然矿藏,其化学式写作Na2A4O7·10H2O,实际上它的结构单元是由两个H3AO3和两个[A(OH)4]-缩合而成的双六元环,应该写成Na2A4O5(OH)4·8H2O,其结构如图1。①A原子的杂化轨道类型为
②该阴离子由极性键和配位键构成,请在图1中用“→”标出其中的配位键
③已知H3AO3为一元弱酸,根据上述信息,用离子方程式解释分析H3AO3为一元酸的原因(用元素符号表示)
(4)①写出ECl3与苯酚(C6H5OH)反应生成[E(OC6H5)6]3-的化学方程式:
②请从分子结构的角度解释苯酚室温下在水中的溶解度小,当温度高于65℃时,能与水混溶:
(5)由元素B、D组成的某离子化合物的晶胞结构如图2,写出该物质的电子式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】锰(Mn)、钴(Co)、镍(Ni)等过渡金属元素化合物的应用研究是前沿科学之一,回答下列问题:
(1)Mn的价电子排布式为___________ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用“___________ 理论”解释。
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列___________ (填序号),每个Mn原子周围紧邻的原子数为___________ 。
A.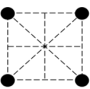 B.
B.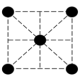 C.
C.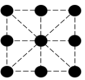 D.
D.
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为SO(CH3)2。DMSO中硫原子的杂化轨道类型为___________ ,SO(CH3)2中键角∠C—S—O___________ CH3COCH3中键角∠C—C—O(填“大于”“小于”或“等于”),ClO 的空间构型是
的空间构型是___________ ,元素S、Cl、O的电负性由大到小的顺序为___________ 。
(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(CH2=CH—CH2OH),其相对分子质量等于丙醛(CH3CH2CHO),但两者沸点相差较大,原因是___________ 。
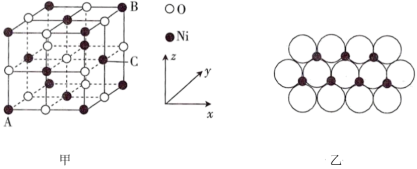
(5)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为___________ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为apm,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为___________ g(用含a、NA的代数式表示)。
(1)Mn的价电子排布式为
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列
A.
 B.
B. C.
C. D.
D.
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为SO(CH3)2。DMSO中硫原子的杂化轨道类型为
 的空间构型是
的空间构型是(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(CH2=CH—CH2OH),其相对分子质量等于丙醛(CH3CH2CHO),但两者沸点相差较大,原因是
(5)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
(1)基态硼原子的电子排布式为_______ ,占据最高能级的电子云轮廓图为_______ 形。
(2)氨硼烷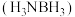 是目前最具潜力的储氢材料之一。
是目前最具潜力的储氢材料之一。
①氨硼烷能溶于水,其主要原因是_______ 。
② 分子中存在配位键,提供孤电子对的原子是
分子中存在配位键,提供孤电子对的原子是_______ (填元素符号);与 互为等电子体的分子
互为等电子体的分子_______ (任写一种满足条件的分子式)。
③氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“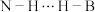 ”表示。以下物质之间可能形成双氢键的是
”表示。以下物质之间可能形成双氢键的是_______ 。
A. 和
和 B.LiH和HCN C.
B.LiH和HCN C. 和
和 D.
D. 和
和
(3)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图1所示,它的阴离子可形成链状结构,阴离子中B原子的杂化轨道类型为
,其结构如图1所示,它的阴离子可形成链状结构,阴离子中B原子的杂化轨道类型为_______ ,该晶体中不存在的作用力是_______ (填字母)。
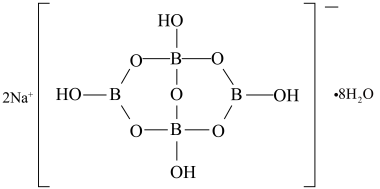
A.离子键B.共价键C.氢键D.金属键
(4)硼氢化钠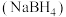 是一种常用的还原剂,其晶胞结构如图2所示:
是一种常用的还原剂,其晶胞结构如图2所示:

① 的配位数是
的配位数是_______ 。
②已知硼氢化钠晶体的密度为 ,
, 代表阿伏加德罗常数的值,则
代表阿伏加德罗常数的值,则 与
与 之间的最近距离为
之间的最近距离为_______ nm(用含 、
、 的代数式表示)。
的代数式表示)。
③若硼氢化钠晶胞上下底心处的 被
被 取代,得到晶体的化学式为
取代,得到晶体的化学式为_______ 。
(1)基态硼原子的电子排布式为
(2)氨硼烷
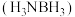 是目前最具潜力的储氢材料之一。
是目前最具潜力的储氢材料之一。①氨硼烷能溶于水,其主要原因是
②
 分子中存在配位键,提供孤电子对的原子是
分子中存在配位键,提供孤电子对的原子是 互为等电子体的分子
互为等电子体的分子③氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“
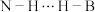 ”表示。以下物质之间可能形成双氢键的是
”表示。以下物质之间可能形成双氢键的是A.
 和
和 B.LiH和HCN C.
B.LiH和HCN C. 和
和 D.
D. 和
和
(3)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作
 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图1所示,它的阴离子可形成链状结构,阴离子中B原子的杂化轨道类型为
,其结构如图1所示,它的阴离子可形成链状结构,阴离子中B原子的杂化轨道类型为
A.离子键B.共价键C.氢键D.金属键
(4)硼氢化钠
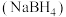 是一种常用的还原剂,其晶胞结构如图2所示:
是一种常用的还原剂,其晶胞结构如图2所示:
①
 的配位数是
的配位数是②已知硼氢化钠晶体的密度为
 ,
, 代表阿伏加德罗常数的值,则
代表阿伏加德罗常数的值,则 与
与 之间的最近距离为
之间的最近距离为 、
、 的代数式表示)。
的代数式表示)。③若硼氢化钠晶胞上下底心处的
 被
被 取代,得到晶体的化学式为
取代,得到晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】“刀片电池”通过结构创新,大大提升了磷酸铁锂电池的能量密度。以下是以磷矿石(主要成分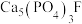 ,还有
,还有 、
、 ,等杂质)为原料生产白磷(
,等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程:
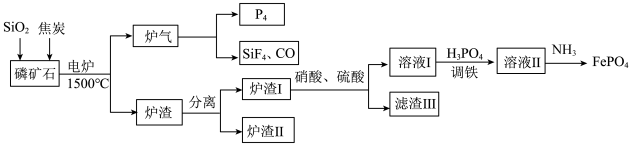
已知: 可溶于强酸性溶液。
可溶于强酸性溶液。
回答下列问题:
(1)白磷( )不溶于水但易溶于二硫化碳,说明
)不溶于水但易溶于二硫化碳,说明 是
是___________ (填“极性分子”或“非极性分子”)。
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中 溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:___________ 。
(3)炉渣Ⅱ的主要成分是___________ 。
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是___________ 。若此条件下 恰好完全转化为
恰好完全转化为 沉淀(当溶液中某离子浓度
沉淀(当溶液中某离子浓度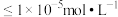 时,可视为该离子沉淀完全),求此时溶液中
时,可视为该离子沉淀完全),求此时溶液中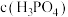 =
=___________ 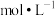 (已知
(已知 的
的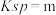 ;
; 的电离平衡常数为:
的电离平衡常数为: ,
,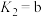 ,
,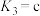 )。
)。
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:
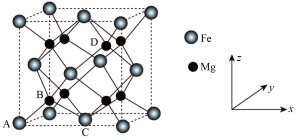
其中A的原子坐标参数为(0,0,0),B为( ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为___________ 。该晶胞沿体对角线方向的投影图为___________ 。
A.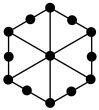 B.
B.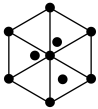 C.
C.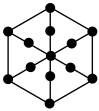 D.
D.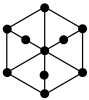
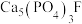 ,还有
,还有 、
、 ,等杂质)为原料生产白磷(
,等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程:
已知:
 可溶于强酸性溶液。
可溶于强酸性溶液。回答下列问题:
(1)白磷(
 )不溶于水但易溶于二硫化碳,说明
)不溶于水但易溶于二硫化碳,说明 是
是(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中
 溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:(3)炉渣Ⅱ的主要成分是
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是
 恰好完全转化为
恰好完全转化为 沉淀(当溶液中某离子浓度
沉淀(当溶液中某离子浓度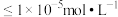 时,可视为该离子沉淀完全),求此时溶液中
时,可视为该离子沉淀完全),求此时溶液中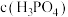 =
=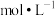 (已知
(已知 的
的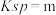 ;
; 的电离平衡常数为:
的电离平衡常数为: ,
,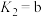 ,
,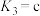 )。
)。(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:

其中A的原子坐标参数为(0,0,0),B为(
 ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次



